
- •Міністерство освіти і науки україни
- •Номенклатура комплексних сполук.
- •Природа координаційного зв’язку
- •Класифікація комплексних сполук.
- •Дисоціація комплексних сполук у розчинах. Стійкість комплексних іонів.
- •Ізомерія комплексних сполук.
- •Властивості комплексних сполук.
- •Основні способи одержання комплексних сполук.
- •Значення та застосування комплексних сполук.
- •Практична частина.
- •Лабораторна робота “Комплексні сполуки”.
- •Запитання для самоконтролю
- •Задачі для самоконтролю
- •Література
Ізомерія комплексних сполук.
Ізомери – сполуки однакового якісного та кількісного складу, але з різними фізико-хімічними властивостями. Причиною ізомерії є різне розташування лігандів навколо комплексоутворювача у внутрішній та зовнішній сферах.
Розрізняють такі види ізомерії: геометрична (цис-, транс-), координаційна, гідратна, іонізаційна, сольватна, оптична, полімерія.
І. Геометрична (цис-, транс-) ізомерія має місце для комплексів з різнорідними лігандами. Для сполуки складу [Pt(NH3)2Cl2] можливі два геометричні ізомери:
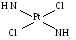
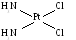
цис-ізомер транс-ізомер
оранжевого кольору світложовтого кольору
ІІ. Координаційна ізомерія виявляється в різній
координації двох типів лігандів відносно двох різних комплексоутворювачів.
Наприклад:
[Cu(NH3)4][PtCl4] та [Pt(NH3)4][CuCl4]
сполука фіолетового сполука зеленого
кольору кольору
ІІІ. Гідратна ізомерія полягає в неоднаковому розподілі молекул води між внутрішньою та зовнішньою сферами координаційної сполуки. Наприклад:
[Cr(H2O)6]Cl3 [Cr(H2O)5Cl]Cl2 · H2O
синьо-сірий світло-зелений
колір колір
[Cr(H2O)4Cl2]Cl · 2H2O
темно-зелений колір
IV. Іонізаційна ізомерія виражається в неоднаковому розподілі аніонів між зовнішньою та внутрішньою сферами комплексної сполуки.
[Co(NH3)5Cl]NO2 [Co(NH3)5NO2]Cl
Властивості комплексних сполук.
Комплексні сполуки вступають в реакції обміну, сполучення, розкладу, окислення-відновлення та інші.
1. Реакція обміну 3K4[Fe(CN)6] + 4Fe Cl3
Fe4[Fe(CN)6]3 + 12KCl
в іонній формі 3[Fe(CN)6]4– + 4Fe3+ Fe4[Fe(CN)6]3
2. Реакція витіснення лігандів (заміщення)
K2[PtCl6] + 6KJ K2[PtJ6] + 6KCl
3. Реакція розкладу комплексів під впливом температури або розбавлення розчинів
H2[CuCl4] 2H+ + Cu2+ + 4Cl– при розбавленні розчинів
[Pt(NH3)4]Cl2 [Pt(NH3)2Cl2] + 2NH3 при нагріванні
4. Розкладання комплексів під дією кислот
[Ag(NH3)2]Cl + 2HNO3 AgCl + 2NH4NO3
5. Реакція окислення-відновлення
[Pt+2(NH3)2Cl2] + Cl20 [Pt+4(NH3)2Cl4-1]
6. Реакції сукупної кристалізації, при яких утворюються різнолігандні комплекси
K2[PtCl4] + K2[Pt(NO2)4] 2K2[Pt(NO2)2Cl2]
Основні способи одержання комплексних сполук.
1. Реакції сполучення простих і складних речовин
CrCl3 + 6NH3·H2O [Cr(NH3)6]Cl3 + 6H2O
![]()
Fe + 5CO [Fe(CO)5]
2.Витіснення одних лігандів із готової комплексної сполуки іншими лігандами. Причому, тільки ліганди, які утворюють більш міцний зв’язок з йоном-комплексоутворювачем, можуть витісняти ліганди, які утворюють менш міцні зв’язки з тим же комплексоутворювачем.
K2[PtCl4] + 4NH3 [Pt(NH3)4]Cl2 + 2KCl
Кнест.[PtCl4]2–=1·10–16 > Кнест.[Pt(NH3)4]2+=5·10–34
3.Нові комплексні сполуки утворюються в результаті проведення реакцій обміну між комплексними та простими сполуками.
Na3[Co(NO2)6] + 2KCl K2Na[Co(NO2)6] + 2NaCl
та між двома різними комплексними сполуками:
![]()
4.Синтез комплексних сполук відбувається і в реакціях окислення-відновлення:
3Pt + 18HCl + 4HNO3 3H2[PtCl6] + 4NO + 8H2O
5.Нові комплексні сполуки можуть утворюватись в результаті заміщення одного йона-комлексоутворювача іншим:
2Na[Au(CN)2] + Zn Na2[Zn(CN)4] + 2Au
