
- •Періодичні культури
- •Спиртове бродіння
- •Молочнокисле бродіння
- •Види молочнокислих бактерій, які мають важливе значення для промисловості
- •Мікрофлора і процеси, які використовують для виробництва кисломолочних продуктів
- •Пропіоновокисле бродіння
- •Маслянокисле бродіння
- •Мурашинокисле бродіння
- •Алостеричне регулювання
- •Ковалентна модифікація ферментів
- •Інгібування кінцевим продуктом
- •Індукція і репресія
- •Механізм індукції та репресії
- •Будова лактозного оперону
- •Будова триптофанового оперону
- •Позитивний контроль оперону і катаболітна репресія
- •Тема: генетика мікроорганізмів
- •Фотореактивація (світлова репарація)
- •Темнова реактивація (репарація)
- •Види генетичних рекомбінацій
- •Мікрофлора шкіри
- •Мікрофлора діхальних шляхів
- •Мікрофлора порожнини рота
- •Мікрофлора шлунково-кишкового тракту
- •Кількісний вміст мікроорганізмів у різних відділах шлунково-кишкового тракту
- •Мікрофлора сечостатевих органів
- •Мікрофлора очей і вух
- •Роль аутофлори в життєдіяльності організму людини
- •Мікрофлора ґрунту
- •Мікрофлора води
- •Мікрофлора повітря
- •Кругообіг елементів у природі
Лекція №7
Тема: ЖИВЛЕННЯ МІКРООРГАНІЗМІВ
Зміст життя мікроорганізмів – це постійне відтворення своєї біомаси. Сукупність процесів, які протікають в клітині називаються обміном речовин або метаболізмом. Клітинний метаболізм складається з двох напрямів реакцій, які мають різну спрямованість: енергетичного і конструктивного метаболізму.
Енергетичний метаболізм – це реакції, які здійснюють мобілізацію енергії і перетворюють її в електрохімічну (∆µн+) або хімічну (АТФ) форму.
Конструктивний метаболізм (біосинтези) – реакції, в результаті яких будуються речовини клітин (за рахунок речовин, що поступають ззовні). Конструктивні і енергетичні процеси проходять в клітині одночасно і тісно пов’язані один з одним.
Катаболізм – розпад органічних молекул з виділенням енергії хімічних зв’язків.
Анаболізм – синтез органічних молекул з використанням енергії АТФ.
ХІМІЧНИЙ СКЛАД МІКРОБНОЇ КЛІТИНИ
Хімічний склад мікробної клітини принципово подібний до хімічного складу клітин інших живих організмів. Близько 70-90% загальної маси клітини становить вода, решта 30-10% - сухі речовини. Основну масу сухих речовин складають білки (40-80%), полісахариди (17%), ліпіди (10%), РНК (10-20%), ДНК (3-4%). Невеликий відсоток припадає на долю низькомолекулярних органічних речовин і солей.
ПОТРЕБИ МІКРООРГІНІЗМІВ У ПОЖИВНИХ РЕЧОВИНАХ
Мономери, необхідні для синтезу основних клітинних компонентів, можуть бути синтезовані клітиною або поступати в неї у готовому вигляді. В конструктивному метаболізмі основна роль належить Карбону, оскільки всі сполуки, з яких побудовані живі організми – це сполуки вуглецю. При достатньому бажанні можна знайти мікроорганізм, який здатний впливати на будь-яку з відомих вуглецевих сполук.
В залежності від джерела вуглецю всі мікроорганізми поділяються на автотрофи і гетеротрофи.
Автотрофи (від грец. autos – сам, trophe – їжа) – це мікроорганізми, які здатні засвоювати СО2 в якості єдиного джерела вуглецю і синтезувати з нього всі органічні речовини клітини.
Гетеротрофи (від грец. heteros – інший, trophe – їжа) - це мікроорганізми, для яких джерелом вуглецю є готові органічні сполуки.
Якщо автотрофія – поняття досить чітке і вузьке, то гетеротрофія – поняття широке і об’єднує мікроорганізми, які досить сильно різняться за своїми потребами в поживних речовинах.
Серед гетеротрофів розрізняють паразитів, це мікроорганізми, які використовують органічні речовини живих істот (клітин господаря). Облігатні паразити (рикетсії, хламідії) ростуть виключно в клітинах господаря, а факультативні (клостридії, ентеробактерії) як у тілі господаря, так і поза ним.
Наступну групу гетеротрофів складають так звані сапрофіти ( від sapros – гнилий, phyton – рослина) – організми, які використовують готові органічні сполуки, мертвий органічний матеріал, а саме відмерлі рослини, тварини, мікроорганізми, продукти їх життєдіяльності. Сапрофіти складають більшість мікроорганізмів.
Серед сапрофітів виділяють групу оліготрофних мікроорганізмів, які здатні рости при низьких концентраціях органічних речовин у середовищі, зокрема вуглецю та азоту. Наприклад, якщо для звичайних сапрофітів концентрація вуглецю у середовищі становить 10 г/л, то для оліготрофів достатньо 1-15 мг/л. На середовищах з високим вмістом органічних сполук вони гинуть.
Серед гетеротрофів є організми, які засвоюють лише одну органічну сполуку, наприклад, метаноокиснювальні бактерії утилізують метан і/або метанол. Є і такі, які використовують цілий ряд вугецьвмісних органічних сполук. Так, представники роду Pseudomonas здатні метаболізувати до 90 різних органічних речовин.
Нітроген є одним з чотирьох основних компонентів, з яких побудовані живі клітини. Він входить до складу білків, нуклеїнових кислот, порфіринів, багатьох вітамінів.
Більшість мікроорганізмів засвоює Нітроген у відновленій формі, у вигляді солей амонію сечовини, амінокислот. Деякі мікроорганізми засвоюють окиснені форми азоту (нітрати, нітрити), але в клітині вони перед використанням відновлюються. Азотфіксувальні мікроорганізми здатні засвоювати молекулярний азот, який в організмі теж відновлюється до амоніаку.
Сульфур входить до складу амінокислот (цистеїн, цистин, метіонін), вітамінів і кофакторів (біотин, ліпоєва кислота, кофермент А). Найчастіше цей елемент мікроорганізми засвоюють у формі сульфату, але обов’язково відновлюють його до сульфіду. Деякі групи прокаріотів потребують готових відновлених форм сірки.
Фосфор є компонентом нуклеїнових кислот, фосфоліпідів, коферментів. Основне джерело фосфору для мікроорганізмів – його окиснена форма у вигляді фосфатів.
Вивчення потреб мікроорганізмів в елементах живлення показало, що всі вони потребують метали в тих чи інших кількості, як правило, у формі катіонів неорганічних солей. Для росту мікроорганізмів необхідні мікроелементи – Mn, Mo, Zn, Co, Cu, Ni, Va, B, Se тощо. Їх можна отримати з поживного середовища, скляного посуду, ферментерів.
Деякі мікроорганізми виявляють потребу в невеликій кількості якихось певних органічних сполук, які вони самі синтезувати не можуть. Такі речовини отримали назву факторів росту. Це можуть бути амінокислоти, нуклеїнові основи, вітаміни, які лімітують ріст мікроорганізмів і не синтезуються ними в процесі життєдіяльності. Їх вносять у поживне середовище у незначній кількості.
Мікроорганізми, які потребують певного фактора росту, називають ауксотрофами, на відміну від прототрофів, які синтезують всі необхідні для росту сполуки.
ТИПИ ЖИВЛЕННЯ МІКРООРГАНІЗМІВ
У мікроорганізмів виявлено велику різноманітність типів живлення. Для їх характеристики необхідно врахувати три фактори: джерело вуглецю, джерело енергії та донорів електронів.
В залежності від джерела вуглецю всі мікроорганізми поділяються на автотрофи і гетеротрофи.
За типом засвоєння джерел енергії мікроорганізми поділяються на фототрофи (джерело енергії - світло) і хемотрофи (джерело енергії – окисно-відновні реакції).
Організми, у яких джерелом (донором) електронів є неорганічні речовини, називають літотрофами, а якщо органічні сполуки – органотрофами.
Враховуючи все вищесказане, мікроорганізми за типом живлення можна поділити на вісім груп.
|
Джерело енергії |
Донор еле-ктронів |
Джерело вуглецю |
Типи живлення |
Представники |
|
Окисно-відновні реакції |
Неорганічні сполуки |
СО2 |
Хемолітоавторофія |
Сульфатредукувальні, нітрифікувальні, тіонові, ацидофільні, залізобактерії |
|
Органічні сполуки |
Хемолітогетеротрофія |
Сульфатредукувальні, метаноутворювальні, тіонові, водневі бактерії | ||
|
Органічні сполуки |
СО2 |
Хемоорганоавтотрофія |
Факультативні метилотрофи | |
|
Органічні сполуки |
Хемоорганогетеротрофія |
Більшість бактерій, гриби | ||
|
Світло |
Неорганічні сполуки |
СО2 |
Фотолітоавтотрофія |
Ціанобактерії, пурпурні, зелені бактерії |
|
Органічні сполуки |
Фотолітогетеротрофія |
Деякі ціанобактерії, пурпурні, зелені бактерії | ||
|
Органічні сполуки |
СО2 |
Фотоорганоавтотрофія |
Деякі пурпурні бактерії | |
|
Органічні сполуки |
Фотоорганогетеротрофія |
Деякі ціанобактерії, пурпурні, деякі зелені бактерії, галобактерії |
Для всіх цих типів живлення реально існують представники мікроорганізмів.
При зміні складу середовища та умов культивування деякі мікроорганізми можуть переключатись з одного типу живлення на іншій (міксотрофи). Розрізняють також облігатних і факультативних представників.
КУЛЬТИВУВАННЯ І РІСТ МІКРООРГАНІЗМІВ
Для дослідження властивостей мікроорганізмів використовують чисті культури - популяції клітин одного виду, які одержані з однієї клітини. Виділенню чистої культури з природних джерел передує одержання нагромаджувальної культури, в якій переважають мікроорганізми однієї фізіологічної групи. Для цього треба створити елективні (вибіркові) умови – сприятливі для мікроорганізмів, які виділяють і несприятливі для всіх інших. До факторів регулювання елективних умов відносять температуру, рН середовища, наявність кисню, наявність або відсутність органічних речовин тощо.
Відносини між різними групами мікроорганізмів вивчають у змішаних культурах. Природні популяції – це переважно змішані культури, між якими існують різні форми взаємовідносин (конкуренція за субстрат, коменсалізм, мутуалізм та інші).
РІСТ КУЛЬТУР МІКРООРГАНІЗМІВ
Під ростом організму розуміють збільшення біомаси за рахунок засвоєння ним поживних речовин: у багатоклітинних організмів при цьому збільшуються розміри, а в одноклітинних зростає кількість клітин.
Ріст культур мікроорганізмів характеризується різними параметрами: швидкістю росту, величиною урожаю клітин, часом генерації, економічним коефіцієнтом.
Абсолютна швидкість росту – приріст біомаси за одиницю часу.
dx
V= ─── ,
dt
де х – біомаса
t – час.
Питома швидкість росту – приріст біомаси за одиницю часу на одиницю біомаси.
dx 1
μ= ─── ∙───,
dt x
де х – початкова біомаса;
t – час.
Величина питомої швидкості росту є важливою характеристикою як самого мікроорганізму, так і умов культивування.
Урожай культури (вихід біомаси) – це та максимальна кількість клітин або біомаси, яку можна одержати за даних умов в одиниці об’єму. Виражається кількістю клітин або г в 1мл або в 1 л середовища. На величину врожаю впливають умови культивування.
Критерієм росту мікробної популяції є час генерації – час подвоєння біомаси. У E.coli ця величина становить 20-30 хв., у Treponema pallidum – 34 год.
Nt = No∙2n,
де No – початкова біомаса;
Nt - біомаса через час t;
n – число генерацій через час t.
Для оцінки ефективності процесів росту застосовують показник, який одержав назву економічного коефіцієнту. Він визначає відношення кількості утвореної біомаси до кількості використаного субстрату.
МЕТОДИ ВИЗНАЧЕННЯ БІОМАСИ
Визначення сухої ваги клітин;
Визначення вмісту клітинного азоту;
Визначення вмісту клітинного білку;
Визначення кількості ДНК;
Підраховування клітин в одиниці об’єму;
Оптичні методи, наприклад, визначення густини суспензії.
Періодичні культури
Якщо клітини мікроорганізмів культивувати у закритому об’ємі і не поновлювати склад поживних речовин, тобто створити закриту систему, то культивування буде періодичним.
В цих умовах популяція мікроорганізмів проходитиме певний цикл розвитку, для якого притаманна певна зміна фаз. Графічно крива росту періодичної культури зображується наступним чином:
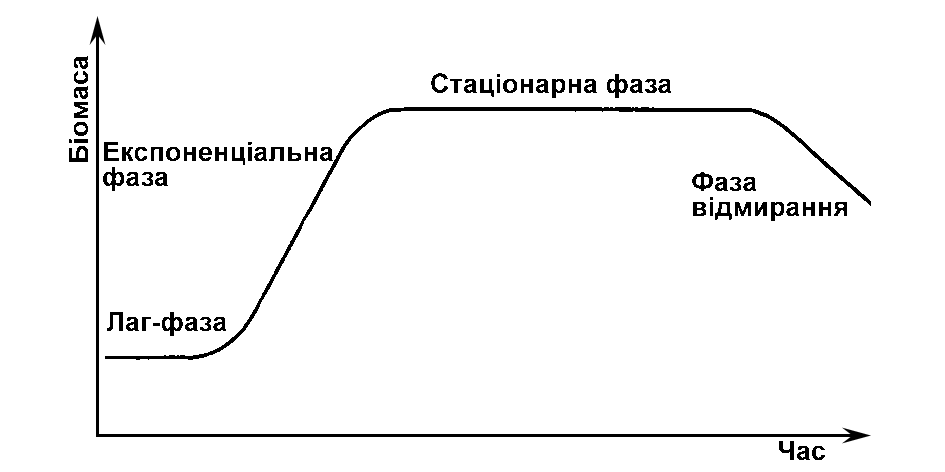
Рис. 1. Крива росту періодичної культури.
Лаг – фаза починається з моменту посіву мікроорганізмів у поживне середовище. В лаг – фазі проходить адаптація культури до умов культивування, якщо потрібно, то клітини синтезують нові ферменти. При цьому чисельність клітин не змінюється. Тільки в кінці лаг – фази спостерігається різке зростання швидкості росту від 0 до максимального. Довга лаг – фаза реєструється, коли культура для пересіву стара, з холодильнику або пересівається з іншого середовища. Якщо умови культивування сприятливі, то цієї фази може і не бути.
Експоненціальна (логарифмічна) фаза розпочинається після адаптації клітин до умов культивування. При цьому встановлюється максимальна швидкість росту. Для клітин цієї фази росту характерна висока біохімічна активність. В лог - фазі є період, коли швидкість приросту біомаси стає постійною. На графіку це зображено у вигляді прямої лінії. Завершується лог – фаза сповільненням росту за рахунок змін умов культивування.
У стаціонарній фазі швидкість росту культури знижується, процеси росту і відмирання врівноважуються. На даний момент максимальний рівень популяції може становити 109 кл/мл. Умови для життя культури стають менш сприятливими. Інтенсивність обмінних процесів знижується, нагромаджуються вторинні метаболіти, токсичні продукти обміну, вичерпуються поживні речовини, що і лімітує ріст культури.
У фазі відмирання крива росту падає вниз із логарифмічною залежністю, оскільки число живих клітин в культурі значно зменшується. Починається лізис клітин під дією власних ферментів (автоліз). Умови для існування культури стають несприятливими, і тому спостерігається збільшення клітин у стані спокою (цисти, спори). Деякі методи руйнування клітин на виробництві з метою отримання внутрішньоклітинних компонентів базуються саме на штучному введенні культури у фазу відмирання, наприклад, додавання до середовища толуолу.
Якщо впливати на умови культивування таким чином, щоб виводити продукти обміну і додавати свіже поживне середовище, то можна тривалий час підтримувати культуру в експоненціальній фазі росту.
Саме такий спосіб культивування мікроорганізмів знайшов своє застосування у виробничих і напіввиробничих умовах, і він називається безперервним культивуванням. Контроль і управління процесами безперервного культивування здійснюють двома способами: хемостатним і турбідостатним.
Хемостат складається з ємності – культиватора, в який з резервуару поступає з постійною швидкістю поживне середовище. Завдяки аерації і механічному перемішуванні в культиваторі створюються оптимальні умови для постачання клітин киснем і для більш швидкого та рівномірного розподілу поживного середовища. По мірі поступлення в культиватор поживного середовища з нього витікає бактеріальна суспензія.
Бактерії в хемостаті знаходяться, як правило, в експоненціальній фазі. Коли швидкість росту і розведення рівні, то втрата в результаті вимивання клітин і приріст біомаси відносяться як 1:1.
Ріст культури в хемостаті контролюється концентрацією субстратів.
Стабільність динамічної рівноваги культури в хемостаті обумовлена там, що її ріст лімітує концентрація якого-небудь субстрату.
Вирощування культури в турбідостаті суттєво відрізняється від вирощування в хемостаті. Робота турбідостату базується на підтримуванні постійної щільності бактеріальної суспензії або постійної мутності (екстинції).
Датчик мутності регулює через керуючу систему поступлення живильного розчину. В ємності для культивування всі поживні речовини знаходяться у надлишку, і швидкість росту бактерій наближується до максимальної. Робота з турбідостатами технічно складніша, ніж з хемостатами.
BOX
|
Деякі автори [1] вважають, що процес росту періодичної культури доцільно поділити на більшу кількість стадій. I II III IV V VI VII VIII
I – лаг-фаза; II – фаза позитивного прискорення; III – фаза логарифмічного росту; IV – фаза негативного прискорення; V – стаціонарна фаза; VI – фаза прискореної загибелі; VII – фаза логарифмічної загибелі; VIII – фаза зменшення швидкості загибелі. |
ВИКОРИСТАНА ЛІТЕРАТУРА:
С.В.Бирюкова. Основные принципы классификации микроорганизмов// Клиническая микробиология. - №1 (3), февраль, 2000. – С.12-15.
Лекція № 8
Тема: ВПЛИВ ФАКТОРІВ ЗОВНІШНЬОГО СЕРЕДОВИЩА НА МІКРООРГАНІЗМИ
Мікроорганізми, з одного боку, більше залежать від умов оточуючого середовища, ніж тварини і рослини, а з іншого боку їм властива здатність існувати в значно ширшому діапазоні змін умов зовнішнього середовища, ніж вищим еукаріотам.
ВПЛИВ ТЕМПЕРАТУРИ
Температура оточуючого середовища так само впливає на мікроорганізми, як і на інші живі організми. Оскільки всі мікроорганізми, як правило, одноклітинні і всі без виключення пойкілотермні – їх температура варіює в залежності від температури оточуючого середовища.
Найважливіший ефект, який має температура на мікроорганізми – це вплив на швидкість протікання хімічних реакцій. При зниженні температури швидкість ензиматичних реакцій знижується і, відповідно, сповільнюється швидкість росту мікроорганізмів. З підняттям температури на кожні 100С швидкість реакцій подвоюється. Однак, значне підняття температури призводить до летального ефекту. При високій температурі денатуруються ферменти, транспортні переносники, інші білки; ліпідний бішар у мембранах плавиться.
Ріст мікроорганізмів лежить у певних температурних межах і визначається кардинальними точками – мінімальною, оптимальною та максимальною температурами росту. Хоча форма кривої температурної залежності варіює, температурний оптимум завжди ближче до максимуму, ніж до мінімуму.
Кардинальні температури для певних штамів не обов’язково строго фіксовані, вони залежать від інших факторів оточуючого середовища.
Деякі види, наприклад, Neisseria gonorrhoeae мають невеликий температурний діапазон і називаються стенотермалами, інші, як Enterococcus faecalis, можуть рости в широкому діапазоні температур і називаються еврітермалами.
Основні групи мікроорганізмів відрізняються одна від одної максимальними температурами росту. Так, верхня межа для Protozoa становить приблизно 500С. Деякі водорості та гриби ростуть при температурі до 55-600С. Виявлено, що бактерії можуть рости при температурі, близькій до 1000С (в точці кипіння води), а окремі штами і при вищій температурі.
BOX
|
Екстремальні термофіли Було виділено мікроорганізми з «чорних курильщиків» (“black smokers”), які розташовані на дні океану серед рифів і скал. Вода в у цих ділянках океану має високий вміст сірководню і температуру до 3500С. Бактерії, що виділені звідти, росли при 1150С, але можуть рости і при вищій температурі. Тиск у цих середовищах існування достатній, щоб тримати воду в рідкому стані, і він становить 265 атм. Для того, щоб морська вода закипіла при цьому тиску, треба підняти температуру до 4600С. |
На основі температурного діапазону росту мікроорганізми поділяють на такі групи:
Психрофіли. Вони добре ростуть при 00С, мають оптимальну температуру росту при 150 і нижче, максимальну + 200С.
Розповсюджені в Арктиці, Антарктиці. Оскільки 90% води світового океану має температуру 50С, то очевидно там існують психрофільні мікроорганізми. Водорості Chlamydomonas nivalis призводять до утворення рожевих плям на снігових полях та льодовиках за рахунок своїх яскраво червоних спор. Більшість психрофілів – представники родів Pseudomonas, Flavobacterium, Achromobacter, Alcaligenes.
Психрофіли адаптувались до умов існування наступним чином:
Їм притаманний високий вміст у клітинних мембранах коротколанцюгових ненасичених жирних кислот, що дозволяє бути мембрані напіврідкою при холоді;
Низька температура активації ферментів;
Транспорт речовин у психрофілів здійснюється при низьких температурах. У мезофілів за таких умов він інактивується.
Особливості біосинтетичного апарату полягають у тому, що при температурі росту психрофілів у інших мікроорганізмів втрачається здатність утворювати полісоми.
Психротрофи або факультативні психрофіти. Багато видів можуть рости при 00С, навіть якщо вони мають оптимум між 200 і 300 та максимум при 350С. Психротрофні бактерії і гриби спричиняють псування заморожених продуктів.
Мезофіли – це мікроорганізми з ростовим температурним оптимумом від 200до 450С і мінімумом – від 15 до 200С. Їх температурний максимум становить 450С і нижче. До цієї групи належить більшість мікроорганізмів. Всі патогени людини – мезофіли, оскільки температура їх оточуючого середовища майже постійно 370С.
Термофіли. До цієї групи належать мікроорганізми, яки можуть рости при температурі 550С і вище. Ростовий мінімум становить 450, оптимум – 55-650С. Як згадано вище, деякі термофіли можуть рости при температурі віще 1000С. Термофіли в основному представлені бактеріями, хоча серед них є декілька видів дріжджів і грибів. Вони зустрічаються в таких екосистемах як компост, скирди сіна, що самонагріваються, гарячі джерела.
Термофілія пояснюється наступним чином:
У ліпідах клітинних мембран наявний високий вміст насичених жирних кислот з довгими розгалуженими ланцюгами;
Ферменти термофілів мають низьку молекулярну масу, а також стабільність при високих температурах;
Білки цих мікроорганізмів відрізняються за первинною структурою, вони містять більше амінокислот з вільними NH2-групами;
Спостерігається менший вміст вільної та зв’язаної води, підвищена кількість іонів Са2+ та К+;
ДНК стабілізується поліамінами, зокрема терміном, кальдотерміном;
Наявність ізоферментів.
В цілому, низькі температури мікроорганізми переносять краще, ніж високі.
ВПЛИВ рН СЕРЕДОВИЩА
Кислотність середовища є важливим фактором, який визначає можливість існування мікроорганізмів. Концентрація іонів Н+ впливає на поверхневі структури, активність ферментів, стабільність макромолекул. Із зміною рН змінюється ступінь засвоєння речовин із середовища:
При низьких значеннях рН зростає розчинність іонів Купруму, Мангану, Алюмінію, відповідно, підвищується їх токсичність;
При високих значеннях рН зменшується розчинність іонів Fe, Ca, Mg, Mn. Внаслідок цього вони стають недоступними для мікроорганізмів.
Життя мікроорганізмів можливе в широких межах рН – від 0 (0,6) до 11 (11,5). Проте кожний вид існує в певних значеннях рН середовища, тому, як правило, розрізняють нижню межу, оптимальне значення рН, а також верхню межу кислотності середовища.
Ацидофіли (рН 1 – 5,5) - мікроорганізми, для яких оптимальні значення рН середовища лежать у кислій зоні. Це переважно гриби (оптимум рН 4 - 6), водорості, тіонові бактерії. Водорості Cyanidium caldarium і бактерії Sulfolobus acidocaldarius добре ростуть при рН 1 – 3 і високій температурі; дріжджі Saccharomyces telluris – при рН 0,9 – 1,1.
Бактерії, які ростуть в діапазоні рН 5,5 – 8 називають нейтрофілами. До них належить більшість бактерій і найпростіших, зокрема E.coli, B.subtilis, Streprococcus faecalis тощо.
У природі зустрічаються зони з високим значенням рН (рН 8,5 – 11,5), де розвиваються алкалофіли. До них належать амоніфікатори, сульфат- і нітратредукувальні бактерії, уробактерії, ціанобактерії, B.alcalophilus тощо.
Зазвичай здатність до росту при низьких або високих значеннях рН надає певну перевагу мікроорганізмам, оскільки таким чином обмежується конкуренція з боку інших організмів.
Не дивлячись на те, що мікроорганізми здатні рости в широкому діапазоні рН, кислотність середовища в клітині залишається на нейтральному рівні (рН ≈7). Якщо внутрішньоклітинний рН знижується до 5,0 – 5,5, то наступає смерть клітини.
Існують певні механізми для підтримування внутрішнього рН:
Цитоплазматична мембрана непроникна для протонів Н+;
Змінюється вміст іонів К+, Na+ в клітині;
Спрацьовує внутрішня буферна система;
Коли рН в клітині знижується до 4,5 або нижче, то вона починає синтезувати чаперони (chaperons) – білки кислотного шоку або білки температурного шоку.
Протягом багатьох років вважалось, що після синтезу на рибосомах поліпептиди спонтанно утворюють свою кінцеву конфігурацію – вторинну, третинну і четвертинну структуру. І, хоча ці структури визначаються послідовністю амінокислот в ланцюгу, тепер відомо, що абсолютно в усіх клітинах (прокаріотних та еукаріотних) існують допоміжні білки – молекулярні чаперони – які допомагають скручуванню поліпептидів. Вони запобігають неправильному скручуванню, тобто формуванню неправильних білкових молекул і утворенню нефункціональних білкових агрегатів.
Чаперони вперше були виявлені тому, що їх кількість значно зростала у випадку, коли клітини поміщали в стресові умови: висока температура, токсичні речовини. Тому багато чаперонів отримали назву білків температурного шоку (heat – shock proteins) або стресових білків (stress proteins). Якщо культуру E.coli переносили з 300С в 420С, то концентрація стресових білків суттєво зростала протягом всього п’яти хвилин. При летальній температурі синтез всіх білків припинявся, окрім синтезу білків температурного шоку.
Вважається, що чаперони виконують наступні функції:
Захищають РНК-полімеразу від температурної інактивації in vitro;
Можуть відновити термічно інактивовану РНК-полімеразу;
Відіграють важливу роль у транспорті білків через мембрану. Наприклад, чаперон Sec B E.coli зв’язується з частково розкрученим білком і підтримує його в такому вигляді протягом всього процесу переносу через ЦПМ (export competent state).
В процесі росту деякі мікроорганізми самі здатні змінювати рН середовища за рахунок утворення кислих або лужних продуктів метаболізму: оцтової, масляної, пропіонової кислот; амоніаку тощо.
Чутливість мікроорганізмів до рН середовища використовується при консервуванні харчових продуктів. Застосування маринадів, квашення овочів призводить до створення низького рН, несприятливого до розвитку гнильних мікроорганізмів.
ВПЛИВ КИСНЮ
По відношенню і за потребою в молекулярному кисні мікроорганізми поділяються на такі групи:
Аероби Анаероби
/ \ / \
Облагатні Факультативні Облігатні
/ \ / \
Які ростуть Мікроаерофіли Аеротолерантні Строгі
у повітрі
Облігатні аероби потребують О2 для росту. Це досить численна група мікроорганізмів. Оптимальна концентрація О2 для їх росту приблизно дорівнює атмосферній (21%). Коли концентрація О2 доходить до 50%, то спостерігається пригнічення росту всіх мікроорганізмів.
Деякі аероби розвиваються при значно нижчих концентраціях О2: 2 – 10%. Такі мікроорганізми одержали назву мікроаерофілів. До них належать молочнокислі бактерії, Campylobacter sp. та інші.
Облігатні анаероби у присутності О2 гинуть (метаногенні бактерії, Clostridium, Treponema, Bacteroides). В природі живуть, як правило, в асоціаціях з аеробами або факультативними анаеробами, які здатні зменшувати концентрацію кисню. Наприклад, облігатний анаероб Bacteroides gingivalis живе в ротовій порожнині в щілинах між зубами у мишей.
Серед аеробів та анаеробів є мікроорганізми, які добре ростуть як без О2, так і при його наявності. Їх називають факультативними анаеробами. Наприклад, представники родини Enterobacteriaceae, які здатні здійснювати як дихання, так і бродіння.
Аеротолерантні мікроорганізми ростуть однаково добре як з киснем, так і без нього. При контакті з О2 вони не гинуть (наприклад, Enterococcus faecalis).
Різне відношення мікроорганізмів до О2 залежить від декількох факторів, включаючи інактивацію білків та вплив токсичних кисневих похідних. Ферменти інактивуються, коли чутливі групи, зокрема сульфгідрильні, окиснюються. Наприклад, фермент нітрогеназа дуже чутливий до наявності кисню в середовищі, тому в різних мікроорганізмів у процесі еволюції виробилися різні пристосування до захисту від кисню.
Кисень приймає електрони і швидко відновлюється, оскільки його 2 зовнішні орбіталі незаповнені. В процесі відновлення кисню в клітині утворюються наступні речовини:
Супероксидний радикал
О2 + е → О2-
Пероксид водню
О2- + е + 2Н+ → Н2О2
Гідроксил радикал
Н2О2 + е + Н+ → Н2О + ОН.
Ці продукти відновлення кисню є надзвичайно токсичними, оскільки вони дуже швидко руйнують клітинні компоненти. Мікроорганізми повинні вміти захистити себе від шкідливих продуктів відновлення кисню, або будуть вбиті. Нейтрофіли і макрофаги використовують токсичні продукти відновлення О2 для руйнування проникних патогенів. На цьому ж базується застосування перекису водню у медицині.
Мікроорганізми, як правило, містять ферменти, що дозволяють захистити від токсичних продуктів. Облігатні аероби і факультативні анаероби містять ферменти супероксидисмутазу і каталазу.
супероксидисмутаза
2 О2- + 2Н+ ─────────────→ О2 + Н2О2
каталаза
2 Н2О2 ───────→ 2 Н2О + О2
У аеротолерантних мікроорганізмів немає каталази, але майже завжди є супероксидисмутаза. Аеротолерантний мікроорганізм Lactobacillus plantarium для руйнування супероксидних радикалів використовує замість супероксидисмутази іони Мg2+.
У всіх строгих анаеробів ці ферменти відсутні.
Відношення мікроорганізмів до кисню обов’язково враховується при їх культивуванні. При великих об’ємах рідини, зокрема на виробництві, культури додатково аерують на качалках або у спеціальних апаратах з мішалками (ферментерах). У промисловості культивування аеробних мікроорганізмів здійснюють найчастіше глибинним способом з продуванням стерильного повітря.
ВПЛИВ ГІДРОСТАТИЧНОГО ТА ОСМОТИЧНОГО ТИСКУ
До високого гідростатичного тиску мікроорганізми проявляють значну стійкість, зокрема морські бактерії переносять тиск в 200-300 атм, дріжджі зберігають життєздатність при 500 атм.
Культури, які ростуть як при звичайному атмосферному, так і при підвищеному тиску належать до баротолерантних. Відомі і культури, які краще розмножуються при вищому тиску, ніж атмосферний, і вони називаються барофільними.
Більш важливе значення для життєдіяльності мікроорганізмів має осмотичний тиск, який визначається концентрацією розчинених у середовищі сполук. Осмотичну рівновагу регулює ЦПМ клітини. При високому осмотичному тиску клітина втрачає здатність поглинати воду з оточуючого середовища і зневоднюється (явище плазмолізу). При низькому осмотичному тиску вода посилено поступає в клітину і викликає плазмоптиз.
Проте деякі мікроорганізми ростуть у концентрованих розчинах солей або органічних речовин, тобто у середовищах з високим осмотичним тиском, наприклад, дріжджі в меді, в якому вміст цукрів становить 80%.
Мікроорганізми, які здатні витримувати високий осмотичний тиск, але краще розвиваються при нормальному тиску, називаються осмотолерантними. Мікроорганізми, для яких високий осмотичний тиск є необхідним для росту, називаються осмофільними.
Різні групи мікроорганізмів відрізняються за своїм відношенням до іонів натрію. Більшість мікроорганізмів росте в інтервалі концентрацій іонів натрію 0 – 4%. Але є осмофільні мікроорганізми, для розвитку яких необхідні високі концентрації солі, і вони отримали назву галофільних. По відношенню до NaCl в середовищі розрізняють наступні групи (табл.1):
Таблиця 1
|
Назва |
Концентрація солі, % |
Представники |
|
Морські бактерії |
2,5 – 5 |
|
|
Помірні галофіли |
5 – 15 |
|
|
Екстремальні галофіли |
12 – 15 і до насичення |
Halobacterium,Halococcus |
BOX
|
Багато бактерій підтримують осмотичну концентрацію цитоплазми більше, ніж в оточуючому середовищі шляхом синтезу сумісних речовин (осмопротекторів): холіну, бетаїну, проліну, глютамінової кислоти; в клітинах бактерій спостерігається підвищений вміст К+, у дріжджів і водоростей синтезується надмірна кількість гліцеролу. Галофіли накопичують у цитоплазмі високі концентрації іонів калію (4-7 М). Ферменти, рибосоми, транспортні системи у таких мікроорганізмів для стабільності, активності та нормального функціонування потребують високий рівень К+. Плазматична мембрана Halobacterium стабілізується іонами кальцію. |
ВПЛИВ ВОЛОГОСТІ СЕРЕДОВИЩА
Вода – один з найважливіших компонентів мікробної клітини і становить приблизно 80% складу вегетативної клітини. Вода є одночасно і середовищем, і реагентом для багатьох реакцій обміну. Відомо, що вода виконує фізіологічні функції лише в рідкій фазі, тому існує певна біокинетична зона, яка обмежена температурою від -20 до 1000С. Найменша кількість води, при якій ще можливий розвиток прокаріотів, становить 20-30% загальної маси організму.
Активна життєдіяльність мікроорганізмів здійснюється лише в умовах достатньої вологості. Існує певний показник – Аw - водна активність, або ступінь доступності води з розчинів.
N2
Аw = ───── ; де
N1-N2
N1 – число молей розчинника;
N2 – число молей розчиненої речовини.
В табл.2 представлені показники водної активності в різних середовищах.
Таблиця 2
|
Аw |
Середовище, можливий вплив на мікроорганізми |
|
1,0 |
Чиста вода |
|
0,95 |
Хліб |
|
0,85 |
Салямі |
|
0,75 |
Солена риба, солоні озера |
|
0,60 |
Шоколад, мед |
|
0,55 |
За таких умов руйнується ДНК |
При дефіциті вологи мікробна активність знижується, а при висушуванні повністю пригнічується. На цьому явищі базується зберігання продуктів у висушеному стані: в’ялене м’ясо, риба, сухі овочі та фрукти.
Найбільша стійкість до висихання притаманна спочиваючим формам мікроорганізмів: спорам і цистам, конідіям грибів, артроспорам.
Для зберігання колекційних штамів мікроорганізмів, для одержання імунних сироваток, ферментних препаратів використовується спеціальне висушування попередньо замороженої суспензії бактерій у вакуумі – ліофілізація.
ВПЛИВ ВИПРОМІНЮВАННЯ
Всі живі організми знаходяться під впливом різних видів випромінювання. Ефекти, які викликає опромінення залежить від довжини хвилі та дози.
Радіохвилі (понад 400 000 нм, або 4∙102 мкм) не викликають біологічного ефекту.
Інфрачервоні промені (800 – 400 000 нм) при поглинання організмом перетворюються у тепло.
Видиме світло (380 – 740 нм) на більшість мікроорганізмів діє згубно. Проте, видиме світло необхідне для життєдіяльності фотосинтезувальних бактерій як джерело енергії і стимулює ріст деяких мікроорганізмів, зокрема грибів.
Стійкість до світла підвищується за рахунок пігментації. Серед мікрофлори повітря зустрічаються, як правило, забарвлені, в основному за рахунок наявності каротиноїдів, форми мікроорганізмів.
Ультрафіолетові промені (200 – 400 нм) є найактивнішою частиною сонячного світла. Ультрафіолетове опромінення має сильний бактерицидний ефект, тому ультрафіолетові промені широко використовуються як стерилізуючий фактор для стерилізації приміщень, інструментів, вакцин і сироваток, при переливанні крові тощо. Як дальній ультрафіолет (220-300 нм), так і ближній (300-380 нм) мають пошкоджуючи дію на біополімери клітини в результаті фотолізу, утворення пиримідинових димерів, гідроксилювання нуклеотидів, індукції заміни пар основ однониткових та двониткових розривів ДНК, зшивки ДНК з білками.
Особливо небезпечна дія УФ-променів з довжиною хвилі 254-265 нм, вони найкраще поглинаються білками та нуклеїновими кислотами, зокрема ДНК та викликають димеризацію тиміну, що перешкоджає розходженню ниток ДНК при реплікації.
При довжині хвилі УФ-променів 325-400 нм у молекулах білків мікроорганізмів амінокислота триптофан руйнується з утворенням токсичних для клітини фотопродуктів.
УФ-промені викликають також різноманітні мутації у мікроорганізмів, що використовуються для одержання в лабораторних умовах мутантів із різними властивостями. Однак, пошкодження, викликані УФ-променями, клітина здатна відновлювати за допомогою спеціальних механізмів репарації (фото- та темнової реактивації).
Іонізуючі промені (менше 10 нм). Іонізуюче випромінювання є компонентом природної радіації, яка складається переважно з корпускулярного ά-, β-опромінення, а також рентгенівського та γ-випромінювання. Радіаційний вплив забезпечують космічні промені, нестабільні ізотопи ґрунту, опадів, розробка копалин радіоактивних мінералів, штучні джерела радіації (випробування ядерної зброї, атомні електростанції, застосування радіоізотопів із медичною та науковою метою).
Дія іонізуючого випромінювання на клітини мікроорганізмів виявляється в численних пошкодженнях, подібних до дії ультрафіолету, переважно однониткових та двониткових розривах ДНК. Опосередкований вплив опромінення пов’язаний з утворенням вільних радикалів, що сприяють перекисному окисненню ліпідів.
Мікроорганізми є найбільш стійкими до радіаційного впливу порівняно з іншими організмами. Летальною дозою для ссавців є рівень, наближений до 103 рад, для комах – 105 рад, для мікроорганізмів – 106 рад. Серед мікроорганізмів резистентність серед коків вища за таку в паличкоподібних формах, проте серед високорезистентних бактерій відомі як коки (Deinococcus radiodurans, D.radiophilus), так і палички (Deinobacter grandis). Стійкість до опромінення притаманна також різним грибам родів Alternaria, Aureobasidium, Stemphylium, Stachybotrys, Cladosporium.
Місцями існування радіорезистентних мікроорганізмів є родонові джерела, охолоджувальні системи атомних електростанцій, об’єкт укриття атомного реактора.
Головним джерелом природного опромінення є сонячна радіація. Основна частина сонячної енергії припадає на долю видимих променів (близько 75%), майже 20% - на інфрачервону частину спектра і лише 5% - на ультрафіолет.
Ультразвук. Звукові хвилі з частотою коливання понад 16 000 Гц належать до ультразвуку. Ультразвукові хвилі чинять мікробоцидну дію на бактерії, гриби та віруси. Їх дію пов’язують з явищем кавітації – утворенням порожнин у рідині. У разі закривання таких порожнин виникають гідравлічні удари, що руйнують клітини. Ультразвук викликає у мікроорганізмів розрив клітинної стінки, розпад клітини на дві половини, відокремлення джгутиків тощо.
До ультразвуку чутливі всі мікроорганізми, включаючи спорові. Тому ультразвук використовують у мікробіологічній практиці для дезінтеграції мікроорганізмів з метою виділення окремих клітинних структур (мітохондрій, рибосом, ядер), для вивільнення біологічно активних сполук (вітамінів, ферментів), для стерилізації термолабільних субстратів.
ДІЯ ГРАВІТАЦІЇ
Усі організми зазнають впливу земного тяжіння. Проте доказів прямої дії гравітації на бактерії не існує. Розміри бактеріальних клітин настільки малі, що у водних розчинах вони практично перебувають у стані невагомості, хоча завислі мікроорганізми все ж поступово осідають. Деякі аеробні бактерії у стані невагомості ростуть краще. Це пояснюється більш рівномірним розподілом поживних речовин.
Ще одним прикладом впливу гравітації на мікроорганізми може бути геотропізм, який проявляється у формування актиноміцетами і мікроскопічними грибами різнонаправленого повітряного та субстратного міцелію.
ДІЯ МАГНІТНОГО ПОЛЯ
Магнітне поле помірно впливає на більшість мікроорганізмів неспеціалізованих форм. Доведена стимуляція росту для Pseudomonas aeruginosa, Staphylococcus epidermidis, Halobacterium salinarium магнітним полем із напруженістю 12∙103 А/м та їх пригнічення магнітним полем з напруженістю 24∙103 А/м і вище. Проте в природних середовищах магнітні поля такої напруженості не зустрічаються.
Значний вплив магнітного поля зареєстрований на спеціалізовані форми мікроорганізмів – магнітобактерії. Вони здатні регулювати напрямок свого руху відповідно до напрямку силових ліній магнітного поля. Це явище було названо магнетотаксисом. У слабких магнітних полях (8-40 А/м) магнітобактерії рухаються зі швидкістю до 70 мкм/с уздовж ліній поля.
Магнітобактерії поширені в морських маршах, заболочених прісноводних водоймах, у збірниках для очистки стічних вод, тобто в місцях з малорухомою водою. Чисельність їх у таких умовах досягає 106 - 107 кл/мл.
Найкраще з магнітобактерій вивчений Aqaspirillum magnetotacticum – мікроаерофільний хемогетеротроф. Його особливістю є наявність магнітосом – кубічних або октаедричних кристалів окису заліза – магнетиту, за рахунок якого вміст заліза в клітинах таких спірил досягає 3,8%, що набагато перевищує його вміст у клітинах неспеціалізованих форм (0,025%). Магнітосоми можуть накопичуватися в осадах водойм у вільному стані, утворюючи біогенні магнетити з високим рівнем природного залишкового магнетизму.
ВПЛИВ ХІМІЧНИХ СПОЛУК
Серед великої кількості хімічних сполук є такі, які необхідні мікроорганізмам для росту, а є і такі, які на них впливають негативно. Вони або гальмують ріст (мікробостатичний, бактеріостатичний, фунгістатичний ефекти), або викликають загибель мікроорганізмів (мікробоцидний, бактеріоцидний, фунгіцидний ефекти). Дія хімічної сполуки залежить від її будови, концентрації, чутливості мікроорганізму та інших факторів.
За хімічною будовою та механізмом впливу на мікроорганізми антимікробні речовини дуже різноманітні:
Солі важких металів (Cu, Ag, Pb, Hg) викликають коагуляцію білків, інактивацію ферментів, інгібування синтезу білка, РНК. Найбільш чутливі до дії важких металів – ціанобактерії, найстійкіші – тіонові бактерії. Найтоксичнішими для мікроорганізмів вважаються іони Hg2+, Ag+.
Галогени та їх похідні (F, I, Cl) є сильними окиснювачами, вони порушують дію ферментів окисно-відновних процесів.
О3, Н2О2, КМпО4, перкислоти є також сильними окиснювачами. Вони взаємодіють з компонентами мембран, посилюють окиснювальні процеси в клітині.
Органічні сполуки. Серед органічних сполук сильними антимікробними агентами є етиловий спирт (50-96%), фенол або його водний розчин (карболова кислота), формальдегід, органічні кислоти (молочна, мурашина, оцтова, хлороцтова), різні барвники (кристалвіолет, метиленовий синій, діамантовий зелений, фуксин тощо).
Використання антимікробних сполук є основою дезінфекції (способу знезараження, за допомогою якого знищують мікроби). Найбільше практичне застосування як дезінфікуючі засоби мають сполуки хлору (хлорамін, хлорна вода, хлорне вапно), 2%-вий розчин йоду, 1-5%-вий розчин карболової кислоти, перманганат калію, поверхнево-активні речовини. Їх використовують для дезінфекції приміщень, питної води, стічних вод, у ветеринарії, хірургії тощо.
Особливу групу антимікробних органічних сполук становлять антибіотики. Це вторинні метаболіти, їхній синтез не пов’язаний з основними процесами розвитку мікроорганізмів. Продуцентами антибіотиків є бактерії, актиноміцети, гриби. Рослини в якості антибіотиків продукують фітонциди, тварини – лізоцим.
Антибіотики діють на чутливі до них мікроорганізми і вибірково порушують протікання певних життєвих процесів. Наприклад:
Пеніцилін пригнічує синтез клітинної стінки, імовірно, порушуючи нормальне формування пептидогліканового шару. Особливо активний проти грампозитивних бактерій.
Поліміксин порушує функції ЦПМ.
Ріфампіцин інгибує синтез нуклеїнових кислот.
Стрептоміцин, хлорамфенікол блокують функції рибосом 70-S типу і тим самим пригнічують синтез білка в бактеріальній клітині.
Антибіотики широко використовуються під час лікування інфекційних захворювань людини, тварин і рослин, для поліпшення росту і розвитку молодняка у тваринництві, як консервуючи засоби у харчовій промисловості.
З метою зниження появи стійких до антибіотиків форм мікроорганізмів не дозволено використовувати у сільському господарстві та промисловості антибіотики, що мають застосування в медицині.
Лекція №9
Тема: ШЛЯХИ ОДЕРЖАННЯ ЕНЕРГІЇ МІКРООРГАНІЗАМИ
Для здійснення роботи живі організми можуть використовувати не всі види енергії. Доступними для живих систем зовнішнім джерелом енергії є електромагнітна (світло певної довжини хвилі) та хімічна (відновлені хімічні сполуки). Енергію світла використовують фотосинтезувальні мікроорганізми, всі решта як джерела енергії використовують процеси окиснення хімічних сполук – органічних або неорганічних.
У прокаріот відомо чотири способи отримання енергії: бродіння, дихання, фотосинтез і хемосинтез.
Бродіння – це метаболічний процес, що призводить до утворення АТФ, при якому органічні сполуки служать як донорами електронів (процес окиснення), так і їхніми акцепторами (процес відновлення). Ці сполуки належать до різних метаболітів, що утворюються з одного субстрату, який підлягає бродінню. При цьому зберігається сувора рівновага процесів окиснення і відновлення.
Вимоги точної окисно-відновної рівноваги лімітує коло субстратів бродіння. Вони мають відповідати певному рівню окисненості, тобто повинні бути ні сильно відновлені, ні сильно окиснені. Тому основними субстратами бродіння є здебільшого вуглеводи.
У процесі бродіння утворюються нестабільні молекули, фосфатна група яких містить багато вільної енергії. Ця група ферментативно переноситься на молекулу АДФ, внаслідок чого утворюється АТФ. Реакції, в яких енергія, що звільнюється на певних етапах бродіння, запасається у вигляді АТФ, називаються субстратним фосфорилюванням. Іншими словами, субстратне фосфорилювання – це перенос на АДФ багатої енергією фосфатної групи від проміжної сполуки катаболізму. Такими проміжними сполуками є 1,3-дифосфогліцеринова кислота, фосфоенолпіруват і ацетилфосфат.
Багато мікроорганізмів отримають енергію в процесі дихання.
Дихання - це метаболічний процес, що призводить до утворення АТФ, при якому донорами електронів служать органічні сполуки, а акцепторами – неорганічні. Здебільшого кінцевим акцептором електронів є молекулярний кисень, тоді розрізняють аеробне дихання. Для невеликої кількості бактерій кінцевим акцептором електронів є інші неорганічні сполуки – сульфати, нітрати або карбонати. Такий процес називають анаеробним диханням.
Коло органічних сполук, що можуть підлягати розщепленню під час дихання, широке. Необхідна тільки та умова, щоб ступінь їхнього окиснення був нижчим, ніж ступінь окиснення СО2. Тому мікроорганізми можуть використовувати як джерело окиснення в процесі дихання будь-які органічні сполуки.
Окиснення відбувається в результаті перенесення електронів через ланцюг перенесення електронів (ЛПЕ) або дихальний ланцюг. Він складається зі сполук, які можуть поперемінно то відновлюватись, то окиснюватись. Компоненти дихального ланцюга у прокаріот локалізовані в ЦПМ, у еукаріот – у внутрішній мембрані мітохондрій. Електрони від окиснюваного субстрату переходять через ЛПЕ і потрапляють до кінцевого акцептора. Якщо ним виступає О2, то він з’єднується з Н2, який походить від субстрату, з утворенням Н2О або Н2О2.
У ЛПЕ протікають реакції, що являють собою біохімічний аналог згоряння водню. Відміна полягає лише в тому, що значна частина вільної енергії переводиться в біологічно доступну форму – АТФ і лише незначна частина розсіюється у вигляді тепла.
Найбільш розповсюджена серед прокаріотів здатність окиснювати органічні субстрати. Є прокаріоти, які здатні окиснювати різні неорганічні субстрати (Н2, NH4+, NO2-) з відповідним відновленням кисню. І, нарешті, прокаріоти можуть окиснювати органічні та неорганічні речовини з використанням в якості кінцевого акцептора електронів цілого ряду органічних та неорганічних сполук (фумарат, СО2, NO3-, сульфати), а не О2.
Транспортування протонів і електронів здійснюється таким чином, що між внутрішньою та зовнішньою сторонами мембрани створюється електрохімічний градієнт з додатнім потенціалом ззовні та від’ємним - усередині. Нерівномірний розподіл зарядів призводить до утворення електрохімічної енергії (∆μн+), яка потім може бути використана для синтезу АТФ.
Оскільки у випадку з дихальним ланцюгом синтез АТФ пов’язаний з мембранами, то реакції, що призводять до його утворення, отримали назву мембранного (окисного) фосфорилювання. Таким чином, мембранне фосфорилювання – це синтез АТФ за рахунок енергії транспортування електронів. Під час цього процесу субстрати окиснюються повністю до вуглекислого газу (за винятком процесів, характерних для неповного окиснення).
Отже, в клітині (і у бактерій, і у багатоклітинних організмів) існує дві універсальні форми енергії: хімічна (енергія високоенергетичних хімічних сполук) та електрохімічна (енергія трансмембранного потенціалу іонів водню).
Фотосинтез. Фототрофні бактерії як джерело енергії використовують світло. В клітинах цих організмів відбувається перетворення світлової енергії в біохімічно доступну енергію АТФ.
Хемосинтез – це отримання енергії внаслідок окиснення неорганічних сполук (аміак, нітрити, сірководень, сірка, водень, Fe2+ ). Ці сполуки використовуються як донори електронів. Хемосинтетики мають ЛПЕ. Синтез АТФ здійснюється при окисному фосфорилюванні. Хемосинтез – унікальний процес, характерний для невеликої групи прокаріот.
ПОЧАТКОВІ ЕТАПИ ОКИСНЕННЯ ВУГЛЕВОДІВ
Вуглеводи для більшості мікроорганізмів є основними поживними речовинами. Тому ці сполуки найчастіше використовують для їхнього культивування. Відомо декілька метаболічних шляхів розщеплення вуглеводів, які є спільними для процесів бродіння та дихання. До них відносять гліколіз (шлях Ембдена – Мейєргофа – Парнаса, фруктозо-дифосфатний шлях), окиснювальний пентозофосфатний шлях (шлях Варбурга – Діккенса – Хорекера, гексозомонофосфатний – ГМФ - шлях), шлях Ентнера – Дудорова (КДФГ – шлях, проміжний продукт 2-кето-3-дезокси-6-фосфоглюконова кислота).
Гліколіз (рис. 1). Характерною особливістю цього шляху катаболізму є утворення фруктозо-1,6-дифосфату – інтермедіату, якого немає у двох інших шляхах. На початкових етапах гліколізу витрачаються дві молекули АТФ на утворення фруктозо-1,6-дифосфату. Далі він розщеплюється на дві фосфорильовані тріози – фосфогліцериновий альдегід і діоксиацетонфосфат, які легко взаємно перетворюються. Окиснення тріозофосфату спряжене з відновленням НАД і супроводжується етерифікацією неорганічного фосфору, внаслідок чого утворюються 1,3-дифосфогліцеринова кислота. У процесі перетворення 1,3-дифосфогліцеринової кислоти в пировиноградну утворюються дві молекули АТФ: одна при дефосфорилюванні 1,3-дифосфогліцеринової кислоти, друга – при перетворенні фосфоенолпіровиноградної кислоти в піруват. Саме ці реакції і називають субстратним фосфорилюванням. Якщо врахувати, що в цих реакціях беруть участь дві молекули тріозофосфату, то вихід АТФ становитиме дві молекули на кожну молекулу тріоди. Крім того, має місце утворення двох молекул НАДН2.
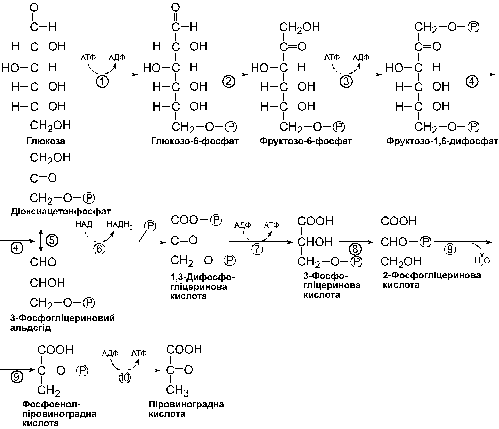
Рис. 1. Схема гліколізу. Ферменти: 1 – гексокіназа; 2 – глюкозофосфатізомераза; 3 – фосфофруктокіназа; 4 – фруктозодифосфатальдолаза; 5 – тріозофосфатізомераза; 6 – гліцеральдегід-3-фосфатдегідрогеназа; 7 – фосфогліцераткіназа; 8 – фосфогліцеромутаза; 9 – енолаза; 10 – піруваткіназа.
Гексозомонофосфатний шлях (рис. 2). Зі схеми гліколізу не можна було з’ясувати, яким чином мікроорганізми використовують як джерела енергії пентози та деякі інші вуглеводи, яким чином утворюється рибоза, необхідна для синтезу нуклеїнових кислот. З’ясовано ці питання у лабораторіях О. Варбурга, Ф. Діккеннса, Г. Хорекера.
Він включає початкове фосфорилювання глюкози і подальше окиснення глюкозо-6-фосфату до 6-фосфоглюконової кислоти. Декарбоксилювання 6-фосфоглюконату призводить до утворення пентозофосфатів. Після цього починається ланцюг трансальдолазних і транскетолазних реакцій, що характеризуються переносом С2 – і С3 – фрагментів між ізомерними пентозофосфатами. Це, з одного боку, забезпечує клітину різними попередниками для біосинтетичних процесів, а з другого, призводить до замикання циклу.

Рис. 2. Окиснювальний пентозофосфатний шлях. Ферменти: 1 – гексокіназа; 2 – глюкозо-6-фосфатдегідрогеназа; 3 – лактоназа; 4 – 6-фосфоглюконатдегідрогеназа; 5 – 5-фосфопентозоізомераза; 6 – 5-фосфопентозоепімераза; 7 – транскетолаза; 8 – трансальдолаза
Проходження шести циклів веде до повного окиснення молекули глюкозо-6-фосфату до СО2, що супроводжується утворенням дванадцяти відновлених молекул НАД.
6 глюкозо-6-фосфат + 12 НАДФ+ → 5 глюкозо-6-фосфат + СО2 + 12 НАДФ∙Н2 + Фн
Таким чином, ГМФ-шлях постачає клітину рибозофосфатом, необхідним для синтезу нуклеїнових кислот, еритрозофосфатом і НАДФ∙Н2 – для біосинтетичних реакцій.
Шлях Ентнера-Дудорова (рис. 3). Цей шлях катаболізму вуглеводів функціонує в обмеженій кількості мікроорганізмів, в основному у представників родини Pseudomonas.
Центральним інтермедіатом цього шляху є 2-кето-3-дезокси-6-фосфоглюконова кислота, тому його ще називають КДФГ-шляхом. Перші реакції є ідентичними ГМФ-шляху. Потім 6-фосфоглюконат дегідратується з утворенням КДФГ. Останній розщеплюється до пірувату і 3-фосфогліцеринового альдегіду.

Рис. 3. Шлях Ентнера – Дудорова. Ферменти: 1 – гексокіназа; 2 – глюкозо-6-фосфатдегідрогеназя а; 3 – 6-фосфоглюконатдегідратаза; 4 - 2-кето-3-дезокси-6-фосфоглюконат альдолаза
Фосфогліцериновий альдегід може під дією ферментів гліколізу перетворюватися до пірувату з утворенням двох молекул АТФ і відновленням молекул НАД. В результаті КДФГ-шляху утворюється по 1ё молю АТФ, НАДН2, НАДФН2.
Лекція № 10
Тема: БРОДІННЯ
Бродіння – це чисто мікробіологічний термін. Він характеризує спосіб добування енергії деякими групами мікроорганізмів, який відбувається в анаеробних умовах з окисно-відновним розщепленням органічних сполук і спосіб її запасання.
Бродіння – це спосіб отримання енергії, при якому АТФ утворюється в процесі анаеробного окиснення органічних субстратів у реакціях субстратного фосфорилювання.
В процесах бродіння утворюються органічні кислоти (молочна, масляна, оцтова, мурашина), спирти (етиловий, бутиловий, пропіловий), ацетон, СО2, Н2.
В залежності від того, який основний продукт нагромаджується в середовищі, розрізняють спиртове, молочнокисле, маслянокисле або ацетобутилове, пропіоновокисле та інші види бродінь.

