
- •1. Предмет і завдання курсу "біохімія"
- •2. Історія розвитку біохімії
- •3. Рівні структурної організації та хімічний склад живих організмів.
- •Відокремлюється тільки при хімічній взаємодії, зокрема при відщепленні гідроксильних (-он) груп від окремих молекул
- •Осмотичне утримування
- •Добова потреба організму у воді - 2,5...3,0 л.
- •4.Роль обміну речовин у життєдіяльності організму
- •1. Білки. Амінокислотний склад
- •2. Біологічна роль білків в організмі
- •3. Сучасні уявлення про структуру білків у білках розрізняють чотири рівні структурної організації:
- •4. Фізико-хімічні властивості білків
- •1. Нуклеїнові кислоти, їх хімічна природа
- •2. Відмінні властивості днк і рнк
- •3. Будова нуклеозидів та нуклеотидів
- •4. Атф - хімічна природа, біологічна роль
- •5.Структура нуклеїнових кислот
- •Тема 5. Ферменти
- •1. Ферменти як біологічні каталізатори
- •2. Хімічна природа та будова ферментів
- •3. Механізм дії ферментів та основи кінетики каталізу
- •4. Активність ферментів, вплив на неї різних факторів. Властивості ферментів
- •5. Номенклатура та класифікація ферментів
- •6. Використання ферментів у харчових технологіях
- •1. Класифікація вітамінів, їх біологічна роль
- •2. Будова вітамінів та їх добова потреба
- •3.Антивітаміни.Гормони
- •Тема 7. Основні поняття динамічної біохімії. Вільна енергія. Механізм дихального ланцюга
- •1. Динамічна біохімія. Вільна енерпя
- •(Окислення, відновлення, гідроліз, фосфорилювання таін.)
- •2. Біологічне окиснення. Тканинне дихання. Дихальний ланцюг
- •3. Окиснювальне фосфорилювання
- •Теми 8-9. Вуглеводи та їх обмін
- •1. Вуглеводи, їх функції
- •2. Класифікація вуглеводів
- •3. Характеристика основних представників вуглеводів
- •4. Перетравлювання та всмоктування вуглеводів в організмі людини
- •5. Взаємоперетворення моносахаридів в організмі
- •6. Анаеробне перетворення вуглеводів -хімізм гліколізу
- •7. Аеробне перетворення вуглеводів. Цикл кребса
- •8. Поняття про пентозний цикл перетворення вуглеводів
- •9. Біосинтез вуглеводів в організмі
- •9. Фотосинтез. Синтез оліго- та полісахаридів
- •25 – 30 Г/добу
- •Теми 10 -11. Ліпіди та їх обмін
- •1. Функції ліпідів в організмі
- •2. Класифікація ліпідів
- •3. Хімічна природа простих та складних ліпідів
- •4.Перетворення ліпідів у шлунково-кишковому тракті
- •5. Внутрішньоклітинний обмін ліпідів
- •6. Біосинтез ліпідів
- •Модуль 3 Тема 12. Білковий обмін
- •1. Перетворення білкових речовин у шлунково-кишковому тракті
- •2. Катаболізм білкових речовин в організмі. Хімізм перетворень
- •4. Синтез білків
- •Тема 13. Взаємозв'язок обмінних процесів
- •1. Взаємозв'язок основних видів обміну речовин
- •2. Ключові метаболіти - ланки переходу вуглеводного, білкового та ліпідного обмінів
- •2.Боєчко ф. Ф. Біологічна хімія. - к.: Вища шк., 1995. - 538 с.
- •3.Филиппович ю.Б. Основн биохимии. -м.: Висш. Шк., 1985. -503с.
- •4.Комов в.П., Шведова в.Н. Биохимия: Учеб. Для вузов. - м.: Дрофа, 2006. - 638с. Для студ Тмя та Тмо
2. Біологічне окиснення. Тканинне дихання. Дихальний ланцюг
!! Біологічне окиснення є основним джерелом енергії в організмі. В основі сучасних уявлень про біологічне окиснення лежать пероксидна теорія Баха і теорія Палладіна-Віланда про дегідрування субстратів.
► За теорією О.М.Баха, окиснення органічних речовин в організмі молекулярним киснем відбувається з утворенням пероксидних сполук, які мають важливе значення в активації молекулярного кисню. Такими речовинами є ненасичеш сполуки -лінолева, ліноленова, арахідонова кислоти, каротин, вітамін А таін.

► У біологічному окисненні беруть участь ферменти окисно-відновної системи, які містять як небілкові частини НАД+, НАДФ+, ФМН, ФАД, убіхінони та залізопорфіринові комплекси.
Тканинне дихання


Спряжуноче
(окиснювальне
фосфорилювання)
паралельно з процесами
окиснення у дихальному
ланцюгу відбувається
фосфорилювання АДФ з
утворенням АТФ
Неспряжуюче
(вільне окиснення)
біологічне окиснення
(нефосфорилюче окиснення
яке не супроводжується
утворенням і запасанням
енергії у виді АТФ. Енергія
вільного окиснення розсіюється у
виді теплоти
Дихальний ланцюг може забезпечувати як фосфорилююче окиснювання, так і вільне окиснення, а тому відіграє важливу роль в адаптації організмів до несприятливих умов. Зокрема, при охолодженні організму відбувається вільне окиснення, внаслідок якого підтримується стала температура тіла, посилюється біологічне окиснення.
Етапи біологічного окнснення
І - дегідрування субстратів - продуктів розпаду білків, жирів та вуглеводів за участю дегідрогеназ, які містять кофермент НАД*, НАДФ+ (вони є акцепторами водню), наприклад:

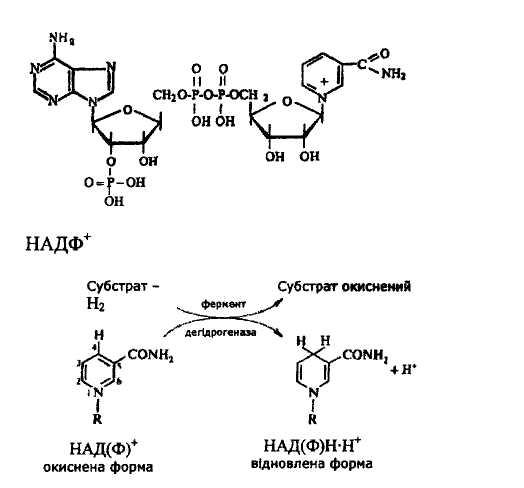
ІІ - акцептором атомів водню є група флавінових ферментів (містять коферменти ФМН і ФАД), наприклад:

ІІІ - акцептором водню є убіхінони (коензим Q), наприклад:

IV - з коензиму Q іони водню переходять у навколишнє середовище, а електрони поступають на цитохромну систему, яка складається з оксидоредуктаз, у яких лебідковою часткою є залізопорфірини. У цитохромній частині є фермент цитохромоксидаза, який переносить електрони з коензиму Q на кисень, останній, сполучаючись з іонізованими атомами водню, утворює воду, наприклад:
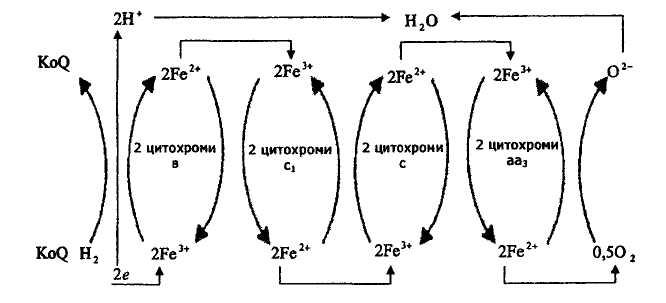
Під час клітинного дихання крім води утворюється СО2 і виділяється енергія.
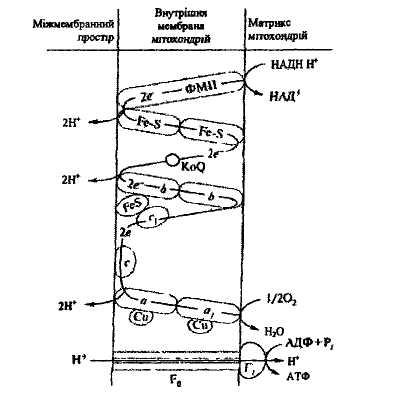
Загальний вигляд дихального ланцюга мітохондрій та комплексів І, II, Ш, IV, які переносять електрони:

3. Окиснювальне фосфорилювання
► Окислювальне фосфорилювання - це фосфорилювання АДФ, яке пов'язане з процесами окиснення в організмі та супроводжується утворенням АТФ.
Два
рівні окиснювального фосфорилювання
Субстратне фосфорилювання
(3-фосфогліцериновий альдегід,
2-фосфогліцеринова кислота тощо).
Дихальний ланцюг
мітохондрій
(проходить у 4 етапи
за схемою)
 Схема
дихального ланцюга
Схема
дихального ланцюга

Шляхи утворення енергії в клітині

Окиснювальне фосфорилювання - це спряження двох клітинних процесів: екзергонічного окиснення відновлених молекул (НАДН*Н+ або ФАД*Н2) і ендергонічного фосфорилювання АДФ з утворенням АТФ.
Механізм окиснювального фосфорилювання пояснюється З гіпотезами: хімічною, хеміосмотичною, конформаційною.
Кількісно спряження і фосфорилювання характеризуються коефіцієнтом окиснювального фосфорилювання (Р/О).
Коефіцієнт Р/О - це відношення зменшення молів неорганічного фосфату (Н3РО4), який витрачається на синтез АТФ, до кількості поглинутого кисню.
Захист від активних форм кисню(АФК)


Нефермантивний
Ферментативний
Неферментативний захист здійснюється з допомогою антиоксидантів — речовин, які виступають як пастки кисневих радикалів. Ці речовини взаємодіють з АФК, за рахунок чого знижують їх реакційну активність та розривають ланцюговий процес утворення.
Антиоксидантну дію мають аскорбінова кислота (вітамін С) та α -токоферол (вітамін E1), а також ряд інших природних речовин: β -каротин, сечова кислота, трипептид глутатіон, дипептид карнозин, таурин та ін.
Ферментативний захист здійснюється за допомогою супероксиддисмутази (СОД), специфічного ферменту, який каталізує реакцію дисмутації, в якій супероксид виступає одночасно як окисник і як відновник:
![]()
Утворений пероксид водню розпадається до води в присутності іншого ферменту — каталази:
2 Н2О2
каталаза
2Н2О+О2
Н2О2
каталаза
2Н2О+О2
Пероксид водню також може розщеплюватися під дією пероксидази — ферменту, який використовує за донора різноманітні органічні сполуки, наприклад, поліфеноли:
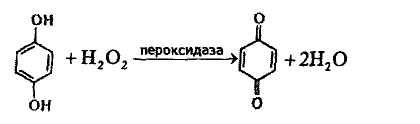
Пероксидаза міститься у живих тканинах (кров, печінка, нирки), але особливо активні ці ферменти у тканинах вищих рослин.
СОД і каталаза знайдені у всіх типах про- та еукаріотичних аеробних клітин. Вони присутні не тільки у клітинах тваринних тканин, але і у плазмі крові, лімфі, синовіальній рідині. У клітинах найбільша кількість цих ферментів міститься у пероксисомах та мітохондріях.
СОД відноситься до металоферментів, у яких у активному центрі йде відновлення та окислення іона металу Zn2+, Са2+.
У захисті тканин від АФК приймає участь ще один фермент - глутатіонпероксидаза (ГП), яка відновлює пероксид водню (а також органічні гідропероксиди R - О - ОН), донором водню у цій реакції є відновлений трипептид глутатіон (Глу - SН):
![]()
де Глу - S- S - Глу - окислений глутатіон.
