
1)Біологія — сукупність наук про живу природу, про живих істот, що населяють Землю чи вже вимерли, їхні функції, розвиток особин і родів, спадковість, мінливість, взаємні стосунки, систематику, поширення на Землі; про зв'язки між живими істотами і живих істот з неживою природою. Біологія встановлює загальні закономірності, властиві життю у всіх його проявах.
Завдання біології Завданням біології є всебічне вивчення всієї сукупності організмів як сучасних, так і викопних. Число сучасних видів організмів досягає близько 2 млн., в тому числі понад 1,5 млн. тварин. Приблизно стільки ж відомо викопних видів. Біологи досліджують будову рослин і тварин, їх життєві функції, спосіб життя та поширення на Землі, їхній історичний розвиток і значення, шляхи використання тощо. Ці дослідження дають можливість все більше і раціональніше використовувати в інтересах людини корисні форми, все успішніше знищувати шкідливі. Питання про історичний розвиток органічного світу й походження людини є одними з найважливіших в сучасній біології; вони завжди стояли в центрі боротьби між матеріалізмом та ідеалізмом. Саме розділ біології, що охоплює ці питання, зазнавав і зазнає сильних нападок з боку реакційних сил в біології. Біологія тепер — складна система наукових дисциплін, кожна з яких має свої завдання, свої методи й об'єкти дослідження.
2)Історія становлення і розвитку Термін «біологія» був вперше вжитий в 1797 р. німецьким професором анатомії Теодором Рузом (1771—1803), пізніше в 1800 р. термін застосував професор Дерптського університету Карл Бурдах (1776—1847), а в 1802 р. — Жан Батист Ламарк (1744—1829) і Лудольф Тревіранус (1779—1864). Біологія як наука виникла при пізнанні людиною оточуючої природи, у зв'язку з матеріальними умовами життя суспільства, розвитком виробничих відносин, медицини, практичних потреб людини. У процесі поступового розвитку й у міру збагачення новими фактами біологія перетворилася в комплекс наук, що досліджує закономірності, властиві живим істотам з різних сторін. Сучасна біологія — це складний високодиференційований комплекс фундаментальних і прикладних досліджень живої природи, яка складається з багатьох біологіч-них дисциплін, що спеціалізуються на вивченні структур-но-функціональних особливостей певних організмів. Теоретичний фундамент біології був закладений еволюційним вченням Дарвіна, клітинною теорією Шванна і целюлярною патологією Вірхова. Перші систематичні спроби пізнання живої природи були зроблені античними лікарями і філософами (Гіппократ, Арістотель, Теофраст, Гален). Їхні праці, продовжені в епоху Відродження, поклали початок ботаніці і зоології, а також анатомії і фізіології людини (Везалій і ін.). У 17 — 18 століттях в біологію проникають експериментальні методи. На основі кількісних вимірів і застосування законів гідравліки був відкритий механізм кровообігу (Вільям Гарвей, 1628). Винахід мікроскопа розсунув границі відомого світу живих істот, поглибив уявлення про їхню будову. Одне з головних досягнень цієї епохи створення системи класифікації рослин і тварин (Карл Лінней, 1735). Разом з тим переважали умоглядні теорії про розвиток і властивості живих істот (самозародження, преформації й ін.). У 19 столітті в результаті різкого збільшення кількості біологічних досліджень (нові методи, експедиції в тропічні і малодоступні райони Землі та ін.), нагромадження і диференціації знань сформувалося багато спеціальних біологічних наук. Так, в ботаніці і зоології появляються розділи, які вивчають окремі систематичні групи, розвиваються ембріологія, гістологія, мікробіологія, палеонтологія, біогеографія тощо. Серед досягнень біології клітинна теорія (Т. Шванн, 1839), відкриття закономірностей спадковості (Грегор Мендель, 1865). До фундаментальних змін у біології призвело еволюційне вчення Чарльза Дарвіна (1859). Для біології 20 століття характерні дві взаємозалежні тенденції. З одного боку, сформувалося уявлення про якісно різні рівні організації живої природи: молекулярний (молекулярна біологія, біохімія й інші науки, які поєднують поняттям фізико-хімічна біологія), клітинний (клітинна біологія), рівень організмів (анатомія, фізіологія, ембріологія), популяційно-видовий (екологія, біогеографія). З іншого боку, прагнення до цілісного, синтетичного пізнання живої природи призвело до прогресу наук, які вивчають певні властивості живої природи на всіх структурних рівнях її організації (генетика, систематика, еволюційне вчення тощо). Разючих успіхів починаючи з 1950-х років досягла молекулярна біологія, яка розкрила хімічні основи спадковості (будова ДНК, генетичний код, матричний принцип синтезу біополімерів). Вчення про біосферу (В. І. Вернадський) розкрило масштаби геохімічної діяльності живих організмів, їхній нерозривний зв'язок з неживою природою. Практичне значення біологічних досліджень і методів (у тому числі генної інженерії, біотехнології) для медицини, сільського господарства, промисловості, розумного використання природних ресурсів і охорони природи, а також проникнення в ці дослідження ідей і методів точних наук висунули біологію в середині 20 століття на передові рубежі природознавства.
3)Рівень – ступінь диференціації біологічного об’єкта.
Виділення рівнів організації біологічних систем має за мету розкриття сутності живої природи в її русі, у пізнанні законів розвитку.
Виділяють нижчі і вищі рівні.
Нижчі рівні організації життя:
- Клітинний - (жива матерія існує тільки на рівні клітини).
- Молекулярний (предмет молекулярної біології, будова білків, нуклеїнових кислот, жирів і інших речовин, їх роль у життєдіяльності).
- Тканинний – (жива матерія існує тільки на рівні органів)
- Системний.
Вищі рівні організації життя.
- Організмовий (вивчення організму як єдиного цілого).
- Популяційний (вивчення популяції)
- Видовий.
- Біогеоценотичний (вивчення проблем взаємовідносин організмів у біогеоценозах)
- Біосферний – вирішуються глобальні проблеми, зв’язані з функціями живої речовини на планеті, вивчення змін в біосфері, зв’язані з діяльністю людини.
23)Трисомии, синдром (болезнь) Дауна, Патау, Эдвардса у детей
Наиболее часто у человека встречаются трисомии по 21-й, 13-й и 18-й паре хромосом.
Синдром (болезнь) Дауна у детей, ребенка
Синдром (болезнь) Дауна - синдром трисомии 21 - самая частая форма хромосомной патологии у человека (1:750). У мальчиков и девочек патология встречается одинаково часто.
Достоверно установлено, что дети с синдромом Дауна чаще рождаются у пожилых родителей. Если возраст матери 35-46 лет, то вероятность рождения больного ребенка возрастает до 4,1 %. Возможность возникновения повторного случая заболевания в семье с трисомией хромосомы 21 составляет 1-2 % (с возрастом матери риск увеличивается).
Для больных характерны округлой формы голова с уплощенным затылком, узкий лоб, широкое, плоское лицо. Типичны эпикант, запавшая спинка носа, косой (монголоидный) разрез глазных щелей, пятна Брушфильда (светлые пятна на радужке), толстые губы, утолщенный язык с глубокими бороздами, выступающий изо рта, маленькие, округлой формы, низко расположенные ушные раковины со свисающим завитком, недоразвитая верхняя челюсть, высокое нёбо, неправильный рост зубов, короткая шея.
Из пороков внутренних органов наиболее типичны пороки сердца (дефекты межжелудочковой или межпредсердной перегородок, фиброэластоз и др.) У маленьких детей резко выражена мышечная гипотония, а у детей старшего возраста часто обнаруживается катаракта. С самого раннего возраста отмечается отставание в умственном развитии. Средняя продолжительность жизни при синдроме Дауна составляет 36 лет.
Диагностика синдрома Дауна
Для дородового выявления синдрома Дауна у плода предложена система пренатальной диагностики. Скрининг I триместра проводится на сроке беременности 11-13 недель и включает выявление специфических УЗИ-признаков аномалии и определение уровня биохимических маркеров (ХГЧ, РАРР-А) в крови беременной. Между 15 и 22 неделями беременности выполняется скрининг II триместра: акушерское УЗИ, анализ крови матери на альфа-фетопротеин, ХГЧ и эстриол. С учетом возраста женщины рассчитывается риск рождения ребенка с синдромом Дауна (точность - 56-70%; ложноположительные результаты - 5%).
Беременным из группы риска по рождению ребенка с синдромом Дауна предлагается прохождение пренатальной инвазивной диагностики: биопсии хориона, амниоцентеза или кордоцентеза с кариотипированием плода и консультация медицинского генетика. При получении данных за наличие у ребенка синдрома Дауна решение вопроса о пролонгации или прерывании беременности остается за родителями.
Новорожденные с синдромом Дауна в первые дни жизни нуждаются в провдении ЭхоКГ, УЗИ брюшной полости для раннего выявления врожденных пороков развития внутренних органов; осмотре детского кардиолога, детского хирурга, детского офтальмолога, детского травматолога-ортопеда.
Синдром Патау у детей, ребенка
Синдром Патау - синдром трисомии 13 - встречается с частотой 1:6000. Между частотой возникновения синдрома Патау и возрастом матери прослеживается зависимость, хотя и менее строгая, чем в случае болезни Дауна.
При синдроме Патау наблюдаются тяжелые врожденные пороки. Дети с синдромом Патау рождаются с массой тела ниже нормы. У них выявляются умеренная микроцефалия, нарушение развития различных отделов ЦНС, низкий скошенный лоб, суженные глазные щели, расстояние между которыми уменьшено, микрофтальмия и колобома, помутнение роговицы, запавшая переносица, широкое основание носа, деформированные ушные раковины, расщелина верхней губы и нёба, полидактилия, флексорное положение кистей, короткая шея. У 80 % новорожденных встречаются пороки развития сердца: дефекты межжелудочковой и межпредсердной перегородок, транспозиции сосудов и др. Наблюдаются фиброкистозные изменения поджелудочной железы, добавочные селезенки, эмбриональная пупочная грыжа. Почки увеличены, имеют повышенную дольчатость и кисты в корковом слое, выявляются пороки развития половых органов. Характерна задержка умственного развития.
Большинство больных детей с синдромом Патау (98 %) умирают в возрасте до года, оставшиеся в живых страдают глубокой идиотией.
Диагностика синдрома Патау
Пренатальная диагностика хромосомных болезней плода (синдрома Патау, синдрома Дауна, синдрома Эдвардса) одинакова. На первом этапе скрининга производится определение биохимических маркеров (бета-ХГЧ, РАРР-А и др.) и УЗИ-исследование, на основании которых рассчитывается риск рождения больного ребенка для данной женщины.
Женщинам, попавшим в группы риска, предлагается проведение инвазивной пренатальной диагностики: биопсии ворсин хориона (8-12 недели), амниоцентеза (14-18 недели) или кордоцентеза (после 20-й недели гестации). В полученных образцах материала плода проводится поиск трисомии по 13-ой хромосоме методом кариотипирования с дифференциальной окраской хромосом или КФ-ПЦР.
Если дородовая диагностика синдрома Патау по каким-либо причинам не проводилась, хромосомная аномалия может быть заподозрена у новорожденного неонатологом на основании ярких клинических признаков и дерматографических изменений. Однако цитогенетический диагноз трисомии 13 может быть получен только после определения хромосомного набора ребенка.
Новорожденные с предполагаемым или установленным диагнозом синдрома Патау нуждаются в углубленном комплексном обследовании для выявления тяжелых пороков развития (эхокардиографии, УЗИ органов брюшной полости и почек,нейросонографии, КТ головного мозга и др.). Для определения показаний к оперативному лечению, в первую очередь, необходимы консультации детского кардиохирурга и детского хирурга общего профиля.
Прогноз и профилактика синдрома Патау
В большинстве случаев плод синдромом Патау погибает антенатально или рождается мертвыми. Живорожденные дети также имеют неблагоприятный прогноз для жизни. В большинстве случаев продолжительность их жизни не превышает одного года.
Специфические методы профилактики синдрома Патау не разработаны. При наличии хромосомных заболеваний в предыдущих поколениях или случаев мертворождения перед планированием беременности родителям необходимо пройти медико-генетического консультирование.
Синдром Эдвардса у детей
Синдром Эдвардса - синдром трисомии 18 - встречается с частотой примерно 1:7000. Дети с трисомией 18 чаще рождаются у пожилых матерей, взаимосвязь с возрастом матери менее выражена, чем в случаях трисомии хромосомы 21 и 13. Для женщин старше 45 лет риск родить больного ребенка составляет 0,7 %. У девочек встречается значительно чаще, чем у мальчиков.
Дети с трисомией 18 рождаются с низким весом, хотя сроки беременности нормальные или даже превышают норму. Фенотипические проявления синдрома Эдвардса многообразны. Наиболее часто отмечаются аномалии мозгового и лицевого черепа, мозговой череп долихоцефалической формы. Нижняя челюсть и ротовое отверстие маленькие. Глазные щели узкие и короткие. Ушные раковины деформированы и в подавляющем большинстве случаев расположены низко, несколько вытянуты в горизонтальной плоскости. Мочка, а часто и козелок отсутствуют. Наружный слуховой проход сужен, иногда отсутствует. Грудина короткая, из-за чего межреберные промежутки уменьшены и грудная клетка шире и короче нормальной. В 80 % случаев наблюдается аномальное развитие стопы: пятка резко выступает, свод провисает (стопа-качалка), большой палец утолщен и укорочен. Из дефектов внутренних органов наиболее часто отмечаются пороки сердца и крупных сосудов: дефект межжелудочковой перегородки, аплазии одной створки клапанов аорты и легочной артерии. У всех больных наблюдаются гипоплазия мозжечка и мозолистого тела, изменения структур олив, выраженная умственная отсталость, снижение мышечного тонуса.
Продолжительность жизни детей с синдромом Эдвардса невелика: 60 % детей умирают в возрасте до 3 мес, до года доживает лишь один ребенок из десяти; оставшиеся в живых - глубокие олигофрены.
Диагностика синдрома Эдварда
Диагноз синдрома Эдвардса может быть поставлен путем определения при физическом осмотре всех вышеперечисленных внешних симптомов. Более точный диагноз можно поставить, проведя анализ «кариотипирования», который включает в себя взятие образцов крови ребенка для определения хромосомного состава.
В связи с большим количеством пороков развития и очень низким процентом выживаемости детей с синдромом Эдвардса, в настоящее время разработаны методы антенатальной диагностики. Одной из первых и доступных методик, которые осуществляют во всех женских консультациях, является УЗИ плода. На УЗИ в ранних сроках беременности можно заподозрить пороки развития головного мозга и конечностей, также наличие обильного количество околоплодной жидкости, что должно насторожить врача. При получении данных результатов необходимо отправить беременную на более детальное и прицельное наблюдение в стационар.
В стационаре должны выполнить все необходимые общеклинические анализы и провести более специфические тесты, такие как эхография, доплерометрия, исследование сывороточных маркеров крови: β-субъединицы хорионического гонадотропина (βХГ), α-фетопротеина (АФП), эстриола (ЕЗ), 17-окси прогестерона. Для оценки степени риска рождения детей с хромосомной патологией во всех наблюдениях используют специально разработанную компьютерную программу PRISCA, учитывающую возраст женщины, показатели сывороточных маркеров и срок беременности. Также необходимо выполнить трансабдоминальный амниоцентез с последующим кордоцентезом. В амниотических водах при наличии синдрома Эдвардса будет определяться: АФП, 17-ОП, ЕЗ, а в крови плода будет определяться кариотип трисомии 18 хромосомы.
Медико-генетичне консультування
Генетична консультація надає допомогу у вирішенні проблем, пов'язаних з ризиком генетичних захворювань. До генетичної консультації найчастіше звертаються подружжя, в яких перша дитина народилася з вродженим дефектом чи з іншою патологією.
В ідеальних умовах подружжю слід звернутися до генетичної консультації та обговорити з лікарем ризик народження дитини з вродженою аномалією ще до зачаття чи в перші 3 міс вагітності.
Існують категорії сімей, яким необхідне генетичне консультування, навіть якщо в роду нема випадків спадкової патології. Це сім'ї, в яких один або обидва партнери мають шкідливі звички, професійні шкідливості; якщо жінка старша 35-річного віку, а також коли в анамнезі були спонтанні викидні, мертвонародження.
Слід вважати обов'язковим для кожної родини з встановленими випадками спадкової хвороби звертатися до генетичної консультації для обговорення питання про планування сім'ї.
Основними задачами генетичного консультування є такі:
1) уточнення генетичного діагнозу та визначення індивідуальної величини генетичного ризику для конкретної родини;
2) вирішення питання про планування вагітності та вибір методу пренатальної діагностики
26)Плейотропія. Це вплив одного гена на розвиток двох і більше ознак (множинне дію гена). Так, Д. К. Бєляєв та А. І. Желєзнова встановили, що у норок більшість мутацій, що супроводжуються зміною забарвлення волосяного покриву, рецессивно і в силу плейотропії при цьому знижуються плодючість і життєздатність тварин. Явище плейотропії пояснюється тим, що гени плейотропійного дії контролюють синтез ферментів, які беруть участь у численних обмінних процесах в клітці і в організмі в цілому і тим самим одночасно впливають на прояв і розвиток інших ознак. На підставі розглянутого дії генів-модифікаторів, взаємодії генів і плейотропних дії генів можна бачити, що формування ознаки - дуже складне явище в якому бере участь не один ген, а певною мірою весь генотип особини. Вплив в цілому генотипу на розвиток ознаки призвело до формування понять «генотипическая середовище» і «генний баланс». Під генотипической середовищем розуміють комплекс генів організму, в якому відбувається дія досліджуваного гена. Генний баланс - співвідношення і взаємовідношення між собою всіх генів, що впливають тією чи іншою мірою на розвиток ознаки.
ВЗАЄМОДІ́Я ГЕ́НІВ — це одночасна дія декількох генів. Розрізняють дві основні групи В.г.: взаємодія між алельними генами і між неалельними генами. Проте слід розуміти, що це не фізична взаємодія самих генів, а взаємодія первинних і вторинних продуктів, які зумовлюють ту чи іншу ознаку. У цитоплазмі відбувається взаємодія між білками-ферментами, синтез яких визначається генами, або між речовинами, які утворюються під впливом цих ферментів. Можливі такі типи взаємодії:
1) для утворення певної ознаки необхідна взаємодія двох ферментів, синтез яких визначається двома неалельними генами;
2) фермент, який синтезувався за участю одного гена, повністю пригнічує або інактивує дію ферменту, утвореного іншим неалельним геном;
3) два ферменти, утворення яких контролюється двома неалельними генами, впливають на одну ознаку або на один процес так, що їх сумісна дія приводить до виникнення і підсилення прояву ознаки.
Відомі такі форми взаємодії між алельними генами: повне, неповне домінування, кодомінування і наддомінування. Основна форма взаємодії — повне домінування, яке вперше описано Г. Менделем. Суть його полягає в тому, що в гетерозиготного організму прояв одного з алелів домінує над проявом іншого. У медичній практиці з 2 тис. моногенних спадкових хвороб майже у половини відмічають домінування прояву патологічних генів над нормальними. Неповне домінування — така форма взаємодії, коли у гетерозиготного організму (Аа) домінантний ген (А) не повністю пригнічує рецесивний ген (а), внаслідок чого проявляється проміжна між батьківськими ознака. При кодомінуванні у гетерозиготних організмів кожний з алельних генів викликає формування залежного від нього продукту, тобто виявляються продукти обох алелів. Класичним прикладом такого прояву є система групи крові АВ0, коли еритроцити людини несуть на поверхні антигени, що контролюються обома алелями. При наддомінуванні домінантний ген у гетерозиготному стані виявляється сильніше, ніж у гомозиготному.
Розрізняють 4 основні типи взаємодії неалельних генів: комплементарність, епістаз, полімерію і модифікуючу дію (плейотропію). Комплементарність — такий тип взаємодії неалельних генів, коли один домінантний ген доповнює дію іншого неалельного домінантного гена, і вони разом визначають нову ознаку, яка відсутня у батьків. Причому відповідна ознака розвивається тільки в присутності обох неалельних генів. Прикладом комплементарної взаємодії генів у людини може бути синтез захисного білка інтерферону. Його утворення в організмі пов’язане з комплементарною взаємодією двох неалельних генів, розташованих у різних хромосомах. Епістаз — це така взаємодія неалельних генів, за якої один ген пригнічує дію іншого неалельного гена. Пригнічення можуть викликати як домінантні, так і рецесивні гени, залежно від цього розрізняють епістаз домінантний і рецесивний. Пригнічувальний ген отримав назву інгібітора, або супресора. Гени-інгібітори в основному не детермінують розвиток певної ознаки, а лише пригнічують дію іншого гена. У людини прикладом може бути «бомбейський фенотип». У цьому разі рідкісний рецесивний алель у гомозиготному стані пригнічує активність гена, який визначає групу крові системи АВ0. Більшість кількісних ознак організмів визначається декількома неалельними генами (полігенами). Взаємодія таких генів у процесі формування ознаки називається полімерною. У цьому разі два або більше домінантних алелі однаковою мірою впливають на розвиток однієї й тієї ж ознаки. Так, пігментація шкіри у людини визначається 5 або 6 полімерними генами. У корінних жителів Африки (негроїдної раси) переважають домінантні алелі, у представників європеоїдної раси — рецесивні. Тому мулати мають проміжну пігментацію, але в шлюбах мулатів можлива поява як більш, так і менш інтенсивно пігментованих дітей. Багато морфологічних, фізіологічних і патологічних особливостей людини визначається полімерними генами: зріст, маса тіла, величина артеріального тиску та ін. Розвиток таких ознак у людини підпорядковується загальним законам полігенного успадкування і залежить від умов середовища. У цих випадках спостерігається, напр., схильність до гіпертонічної хвороби, ожиріння тощо. Ці ознаки за сприятливих умов середовища можуть не проявитися або проявитися незначною мірою. Плейотропія — це залежність кількох ознак від одного гена, тобто множинна дія одного гена. У людини відома спадкова хвороба — арахнодактилія («павучі пальці» — дуже тонкі і довгі пальці), або хвороба Марфана. Ген, який відповідає за цю хворобу, викликає порушення розвитку сполучної тканини й одночасно впливає на розвиток кількох ознак: порушення будови кришталика ока, аномалії у серцево-судинній системі.
27)Кроссинговер —перекрест,взаимный обмен гомологичными участками гомологичных хромосом в результате разрыва и соединения в новом порядке их нитей — хроматид; приводит к новым комбинациям аллелей разных генов. Важнейший механизм, обеспечивающий комбинативную изменчивость в популяциях и тем самым дающий материал для естественного отбора. Протекает в мейотически, реже — вмитотически делящихся клетках. Может приводить к перекомбинации больших участков хромосомы с несколькими генами или частей одного гена (внутригенный кроссинговер), обеих нитей молекулы ДНК или только одной. Частота кроссинговера между генами отражает расстояние между ними в хромосоме. Иными словами, в паре гомологичных хромосом между несестринскими хроматидами происходит обмен гомологичными участками. Поскольку в паре хромосом одна хромосома происходит от матери, а другая — от отца, процесс кроссинговера ведет к внутрихромосомным рекомбинациям наследственности. Молекулярный механизм кроссинговера окончательно не выяснен.
Х-зчеплене успадкування
Гени,
локалізовані в статевих хромосомах,
позначають як зчеплені з підлогою. Вони
по-різному розподіляються у чоловіків
і жінок. Зчеплені з підлогою гени можуть
розташовуватися як на X, так і на
Y-хромосомі. Проте в клінічній генетиці
практичне значення мають Х-зчеплені
захворювання, тобто такі, коли патологічний
ген розташований на Х-хромосомі.
Розподіл
Х-зчепленого ознаки залежить від
розподілу Х-хромосоми, що несе аномальний
ген. Враховуючи, що у жінок є дві
Х-хромосоми, а у чоловіків одна, можливі
такі варіанти генотипів: у чоловіка -
ХАY, ХаY, у жінки - ХАХА, хаха, ХаХа.
Х-зчеплене
рецесивне захворювання (або ознака)
завжди проявляється у чоловіків, що
мають відповідний ген, а у жінок-тільки
у випадках гомозиготного стану (що
спостерігається вкрай рідко). Прикладом
Х-зчепленого рецесивного захворювання
є гемофілія А, що характеризується
порушенням згортання крові внаслідок
дефіциту VIII фактора - антігемофіль-ного
глобуліну А. Родовід хворого з гемофілією
представлена ??на рис. IX.11. Клінічно
захворювання проявляється частими
тривалими кровотечами навіть при
невеликому пораненні, крововиливами в
органи і тканини. Частота захворювання
становить 1 на 10 000 новонароджених
хлопчиків. Використовуючи наведені
вище позначення, можна визначити всі
можливі генотипи в потомстві хворого
чоловіка і здорової жінки.
Згідно
зі схемою всі діти будуть фенотипічно
здорові, але ге-нотіпіческі всі дочки
є носіями гена гемофілії.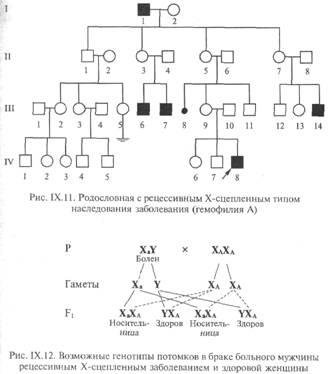
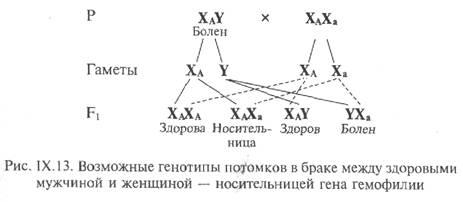
Якщо жінка - носій гена гемофілії, вийде заміж за здорового чоловіка, можливі такі варіанти генотипів потомства. Дочки в 50% випадків будуть носіями патологічного гена, а для синів існує 50%-ний ризик бути хворим на гемофілію. Таким чином, основними ознаками Х-зчепленого рецесивного успадкування є наступні: 1) захворювання зустрічається в основному у осіб чоловічої статі; 2) ознака (захворювання) передається від хворого батька через його фенотіпіческм здорових дочок половині його онуків; 3) захворювання ніколи не передається від батька до сина; 4 ) у носіїв іноді виявляються субклінічні ознаки патології. Домінантний Х-зчеплений тип успадкування захворювання На відміну від захворювань з Х-зчепленим рецесивним типом успадкування захворювання з Х-сцсштенним домінантним типом успадкування зустрічаються в 2 рази частіше у жінок, ніж у чоловіків. Головна характеристика Х-зчепленого домінантного успадкування полягає в тому, що хворі чоловіки передають аномальний ген (або захворювання) всім своїм дочкам і не передають його синам. Хвора жінка передає Х-зчеплений домінантний ген половині своїх дітей незалежно від статі (рис. IX.14). Особливості розподілу хворих у родоводі залежать від статі ураженого батька.
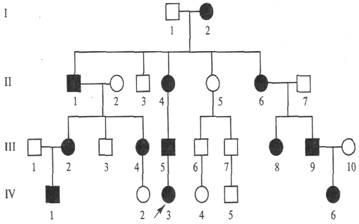
Родовід з Х-зчепленим домінантним типом успадкування захворювання (вітамін-Д-резистентний рахіт)
28) Мінливість — загальна властивість всіх організмів яка відображає взаємозв’язок організму з навколишнім середовищем і зачіпає будь-які його ознаки та генетичні структури: гени, хромосоми і генотип в цілому.
Мінливість, яка з’являється у зв’язку із зміною генетичного матеріалу, називається спадковою або генотипною.
Одним з результатів спадкової мінливості є утворення нових організмів (нових генотипів), що забезпечує різноманітність життя, її продовження і еволюційний розвиток.
Генотипна мінливість широко представлена в природі. Іноді це дуже великі зміни, які проявляються, наприклад, в ознаках махровості у квіток, коротконогими у тварин (у овець, курей), але частіше це дрібні, ледь помітні відхилення від норми.
Зміна генотипу призводить, як правило, до зміни фенотипу.
В основі спадкової мінливості зазвичай лежать нові комбінації алелей, які утворюються в процесі мейозу, при заплідненні або мутації. Тому спадкову (генотипическую) мінливість поділяють на два види: комбинативную і мутационную. В обох випадках порушується структура гена і структура хромосом, т. Е. Змінюється послідовність нуклеотидів в ДНК, число хромосом, а також відбувається розщеплення пар алелів генів; іншими словами, змінюється генотип. Все це і призводить до появи нових успадкованих ознак.
Спадкова мінливість у свою чергу поділяється на комбінативну і мутаційну.
Комбінативна (рекомбінативна) мінливість виникає при гібридизації внаслідок незалежного перекомбінування генів та хромосом. Тут відбувається перекомбінація певних генетичних угруповань без якісної і кількісної зміни генетичного матеріалу.
Мутаційна мінливість виникає раптово, в результаті взаємодії організму і середовища, без схрещування. Вона зумовлена якісною зміною генетичного матеріалу, виникненням нових варіантів дискретних одиниць генетичного матеріалу, перш за все нових алелів.
29) Хімічна структура гену
Докладніше: ДНК та РНК
У переважної більшості живих організмів гени закодовані в ланцюгах ДНК. ДНК (дезоксирибонуклеїнова кислота) є полімером з чотирьох типів нуклеотидів, кожен з яких складається з моносахариду класу пентоз (2'-дезоксирибози),фосфатної групи, і одного з чотирьох азотистих основ: аденіну (А), цитозину (Ц), гуаніну (Г)і тиміну (Т).
Найпоширенішою формою ДНК в клітині є структура у формі правої подвійної спіралі з двох окремих ниток ДНК. Азотисті основи одного з ланцюжків сполучені з азотистими основами іншого ланцюжка водневими зв'язками згідно з принципомкомплементарності: аденін з'єднується тільки з тиміном (два водневих зв'язки), гуанін — тільки з цитозином (три водневих зв'язки).
Завдяки хімічним особливостям зв'язку між пентозними залишками нуклеотидів, ДНК мають полярність. Один кінець ДНК-полімеру закінчується 3-гідроксильною (3 —ОН) групою дезоксирибози і називається 3' (три-прайм), а інший - 5-фосфатною групою (5 —РО3) і називається 5' (п'ять-прайм). Полярність ланцюжка грає важливу роль в клітинних процесах. Наприклад, при синтезі ДНК подовження ланцюжка можливе тільки шляхом приєднання нових нуклеотидів до вільного 3' кінця.
24)Летальні гени
Зміна розщеплення за фенотипом у відношенні 3:1 у другому поколінні моногибридного схрещування буває пов'язано з різною життєздатністю зигот Ф2 . Різна життєздатність зигот межет бути обумовлена ??наявністю летальних генів. Летальним називається ген, що викликає порушення в розвитку організму, що приводить його до загибелі або каліцтва. Вивчення вроджених аномалій показало, що при різних літальних генах загибель особин буває різною і може відбуватися на різних стадіях розвитку. За класифікацією, запропонованої Розенбауером (1969), гени, що викликають загибель 100% особин до досягнення ними п'ловой зрілості, називаються летальними, більше 50%-сублетальні (напівлетальними) і менше 50% - субвітальних. Однак слід зазначити, що поділ це до деякої міри умовно і іноді не має чітких кордонів. Прикладом може служити сцепленная з підлогою голость у курей. Майже половина голих курчат гине в останні 2-3 дні інкубації. З числа вилупилися близько половини курчат гине до 6-тижневого віку, якщо їх вирощують при температурі 32-35 "С. Але якщо температура в брудерах буде підвищена на 5,5 ° С, то загине значно менше голих курчат. У 4-5 міс у голих курчат виростає рідкісне оперення і вони вже в змозі переносити досить низькі температури.
У природних умовах ця мутація, очевидно, буде летальної і призведе до 100%-ної загибелі птахів. Наведений приклад показує , що характер прояву напівлетальний гена значною мірою може залежати від умов середовища. Летальні гени можуть бути домінантними і рецесивними. У числі перших летальних факторів був відкритий аллель, що обумовлює жовте забарвлення мишей. Ген жовтого забарвлення є домінантним (Y). Його рецесивний аллель (у) в гомозиготному стані обумовлює появу чорного забарвлення. Схрещування жовтих мишей між собою давало в потомстві дві частини особин жовтих і одну частину чорних, тобто виходило розщеплення 2:1, а не 3: 1, як випливало з правила Менделя. Виявилося, що всі дорослі миші гетерозіготни (Yy). При схрещуванні між собою вони мали дати одну частину гомозиготного потомства по жовтому забарвленню (IT), але воно гине ще в ембріональному періоді, дві частини гетерозигот ( Yy) будуть жовтими і одна частина гомозигот за рецесивним ознакою (уу) буде чорної. Схема схрещування виглядає так: Таким же чином успадковується сіре забарвлення шерсті у каракульських овець (сокільських, Маліч та ін), платинова забарвлення у лисиць, розподіл луски у лінійних коропів і т. д. Летальні гени в більшості випадків рецесивні і тому тривалий час можуть перебувати в прихованому стані.
Абсолютно здорове і нормальне за фенотипом тварина може бути носієм летального гена, дія якого виявляється тільки при переході в гомозиготний стан. В гомозиготний стан летальні гени найчастіше переходять при родинному спарюванні. У практиці тваринництва при розведенні коней був випадок загибелі 25 лошат на 2-4 - й день після народження від каліцтва прямої кишки - відсутність анального отвору (Atresia ani). Виявилося, що всі жеребці і кобили, від яких народжувалися такі ненормальні лошата, походили від одного жеребця. Він був гетерозиготен по летального гену (LI). Спочатку цей жеребець при схрещуванні з нормальними кобилами (LL) дав потомство, за фенотипом нормальне, але за генотипом половина нащадків була благополучною (LL), a половина - гетерозиготною (LI), несучої рецесивний завдаток (0 летального гена. При родинному спарюванні гетерозиготних тварин (И х И) з'явилася частина лошат, гомозиготних по летального гену (II), з потворністю прямої кишки. Вони всі загинули. (Більш докладно про аномалії при летальних генах буде сказано у відповідній главі.)
