
14.Многоядерные арены
.pdf
Глава 14. МНОГОЯДЕРНЫЕ АРЕНЫ
=============================================================
Многоядерные (полиядерные, полициклические) арены – это арома-
тические соединения, молекулы которых содержат несколько бензольных колец. В зависимости от способа соединения последних многоядерные арены делят на две группы: соединения с изолированными бензольными кольцами и соединения с конденсированными бензольными кольцами.
=============================================================
14.1. МНОГОЯДЕРНЫЕ АРЕНЫ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ КОЛЬЦАМИ
=============================================================
К многоядерным аренам с изолированными бензольными кольцами относят углеводороды, содержащие два или более бензольных цикла, соединенных между собой либо σ-связью, либо через алифатическую углеродную цепь. Например: дифенил, дифенилметан, трифенилметан и др.
|
СН2 |
С |
|
|
Н |
дифенил (бифенил) |
дифенилметан |
трифенилметан |
14.1.1. ДИФЕНИЛ (БИФЕНИЛ)
Молекула дифенила содержит два бензольных кольца, соединенных σ- связью. Нумерацию углеродных атомов в каждом цикле проводят отдельно, начиная с атомов углерода, через которые осуществляется связь колец (они всегда имеют номера 1 и 1'). Замещенные производные дифенила получают названия с минимальным набором локантов; при этом цифра без штриха считается меньшей, чем цифра со штрихом. Например, 2,3,3',4',5'-
пентаметилдифенил, но не 2',3',3,4,5-пентаметилдифенил. Расположение заместителей в положениях 2,6,2',6' часто обозначают в названиях приставкой
орто-, в положениях 3,5,3',5' – мета- , в 4,4' – пара-.
3 |
|
2 |
2' |
3' |
|
СН3 |
|
|
СН3 |
|
СН3 |
|
|
м'- |
о'- |
|
о- |
м- |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 1' |
|
|
СН3 |
|
3' 2' |
|
|
2 |
3 |
|
п'- |
|
|
|
|
п- |
|
||||||||
4 |
|
|
|
4' |
|
|
|
1' |
|
|
|
|
|
С2Н5 |
|
|
|
|
С2Н5 |
|||||||||
|
|
|
|
|
4' |
|
|
1 |
|
4 |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
5' |
6' |
6 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
6 |
6' |
5' |
|
СН3 |
|
|
|
|
|
|
|
|
|
м'- о'- |
|
о- |
м- |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
дифенил (бифенил) |
2,3,3',4',5'-пентаметилдифенил |
|
4,4'-диэтилдифенил или |
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
п,п'-диэтилдифенил |
|
|||||||||
292
Дифенил – бесцветное кристаллическое вещество (т. пл. 70 °С, т. кип. 254°С) со слабым своеобразным запахом. Применяется в промышленности как высокотемпературный теплоноситель.
В молекуле дифенила вокруг σ-связи, соединяющей два цикла, возможно их свободное вращение. Оно также имеет место в молекулах тех производных дифенила, у которых в орто-положениях одного из бензольных колец отсутствуют заместители.
Если же в орто-положениях обоих бензольных колец содержатся объемные заместители, то из-за пространственных препятствий свободное вращение вокруг σ-связи между двумя циклами становится невозможным. Так, например, в молекуле 6,6'-динитродифеновой кислоты при попытке вращения нитрогруппа или карбоксильная группа в одном кольце не может пройти мимо нитрогруппы или карбоксильной группы в другом кольце из-за пространственных препятствий, создаваемых объѐмными карбоксильными и нитрогруппами. По этой же причине ароматические ядра в молекулах таких соединений не могут располагаться компланарно (в одной плоскости). Таким образом, возникают две энантиомерные (зеркальные) формы, ставшие стабильными из-за пространственных препятствий вращению вокруг простой связи, атропизомеры:
НООС |
NО2 |
О2N |
СООН |
|
|
||
О2N СООН |
НООС NО2 |
||
Рассмотренные изомеры похожи друг на друга как предмет и его зеркальное изображение и обладают оптической активностью, которая в данном случае обусловлена не наличием асимметрического атома углерода, а асимметрией молекулы в целом.
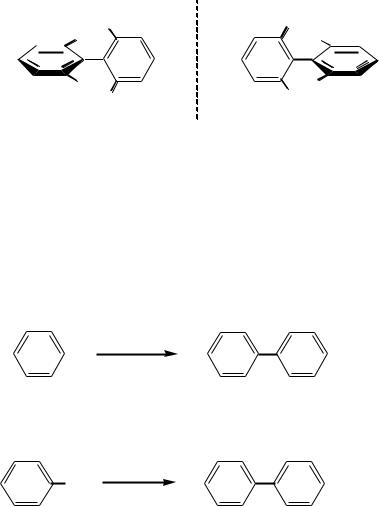
СПОСОБЫ ПОЛУЧЕНИЯ ДИФЕНИЛА
Дегидрирование бензола.
2 |
750-800 |
оС |
+ H2 |
|
|
||
|
бензол |
|
дифенил |
Из йодбензола при нагревании с порошком меди (реакция Ульмана).
2 |
J |
2 Cu |
|
200-250 oC |
|||
|
|
||
йодбензол |
|
дифенил |
+ 2 CuJ
293
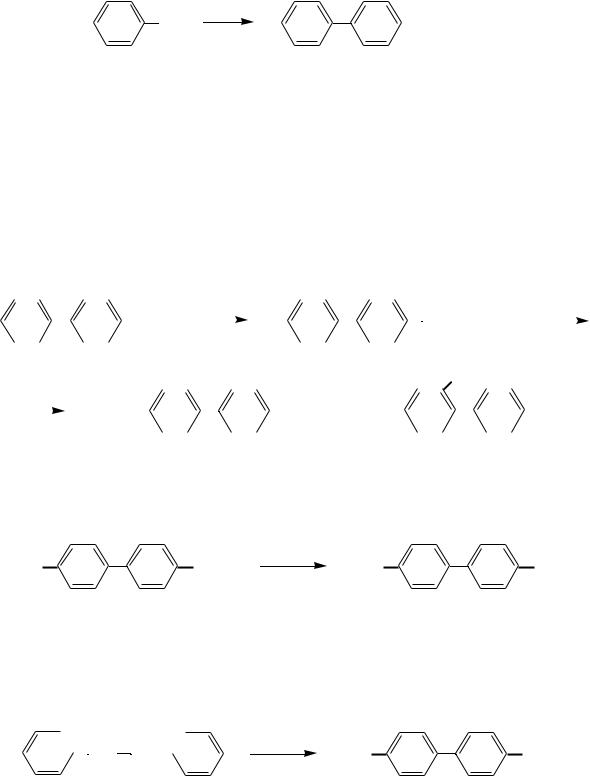
Из галогенбензолов под действием металлического натрия (реакция Фиттига):
2 |
Cl |
2 Na |
|
||
хлорбензол |
|
дифенил |
+ 2 NaCl
ХИМИЧЕСКИЕ СВОЙСТВА ДИФЕНИЛА
Химические свойства дифенила аналогичны свойствам моноядерных аренов. Фенильные группы проявляют по отношению друг к другу слабые электронодонорные свойства (заместители Ι рода). Поэтому в реакции электрофильного замещения (галогенирование, нитрование и др.) дифенил вступает несколько легче, чем бензол, образуя преимущественно продукты пара-, а также орто-замещения. В монозамещенных дифенилах при электрофильном замещении новый заместитель вступает в незамещенное ядро:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2HNO3, H SО |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2HNO , H SО |
|||||||||||||||
2 |
|
2 |
4 |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NО2 |
3 |
2 |
4 |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- 2H2О |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- 2H2О |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
дифенил |
|
|
|
|
|
|
|
|
|
4-нитродифенил |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NО2 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
О2N |
|
|
|
|
|
|
|
|
|
|
|
NО2 |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NО2 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4,4'-динитродифенил |
|
|
|
|
|
|
|
|
|
|
|
2,4'-динитродифенил |
|
|
|||||||||||||||||||||||||
Восстановлением 4,4'-динитродифенила может быть получен 4,4'- диаминодифенил (бензидин), исходное вещество при синтезе бензидиновых красителей:
|
|
восстан. |
|
О2N |
NО2 |
H2N |
NH2 |
|
4,4'-динитродифенил |
|
4,4'-диаминодифенил |
|
|
|
(бензидин) |
Впервые бензидин получен Н. Н. Зининым в 1845г. в результате перегруппировки гидразобензола в присутствии серной кислоты. Эта перегруппировка получила название бензидиновой:
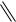
 NH NH
NH NH 

H2SО4 |
H2N |
NH2 |
|
t |
|||
|
|
гидразобензол |
бензидин |
Гидразобензол образуется в качестве одного из промежуточных продуктов при восстановлении нитробензола в щелочной среде.
Бензидиновые красители имеют строение, аналогичное строению азокрасителей. При диазотировании дисоли бензидина получается дисоль диазония с двумя диазогруппами, иногда называемая солью тетразония:
294

- |
+ |
+ |
- |
Cl H3N |
NH3 |
Cl |
|
соль бензидина
2HNO2 |
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
+ |
|
|
+ |
|
|||||||||||||||||||||
|
Cl |
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
Cl |
||||||||
- 4H2О |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
N |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
соль тетразония |
|
||||||||||||||
Полученную соль тетразония можно сочетать, подобно солям диазония, с разнообразными ароматическими аминами или фенолами, например:
- |
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Cl |
N |
|
|
|
|
|
N |
|
Cl + 2ArOH |
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|||||||||||||||||
|
|
|
|
- 2НCl |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
N |
|
N |
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
N |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ar |
|
|
|
|
|
|
|
|
|
|
|
Ar |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
соль тетразония |
|
|
|
|
|
|
Ar - ароматический остаток |
OH |
|
бензидиновый |
|
|
OH |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(бензола, нафталина и др.) |
|
|
|
|
|
краситель |
|
|
|
|
||||||||||
Среди бензидиновых красителей есть очень ценные, способные окрашивать хлопчатобумажное волокно непосредственно, без предварительной обработки протравами. Такие красители называются субстантивными (прямыми). Они обладают более глубокой окраской, чем моно-азокрасители. К бензидиновым красителям относится, например, индикатор конго красный.
14.1.2.ДИФЕНИЛМЕТАН
Вмолекуле дифенилметана два бензольных цикла связаны через метиленовую группу. Продукты замещения в бензольных ядрах дифенилметана называют аналогично замещѐнным дифенила. Номера 1 и 1' получают атомы углерода, связанные с метиленовой группой:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН3 |
|
|
|
|
СН3 |
|||
3 |
|
|
2 |
|
2' |
|
3' |
3 |
|
2 |
|
|
|
2' |
|
3' |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
1 |
1' |
|
|
|
|
|
|
1 |
|
|
1' |
|
|
|
|||||||||
4 |
|
|
|
|
|
СН2 |
|
|
|
|
|
4' |
4 |
|
|
|
|
|
СН2 |
|
|
|
4' |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
6' |
|
|
|
5' |
5 |
|
|
|
6 |
|
|
|
6' |
|
|
|
|||
5 |
6 |
|
|
|
|
|
|
|
|
|
|
5' |
|||||||||||||
|
|
|
|
дифенилметан |
|
|
2,3'-диметилдифенилметан |
||||||||||||||||||
Дифенилметан – бесцветное кристаллическое вещество (т. пл. 26-27 °С, т. кип. 261-262 °С) со слабым приятным запахом. Применяется как растворитель в лакокрасочной промышленности и в парфюмерной промышленности для отдушки мыла.
СПОСОБЫ ПОЛУЧЕНИЯ ДИФЕНИЛМЕТАНА
Алкилирование бензола по реакции Фриделя – Крафтса:
а) дихлорметаном:
H |
+ CH2Cl2 + H |
AlCl3 |
СН2 |
|
- 2HCl |
||||
|
|
|
||
бензол |
дихлорметан |
|
дифенилметан |
295

б) бензилхлоридом:
H + |
ClСН |
AlCl3 |
СН2 |
|
- HCl |
||||
|
2 |
|
||
бензол |
бензилхлорид |
|
дифенилметан |
ХИМИЧЕСКИЕ СВОЙСТВА ДИФЕНИЛМЕТАНА
Реакционная способность дифенилметана обусловлена наличием в его структуре бензольных циклов и активной метиленовой группы.
Реакции с участием бензольных колец – электрофильное замещение с образованием 4,4’-дизамещенных и 2,4,2’,4’-тетразамещенных продуктов:
|
|
CH2 |
|
|
|
|
|
|
|
|
2HNO3, H2SO4 |
|
О2N |
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
NО2 |
||||||||||
|
|
|
|
|
|
- 2H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дифенилметан |
|
|
|
|
|
|
|
|
|
|
|
4,4'-динитродифенилметан |
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NО2 |
NО2 |
|
|
||||||||||||||||||||||
|
|
|
2HNO3, H2SO4 |
О2N |
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
NО2 |
|
|
||||||||||||||||
|
|
|
|
|
- 2H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2,4,2',4'-тетранитродифенилметан
Реакции по метиленовой группе. Электроноакцепторное влияние фенильных радикалов делает подвижными атомы водорода метиленовой группы, поэтому она легко окисляется, а при галогенировании атомы водорода замещаются галогеном:
|
|
O |
|
|
2 |
[ O ] |
C |
|
|
- H2O |
|
|||
|
|
|||
|
|
бензофенон |
|
|
CH2 |
|
Br |
|
|
|
|
|
||
дифенилметан |
Br2 |
CH |
Br2 |
|
- HBr |
- HBr |
|||
|
||||
|
|
|||
Br
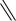
 C
C
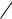
Br
дифенилбромметан |
дифенилдибромметан |
Бензофенон применяется в парфюмерии.
Широкий интерес в качестве исходного вещества для производства ряда красителей представляет аминопроизводное бензофенона, так называемый кетон Михлера. Получают его конденсацией фосгена с N,N-диметиланилином. При обработке аммиаком в присутствии хлорида цинка кетон Михлера превращается в жѐлтый краситель аурамин:
296
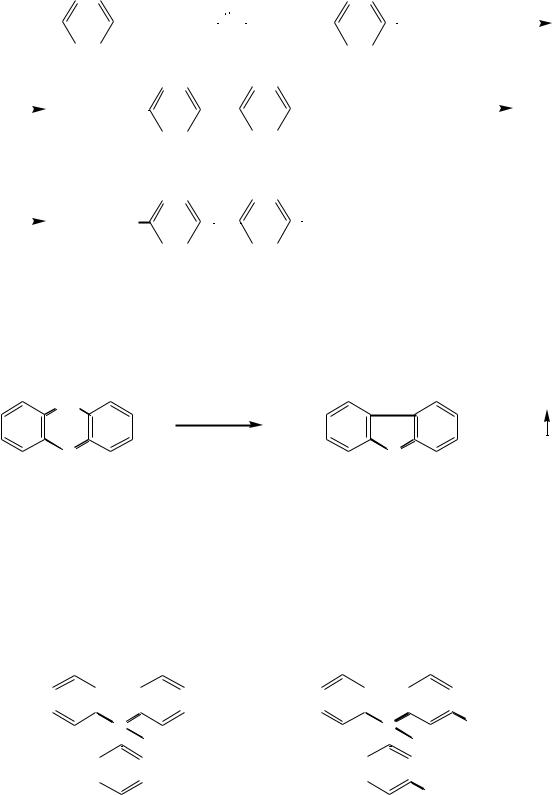
(CH3)2N |
|
|
|
|
|
|
|
|
H + |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
Cl |
|
C |
|
Cl + |
|
H |
|
|
|
|
|
N(CH3)2 |
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- 2HCl |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N,N-диметиланилин |
|
|
|
|
|
фосген |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
(CH3)2N |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
N(CH3)2 |
|
|
|
NH3, ZnCl2 |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H2O |
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4,4'-бис(диметиламин)бензофенон |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кетон Михлера |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
(CH3)2N |
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
N(CH3)2 |
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
аурамин (желтый краситель)
Специфическая реакция дифенилметана. При пропускании паров дифенилметана через раскалѐнные докрасна трубки образуется флуорен, соединение с тремя ядрами – двумя бензольными и одним циклопентадиеновым:
H H |
раскаленные |
|
трубки |
||
|
||
|
+ H2 |
|
CH2 |
CH2 |
|
дифенилметан |
флуорен |
14.1.3. ТРИФЕНИЛМЕТАН
Молекула трифенилметана содержит три бензольных цикла, связанных через метиновую группу (СН). Номенклатура производных трифенилметана аналогична номенклатуре производных дифенилметана. Номера 1, 1' и 1'' получают атомы углерода, связанные с метиновой группой:
.
|
3'' |
|
|
|
|
|
|
5 |
|
|
3'' |
|
|
|
|
|
|
|
5 |
|
|
|
|||||
4'' |
|
|
2'' |
6 |
|
|
4 |
4'' |
|
|
2'' |
6 |
|
|
|
|
|
|
|
4 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
5'' |
|
|
1'' |
1 |
|
|
3 |
5'' |
|
|
1'' |
1 |
|
|
|
|
|
|
|
3 |
СН3 |
||||||
6'' |
|
|
|
|
C |
|
|
|
|
|
|
|
C |
|
|
|
|
Н 2 |
|||||||||
|
|
|
|
|
|
Н 2 |
|
6'' |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
1' |
|
|
|
|
|
|
|
1' |
|
|
|
|
|
|
|||||||
|
6' |
|
|
|
|
|
2' |
|
|
6' |
|
|
|
|
|
|
|
2' |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3' |
|
|
|
||
|
5' |
|
|
|
|
3' |
|
|
5' |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН3 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
4' |
|
|
|
|
|
|
|
|
|
4' |
|
|
|
|
|
|
|||||
|
трифенилметан |
|
3,3'-диметилтрифенилметан |
||||||||||||||||||||||||
Трифенилметан – бесцветное кристаллическое вещество (т. пл. 92 °С), основа трифенилметановых красителей, а также некоторых лекарственных препаратов.
297
СПОСОБЫ ПОЛУЧЕНИЯ ТРИФЕНИЛМЕТАНА И ЕГО ПРОИЗВОДНЫХ
Получение трифенилметана
Алкилирование бензола по Фриделю–Крафтсу а) хлороформом:
3 |
H |
+ |
CHCl3 |
AlCl3 |
C |
|
- 3HCl |
||||||
|
|
|
|
Н |
||
бензол |
|
|
хлороформ |
|
трифенилметан |
б) хлористым бензилиденом:
|
|
CHCl 2 |
|
|
2 |
+ |
AlCl3 |
C |
|
- 2HCl |
||||
|
|
Н |
||
бензол |
|
хлористый |
трифенилметан |
|
|
|
бензилиден |
|
Получение производных трифенилметана
Конденсация ароматических альдегидов с ароматическими аминами:
C |
O |
|
NH2 |
H2N |
NH2 |
H |
|
|
|
||
|
+ |
2 |
|
|
C |
|
|
- H2О |
Н |
||
|
|
|
|
|
|
|
|
|
H |
|
|
бензальдегид |
|
анилин |
|
4,4'-диаминотрифенилметан |
|
Конденсация ароматических альдегидов с фенолами: |
|||||
C |
O |
|
ОН |
НО |
ОН |
H |
|
|
|
||
|
+ |
2 |
|
|
C |
|
|
- H2О |
Н |
||
|
|
|
|
|
|
|
|
|
H |
|
|
бензальдегид |
|
фенол |
|
4,4'-диокситрифенилметан |
|
298
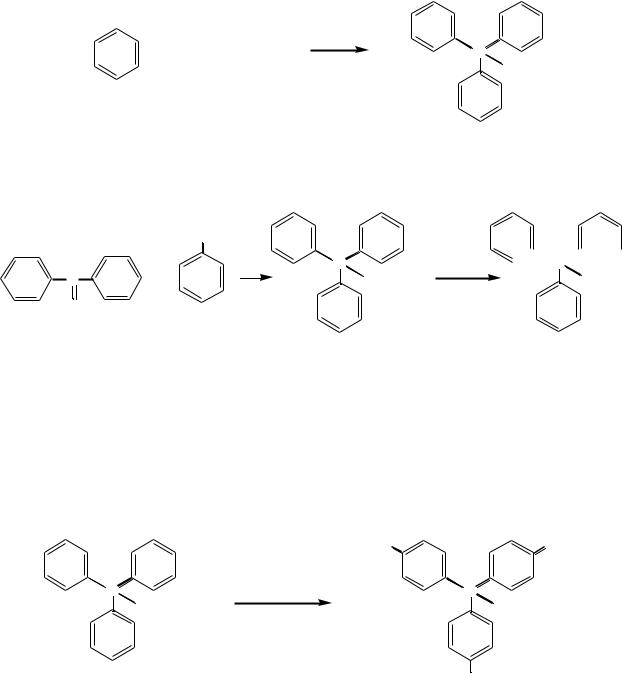
Алкилирование бензола четыреххлористым углеродом:
|
+ |
CCl4 |
AlCl3 |
C |
3 |
- 3HCl |
|||
|
|
|
Сl |
|
|
|
|
|
|
бензол |
|
четырѐххлористый |
|
|
|
|
углерод |
|
трифенилхлорметан |
Из ароматических кетонов магнийорганическим синтезом:
|
|
MgBr |
C |
+ |
C |
OMgBr |
HOH
- MgOHBr

 C
C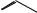

ОН
O
бензофенон |
фенилмагнийбромид |
трифенилметанол |
|
|
(трифенилкарбинол) |
ХИМИЧЕСКИЕ СВОЙСТВА ТРИФЕНИЛМЕТАНА
Химические свойства трифенилметана обусловлены наличием в его молекуле бензольных циклов и подвижного водорода метиновой группы.
Реакции электрофильного замещения с участием бензольных циклов
идут, главным образом, в пара-положения:
|
О2N |
NО2 |
C |
3HNO3, H2SO4 |
C |
Н |
- 3H2O |
Н |
|
|
|
|
|
NО2 |
трифенилметан |
|
4,4',4''-тринитротрифенилметан |
Реакции с участием метиновой группы (СН). Водород метиновой группы трифенилметана обладает высокой подвижностью и способен замещаться на металл или галоген. По метиновой группе трифенилметан легко окисляется, превращаясь в трифенилметанол. Причиной подвижности «метинного» водорода в различных реакциях является большая устойчивость образующихся при разрыве связи С–Н трифенилметильных радикалов (С6Н5)3С∙ или ионов (С6Н5)3С+, (С6Н5)3С-. Устойчивость этих частиц обусловлена участием бензольных циклов в делокализации неспаренного электрона (в радикале), положительного или отрицательного заряда (в ионах) за счѐт сопряжения.
299
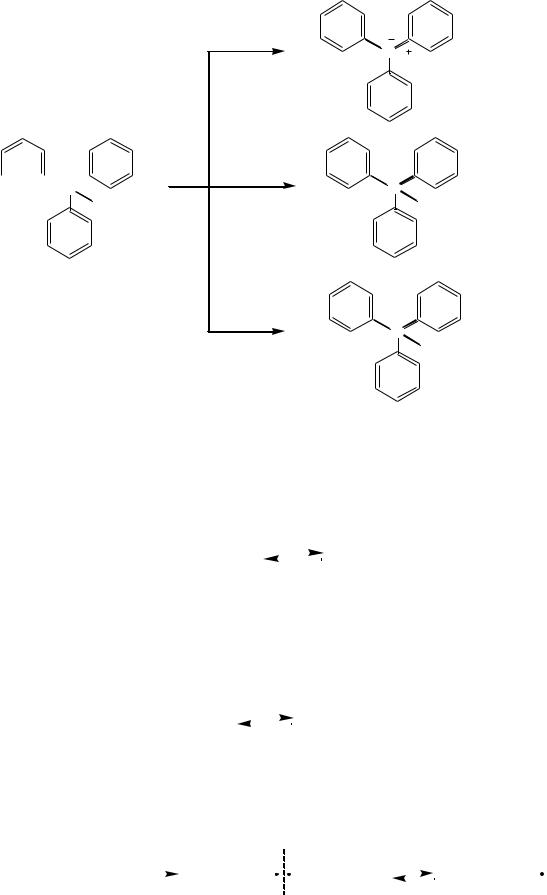
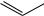
 C
C
H
NaNH2 |
C |
|
+ NH3 |
|
Na |
||
|
|
|
трифенилметилнатрий
Cl2 |
C |
+ HCl |
|
Сl
трифенилхлорметан
[ O ] |
C |
|
OH
трифенилметанол
Химические свойства производных трифенилхлорметана также в значительной степени обусловлены непрочностью связи трифенилметильной группы с другими атомами и группами атомов. Так, например, трифенилметанол под действием HCl легко образует трифенилхлорметан. Последний, гидролизуясь, превращается в исходный спирт:
(C6H5)3С |
|
OH |
|
|
HCl |
|
(C6H5)3С |
|
|
Cl |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||||
|
|
|
H2O |
|
||||||
трифенилметанол |
|
|
трифенилхлорметан |
|||||||
|
|
|
||||||||
Под действием концентрированной серной кислоты происходит ионизация трифенилметанола (прямая реакция) с образованием окрашенного раствора, в котором присутствует носитель цветности катион (С6Н5)3С+. При разбавлении водой окрашенный раствор обесцвечивается (обратная реакция), так как образуется бесцветный трифенилметанол:
|
|
|
|
|
|
|
|
|
|
(C6H5)3С |
|
OH + H2SO4 |
|
|
|
(C6H5)3С |
+ HSO4 + H2O |
||
|
|
|
|||||||
|
|
|
|
||||||
бесцветный раствор |
|
|
|
окрашенный раствор |
|||||
Явление изменения окраски химических соединений при их ионизации называется галохромия (от греч. «гал» - соль, «хромос» - окраска).
При обработке трифенилхлорметана цинком, натрием или серебром образуется свободный трифенилметильный радикал:
2 (C6H5)3C |
|
Cl |
Zn |
(C6H5)3С C(C6H5)3 |
|
|
|
2 (C6H5)3C |
|
|
|
|
|
||||
|
- ZnCl2 |
|
|
|||||
|
|
|
|
|||||
трифенилхлорметан |
|
|
|
радикал трифенилметил |
||||
|
|
|
|
|||||
Свободный трифенилметильный радикал обладает значительной устойчивостью благодаря делокализации неспаренного электрона по всем
300

бензольным циклам и является первым из радикалов, полученных в свободном виде (1900г. М. Гомберг (амер.).
Трифенилметильный радикал, катион и анион ярко окрашены: (C6H5)3C+ - трифенилметил-катион – красно-оранжевый, (C6H5)3C¯ - трифенилметил-анион – красный,
(C6H5)3C∙ - трифенилметил-радикал – желтый.
Окраска этих частиц обусловлена наличием в их структуре достаточно длинной цепи сопряжения (хромофора), включающей три бензольных цикла.
Теория цветности рассматривает зависимость окраски веществ от строения их молекул. Цвет вещества – это результат избирательного поглощения веществом части лучей видимого света. Человеческий глаз воспринимает вещества окрашенными, если они поглощают свет в видимой области спектра (400 – 760 нм). При этом глаз видит предмет окрашенным в цвет, дополнительный к поглощаемому:
Длина |
Поглощенный цвет |
Цвет окраски предмета |
волны, нм |
|
|
400 – 435 |
Фиолетовый |
Зеленовато-желтый |
435 – 480 |
Синий |
Желтый |
480 – 490 |
Зеленовато-синий |
Оранжевый |
490 – 500 |
Синевато-зеленый |
Красный |
500 – 560 |
Зеленый |
Пурпурный |
560 – 580 |
Желтовато-зеленый |
Фиолетовый |
580 – 595 |
Желтый |
Синий |
595 – 605 |
Оранжевый |
Зеленовато-синий |
605 – 730 |
Красный |
Синевато-зеленый |
730 – 760 |
Пурпурный |
Зеленый |
(батохромный сдвиг) |
(гипсохромный сдвиг) |
Углубление цвета |
Повышение цвета |
Яркие окраски обусловлены поглощением света в узком диапазоне волн, неяркие (коричневый, бордо, хаки) – в широком, серая и черная – поглощением практически во всей видимой области спектра. Непрозрачное тело, отражающее все лучи видимого спектра, бесцветно.
Изменение цвета, приводящее к поглощению более длинных волн, называют углублением цвета или батохромным сдвигом; изменение цвета, приводящее к поглощению более коротких волн, называют повышением цвета или гипсохромным сдвигом.
При действии света на молекулу окрашенного вещества π-электроны поглощают кванты лучистой энергии и переходят на более высокие энергетические уровни. Наиболее подвижными в органической молекуле являются π-электроны, образующие длинные цепи сопряжения. Поэтому все органические красители в качестве обязательного структурного фрагмента содержат длинные цепи сопряжения. Согласно хромофорной теории О.Витта (1876г.) структурные фрагменты молекулы, отвечающие за поглощение излучения в видимой области спектра, т. е. за окраску вещества, носят
301
