
- •Содержание
- •Введение
- •Темы практических занятий
- •Общие требования к решению задач
- •Практическое занятие 1 Параметры состояния рабочего тела. Уравнения идеального газа. Определение теплоемкости идеальных газов
- •Практическое занятие 2 Исследование термодинамических процессов идеального газа
- •Практическое занятие 3 Водяной пар. Параметры состояния. Исследованию процессов водяного пара
- •Практическое занятие 4 Истечение газов и паров. Определение скорости истечения и расхода рабочего тела
- •Практическое занятие 5 Расчет циклов двигателей внутреннего сгорания (двс). Расчет циклов газотурбинных установок (гту)
- •Практическое занятие 6 Расчет циклов паротурбинных установок (пту).
- •Список использованной литературы
- •Приложениия
- •Типовые задачи к контрольным работам
Практическое занятие 2 Исследование термодинамических процессов идеального газа
Рекомендуемая литература
Нащокин В.В. Техническая термодинамика и теплопередача. – М.: Высшая школа, 1980. – с. 45-63.
Рабинович О.М. Сборник задач по технической термодинамике – М.: Машиностроение, 1969. – с. 57-117.
Теплотехника/ М.М. Хазен, Г.А. Матвеев, М.Е. Грицевский, Ф.П.Казакевич/ Под ред. Г.А. Матвеева. – М.: Высшая школа, 1981. –с. 16-39.
Юдаев Б.Н. Техническая термодинамика. Теплопередача. – М.: Высшая школа, 1988. – с. 37-56.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАНИЯ
Сформулируйте первый закон термодинамики и напишите его аналитическое выражение.
От каких параметров состояния зависит внутренняя энергия газов?
Чем являются теплота и работа - функцией процесса или состояния? Почему?
Что такое энтальпия и энтропия? В чем заключается их физический смысл?
Как определить приращение энтропии идеального газа в зависимости от основных термических параметров состояния?
Как определить работу и теплоту процесса на
 -
и
-
и - диаграммах?
- диаграммах?В каком случае теплота, работа, изменение внутренней энергии и энтропии считаются положительными? отрицательными?
В каком термодинамическом процессе вся теплота идет на совершение работы?
В каком термодинамическом процессе работа не совершается?
В каком термодинамическом процессе работа совершается за счет изменения внутренней энергии?
В каком термодинамическом процессе показатель политропы равен нулю?
Примеры решения задач
Задача
2.1. Воздух
массой 10 кг расширяется изотермически
при
![]() оС
от начального давления
оС
от начального давления
![]() =
800 кПа до конечного объема
=
800 кПа до конечного объема![]() = 5 м3.
Определить начальный объем, конечное
давление, работу расширения, теплоту
процесса, изменение энтропии, энтальпии
и внутренней энергии.
= 5 м3.
Определить начальный объем, конечное
давление, работу расширения, теплоту
процесса, изменение энтропии, энтальпии
и внутренней энергии.
Решение.
Начальный
объем определяем из уравнения состояния
для
![]() кг газа:
кг газа:
![]() м3.
м3.
Конечное давление определяем из соотношения параметров в изотермическом процессе:
![]() , (11)
, (11)
тогда:
![]() кПа
кПа
Работу расширения в изотермическом процессе определяем по формуле:
![]() . (12)
. (12)
После подстановки данных имеем:
![]() кДж.
кДж.
В изотермическом
процессе вся теплота расходуется на
совершение работы, поэтому в данном
случае
![]() кДж.
кДж.
Изменение энтропии в изотермическом процессе находим по формуле:
![]() , (13)
, (13)
тогда
![]() кДж/кг·К.
кДж/кг·К.
Энтальпия и
внутренняя энергия идеального газа в
изотермическом процессе не изменяются,
таким образом,
![]() и
и
![]() .
.
Ответ:
![]() м3;
м3;
![]() кПа;
кПа;
![]() кДж;
кДж;
![]() кДж/кг·К;
кДж/кг·К;![]() и
и
![]() .
.
Задача 2.2. Сухой воздух массой 1 кг совершает прямой термодинамический цикл, состоящий из четырех последовательных термодинамических процессов.
Заданные
параметры для воздуха:
![]() МПа,
МПа,
![]() 300
К,
300
К,
![]() МПа,
МПа,
![]() =
273 К. Процессы: 1-2 -
=
273 К. Процессы: 1-2 -
![]() ;
2-3-
;
2-3-![]() ;
3-4 -
;
3-4 -![]() ;
4-1 -
;
4-1 -![]() .
.
Требуется:
1. Рассчитать давление Р, удельный объем v, температуру воздуха Т для основных точек цикла.
2.
Для каждого из процессов определить
значения показателей политропы n,
теплоемкости c, вычислить изменение
внутренней энергии
![]() ,
энтальпии
,
энтальпии
![]() ,
энтропии
,
энтропии
![]() ,
теплоту процесса q,
работу процесса
,
теплоту процесса q,
работу процесса
![]() ,
располагаемую работу
,
располагаемую работу
![]() .
.
3.
Определить суммарные количества
подведенной q1
и отведенной q2
теплоты, работу цикла
![]() ц,
термический КПД цикла t.
ц,
термический КПД цикла t.
4. Построить цикл в vP - и sT - координатах.
Принять
газовую постоянную
![]() 287,3
Дж/(кгК), теплоемкость при постоянном
давлении
287,3
Дж/(кгК), теплоемкость при постоянном
давлении
![]() =1,025
кДж/(кгК), что соответствует свойствам
сухого воздуха при Т=273 К.
=1,025
кДж/(кгК), что соответствует свойствам
сухого воздуха при Т=273 К.
Решение.
1. Определим параметры в характерных точках.
Точка
1.
![]() К.
К.
Точка 2. Процесс 1-2 – адиабатный
Показатель
адиабаты:![]() ;
;
![]() кДж/(кгК)
кДж/(кгК)
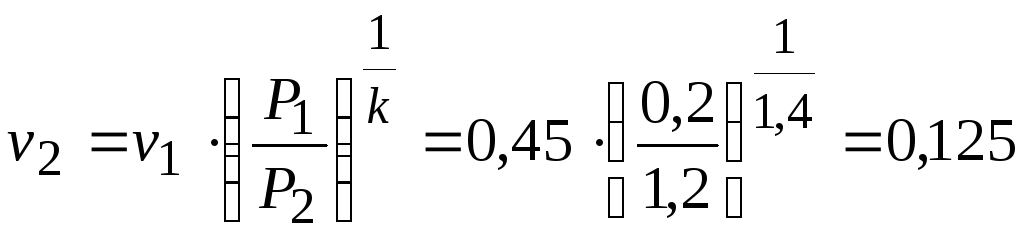 м3/кг.
м3/кг.
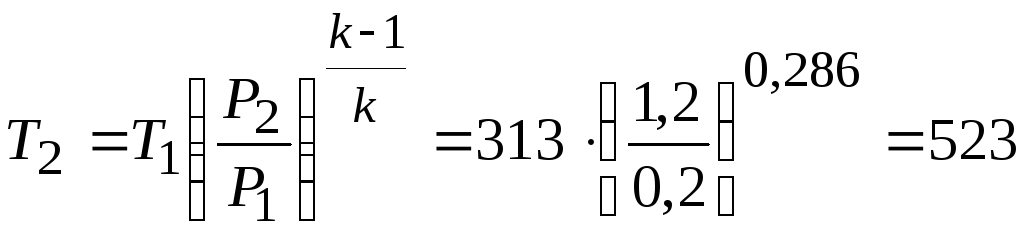 К.
К.
Точка
3. Процесс 2-3 – изохорный =>
![]() =0,125
м3/кг.
=0,125
м3/кг.
![]() МПа.
МПа.
Точка
4.
 м3/кг.
м3/кг.
 К
К
Таблица 2.1.
Результаты вычислений
|
Термические параметры |
Точка цикла | |||
|
1 |
2 |
3 |
4 | |
|
Р, МПа |
0,2 |
1,2 |
1,3 |
0,2 |
|
v, м3/кг |
0,45 |
0,125 |
0,125 |
0,5 |
|
Т, К |
313 |
523 |
573 |
335 |
2. Рассчитаем параметры процессов.
Процесс
1-2
– адиабатный:
![]() .
.
Показатель политропы рассчитаем по формуле:
 .
(14)
.
(14)
Для данного
процесса:
 .
.
Теплоемкость:
![]() . (15)
. (15)
В адиабатном
процессе теплоемкость равна нулю, т.к.
![]() :
:
![]() .
.
Изохорная
теплоемкость:
![]() кДж/кг·К
кДж/кг·К
Изменение внутренней энергии и энтальпии:
![]() кДж/кг;
кДж/кг;
![]() =215,25
кДж/кг.
=215,25
кДж/кг.
Изменение энтропии определяется по формуле:
![]() . (16)
. (16)
Т.к.
в адиабатном процессе
![]() ,
то и
,
то и
![]() =0.
=0.
В адиабатном процессе работа совершается за счет изменения внутренней энергии:
![]() =-
=-![]() , (17)
, (17)
тогда:
![]() =-
=-![]() =-154,98
кДж/кг.
=-154,98
кДж/кг.
Располагаемая
работа в адиабатном процессе в
![]() раз больше работы изменения объема:
раз больше работы изменения объема:
![]() =
=
![]()
![]() =1,4·
=1,4·![]() кДж/кг.
кДж/кг.
Процесс
2-3 – изохорный:
![]() .
.
В изохорном процессе показатель политропы равен бесконечности:
 .
.
![]() =
0,738 кДж/(кг·К).
=
0,738 кДж/(кг·К).
Изменение внутренней энергии и энтальпии:
![]() кДж/кг;
кДж/кг;
![]() кДж/кг.
кДж/кг.
Изменение энтропии в изохорном процессе определяется по формуле:
![]() , (18)
, (18)
Тогда в данном
случае:
![]() кДж/кг·К.
кДж/кг·К.
В изохорном процессе
вся теплота расходуется на изменение
внутренней энергии:
![]() 36,9
кДж/кг.
36,9
кДж/кг.
Работа в изохорном
процессе равна нулю за счет того объем
остается постоянным:
 .
.
Располагаемая
работа:
![]() кДж/кг
кДж/кг
Процесс
3-4 - адиабатный:
![]() .
.
 ;
;
![]() =0.
=0.
![]() кДж/кг;
кДж/кг;
![]() =-243,95
кДж/кг;
=-243,95
кДж/кг;
![]() =-
=-![]() =175,6кДж/кг;
=175,6кДж/кг;![]() =
=![]()
![]() =1,4·
=1,4·![]() кДж/кг;
кДж/кг;![]() =0
=0
Процесс
4-1
– изобарный:
![]() ,
т.е.
,
т.е.![]() .
.
Таким образом,
![]()
Теплоемкость
процесса:
![]() кДж/(кг·К).
кДж/(кг·К).
![]() кДж/кг;
кДж/кг;
![]() кДж/кг;
кДж/кг;
![]() =
=![]() кДж/(кг·К);
кДж/(кг·К);
![]() =
=![]() -22,55
кДж/кг;
-22,55
кДж/кг;
![]()
![]() кДж/кг;
кДж/кг;
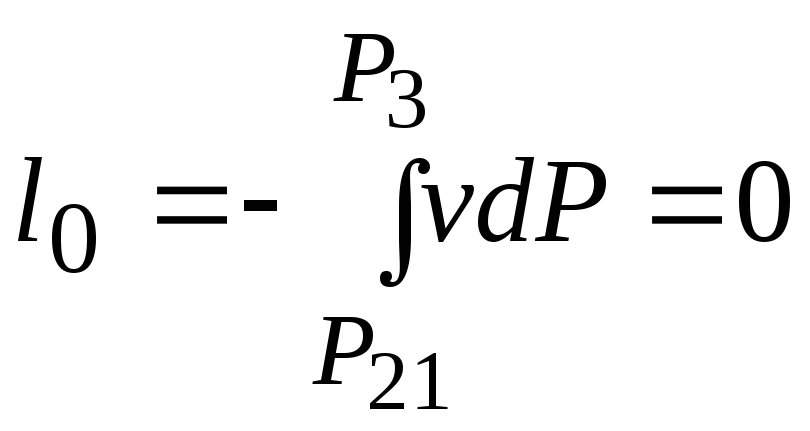 .
.
3. Определим
суммарные количества подведенной q1
и отведенной q2
теплоты, работу цикла
![]() ,
термический КПД цикла t.
,
термический КПД цикла t.
Подведенная
теплота:
![]() кДж/кг.
кДж/кг.
Отведенная теплота:
![]() кДж/кг.
кДж/кг.
Работа
цикла:![]() =36,9-22,55=14,35
кДж/кг.
=36,9-22,55=14,35
кДж/кг.
Термический КПД
цикла
![]() :
:![]()
4. Для построения
цикла в координатах
![]() необходимо определить значение энтропии
необходимо определить значение энтропии![]() (Дж/кг∙К) для каждой характерной точки
цикла по формуле:
(Дж/кг∙К) для каждой характерной точки
цикла по формуле:
![]() .
(19)
.
(19)
Далее получаем:
![]() кДж/(кг·К);
кДж/(кг·К);
![]() кДж/(кг·К);
кДж/(кг·К);
![]() кДж/(кг·К);
кДж/(кг·К);
![]() кДж/(кг·К).
кДж/(кг·К).
Вычислим значения изменения энтропии в термодинамическом цикле:
![]() кДж/(кг·К);
кДж/(кг·К);
![]() кДж/(кг·К);
кДж/(кг·К);
![]() кДж/(кг·К);
кДж/(кг·К);
![]() кДж/(кг·К).
кДж/(кг·К).
Вычисленные значения изменения энтропии совпадают со значениями, полученными для процессов цикла через основные термодинамические параметры.
Таблица 2
Результаты вычислений энтропии в точках цикла
|
|
Точка 1 |
Точка 2 |
Точка 3 |
Точка 4 |
|
|
313 |
523 |
573 |
335 |
|
|
- 0,06 |
- 0,06 |
0,01 |
0,01 |
Цикл в
![]() - координатах строим, используя результаты
вычислений п.1 (таблица 2.1.):
- координатах строим, используя результаты
вычислений п.1 (таблица 2.1.):

Рис. 2. Цикл в vP-координатах

Рис. 3. Цикл в sT – диаграмме
задачи для самостоятельного решения
Задача 2.3. Какое
количество теплоты необходимо подвести
к воздуху в закрытом сосуде объемом
![]() м3,
если начальная температура t1
=100 оС
, давление
м3,
если начальная температура t1
=100 оС
, давление
![]() =
300 кПа, а конечная температура t2
=500 оС?
Определить также массу воздуха и конечное
давление. Зависимость теплоемкости от
температуры считать нелинейной.
=
300 кПа, а конечная температура t2
=500 оС?
Определить также массу воздуха и конечное
давление. Зависимость теплоемкости от
температуры считать нелинейной.
Ответ:
![]() = 1,4 кг;
= 1,4 кг;![]() =
412 кДж;
=
412 кДж;![]() = 623 кПа.
= 623 кПа.
Задача 2.4. В
изохорном процессе температура окиси
углерода массой m
= 2,1 кг
с
начальным давлением p1
=
0,12 МПа изменяется от t1=
25оС
до
t2=63оС.
Определить параметры состояния рабочего
тела в точках 1 и 2, а также теплоту,
энтальпию и изменение внутреней энергии
1 кг окиси углерода в процессе. Принять
ср
= 1,0464
кДж/кг∙К,
![]() =296,8
кДж/кг∙К. Изобразить процесс в vр-
и
sT-диаграммах.
=296,8
кДж/кг∙К. Изобразить процесс в vр-
и
sT-диаграммах.
Ответ:
![]() К;
К;![]() м3/кг;
м3/кг;
![]() К;
К;
![]() 0,735
м3/кг;
0,735
м3/кг;
![]() ;
;![]() ;
;![]() кДж/кг.
кДж/кг.
Задача 2.5.
Воздух массой m
= 1,9 кг с начальным давлением p1
=0,22
МПа адиабатно расширяется. При этом
его температура изменяется от t1
=65 оС
до t2
=21оС.
Определить параметры состояния рабочего
тела в точках 1 и 2, а также теплоту,
энтальпию и изменение внутреней энергии
1 кг азота в процессе. Принять
ср
= 1,0121 кДж/кг∙К,
![]() =287
кДж/кг∙К.
=287
кДж/кг∙К.
Представить процесс в vр- и sT-диаграммах.
Ответ:
![]() К;
К;
![]() м3/кг;
м3/кг;
![]() К;
К;
![]() 0,54
м3/кг;
0,54
м3/кг;
![]() ;
;![]() ;
;![]() кДж/кг;
кДж/кг;![]() =
- 44,53 кДж/кг.
=
- 44,53 кДж/кг.
