
- •III. Задачи Кинематика поступательного и вращательного движения материальной точки (все)
- •Динамика материальной точки. Законы сохранение импульса и энергии. Работа. Мощность (все)
- •Момент инерции. Твердое тело в механике
- •Механические колебания и волны
- •Молекулярно-кинетическая теория идеальных газов
- •Основы термодинамики. Адиабатический процесс. Циклические процессы
Молекулярно-кинетическая теория идеальных газов
1.При нагревании газа на ΔТ=3000С при постоянном давлении объем его увеличился в два раза. В каком интервале температур происходило нагревание?
2.Определите плотность смеси 64 г кислорода и 56 г азота, если давление смешанного газа 200 кПа, а температура 27°С.
3.Газовая смесь, состоящая из кислорода и азота, находится в баллоне под давлениемP = 1 МПа. Определить парциальное давлениеP1/ кислорода иP2/азота, если массовая доля ω1кислорода в смеси равна 0,2.Мк= 32·10-3кг/моль, Маз= 28·10-3кг/моль.
4.В сосуде находится азот при нормальных условиях. Какое давление установится в сосуде после нагревания газа до температуры 1500°С, при которой 30% молекул распадаются на атомы.
5.Чему равны удельные теплоемкостиСVиСРнекоторого двухатомного газа, если плотность этого газа приt= 27ºС иp= 105Па равна 1,4 кг/м3?
6. Разность удельных теплоемкостей СР-СV некоторого двухатомного газа равна 260 Дж/(кг.К). Найти молярную массу М газа и его удельные теплоемкости СР и СV.
Основы термодинамики. Адиабатический процесс. Циклические процессы
+1.Кислород, занимающий объемV1= 5 л при давлениир1= 1 МПа, изотермически сжимается в 3 раза. Определить конечное давлениер2и работуА, совершенную газом.
2. Газ массой m = 10 г расширяется изотермически от объёма V1 до объёма V2 = 2V1. Чему равна наиболее вероятная скорость молекул газа, если работа расширения газа А = 900 Дж.
+3. Некоторый газ массой 5 г расширяется изотермически от объемаV1до объемаV2=2V1. Работа расширения равна 1 кДж. Определить среднюю квадратичную скорость молекул.
+4.Некоторый газ массой 1 кг находится при температуреТ=300 К и под давлением р1=0,5 МПа. В результате изотермического сжатия давление газа увеличилось в 2 раза. Работа, затраченная на сжатиеА=-432 кДж. Определить: 1) какой это газ; 2) первоначальный удельный объем газа.
+5.Для изобарического нагревания ν = 5 молей идеального газа от температурыТ1= 273 К доТ2= 373 К потребовалось сообщить газу теплотуQ = 14,54 кДж. Определить число степеней свободы молекул газа.
+6.Водород массойm = 10 г нагрели на ΔT = 200 К, причем газу было передано количество теплотыQ = 40 кДж. Найти изменение Δuвнутренней энергии газа и совершенную им работуА.М = 2·10-3кг/моль.
+7.Азот массой 2 кг охлаждают при постоянном давлении от 400 до 300 К. Определить изменение внутренней энергии, внешнюю работу и количество выделенной теплоты.
+8.Азот массойm= 280 г расширяется изобарно при давленииP= 1 МПа. Определить работу расширения и конечный объём газа, если на расширение затрачена теплотаQ= 5 кДж, а начальная температура азотаТ1= 290 К.
+9.При изобарном нагревании некоторого идеального газа в количествеν = 2 моль на ΔT = 90 К ему было сообщено количество теплоты 5,25 кДж. Определить работу, совершённую газом, изменение внутренней энергии и коэффициент Пуассона газа.
+10.Для изобарного нагревания ν молей идеального газа от температурыТ1до температурыТ2потребовалось сообщить ему количество теплоты, равноеQ. Определить показатель адиабаты газа.
+11.20 г водорода, имеющего температуру 300 К, сначала расширили адиабатно, увеличив объем в 5 раз, а затем сжали изотермически до первоначального объема. Найти температуру после адиабатного расширения и работу, совершенную в итоге газом.
+12.1 моль воздуха, имевший температуру 0°С и находившийся под давлением 5 кПа, адиабатически расширился до давления 1 кПа. На сколько градусов понизилась температура воздуха в результате расширения? Какую работу совершил газ при расширении?
+13. При адиабатном сжатии кислорода массойm = 20 г его внутренняя энергия увеличилась на ΔU = 8 кДж и температура повысилась доТ2= 900 К. Найти, на сколько повысилась температура ΔTи каково конечное давление газаP2, если начальное давлениеР1= 200 кПа.
+14.Азот массойm= 1 кг занимает при температуреТ1= 300 К объёмV1= 0,5 м3. В результате адиабатического сжатия давление газа увеличилось в 3 раза. Определить конечный объём газа, его конечную температуру и изменение внутренней энергии.
+15. Азот массой m = 2 г, имеющий температуру T1 = 300 К, был адиабатно сжат так, что его объем уменьшился в n = 10 раз. Определить конечную температуру T2 газа и работу А сжатия.
+16. Азот массойm = 1 кг занимает при температуреT1= 300 К объемV1= 0,5 м3. В результате адиабатического сжатия давление газа увеличилось в 3 раза. Определить: 1) конечный объем газа; 2) его конечную температуру; 3) изменение внутренней энергии газа.М = 28·10-3кг/моль.
+17. Кислород массойm = 64 г, занимающий объемV1= 0,5 л при давлениир1= 1 МПа, расширяется вn = 3 раза. Определите конечное давление и работу, совершенную газом, если процесс адиабатический.
+18. При адиабатном расширении 64 г кислорода, вначале находившемся при нормальных условиях, его объем увеличился в 3 раза. Найти изменение внутренней энергии газа и совершенную им работу.
+19.В цилиндре под поршнем находится
водород массой 20 г при температуре .
Водород начал расширяться адиабатно,
увеличив свой объем в 5 раз, а затем
был сжат изотермически, причем объем
газа уменьшился в 5 раз. Найти
температуру
.
Водород начал расширяться адиабатно,
увеличив свой объем в 5 раз, а затем
был сжат изотермически, причем объем
газа уменьшился в 5 раз. Найти
температуру в конце адиабатного расширения и работу
в конце адиабатного расширения и работу ,
совершенную газом.
,
совершенную газом.
+20.Над молем идеального газа совершается замкнутый цикл,

состоящий из двух изохор и двух изобар.
Температуры в точках 1 и 3 равны Т1иТ2. Определить работу, совершенную газом за цикл, если известно, что точки 2 и 4 лежат на одной изотерме.
+21. Один моль одноатомного газа совершает цикл, состоящий из двух изохор и двух изобар. При этом максимальный объем в 3 раза больше минимального, а максимальное давление в 2 раза больше минимального. Определить КПД цикла.
+22.Кислород совершает цикл, состоящий из двух изохор и двух изобар, причем наибольшее давление в 2 раза больше наименьшего, а наибольший объем в 4 раза больше наименьшего. Определить термический КПД цикла.
23. Многоатомный идеальный газ совершает цикл Карно, при этом в процессе адиабатического расширения объем газа увеличивается в n = 4 раза. Определить термический к.п.д. цикла.
+24.Кислород, занимающий объёмV1 = 5 л при давленииp1 = 1 МПа, расширяется вn = 3 раза. Определите конечное давление и работу, совершённую газом, если процесс изотермический. Чему равно изменение энтропии газа, если его масса 64 г?
+25.64 г кислорода изобарно нагрели так, чтоего объем увеличилсяв 2 раза, а затемизохорно охладилитак, что давление упалов 2 раза. Определить приращение энтропии газа.
+26.Азот, занимавший объёмV1 = 10 л под давлениемP1 = 0,2 МПа, изотермически расширился до объёмаV2 = 28 л. Определить работуА расширения газа, количество теплотыQ, полученное газом и изменение энтропии одного моля газа.
+27.Кислород массойm= 10 г нагревают от температурыt1= 50°С до температурыt2= 150°С. Найти приращение ΔSэнтропии, если нагревание происходит: а) изохорически; б) изобарически.
+28. Водород массой m = 100 г был изобарно нагрет так, что его объем увеличился в 3 раза, затем этот водород был изохорно охлажден так, что его давление уменьшилось 3 раза. Найти изменение энтропии в ходе указанных процессов.
+29. Как изменится энтропия 2 г водорода, занимающего объем 40 л при температуре 270 К, если давление увеличить вдвое при постоянной температуре, а затем изохорно повысить температуру до 320К? Молярная масса водорода равна 0,002 кг/моль.
+30.1,7 г гелия адиабатически расширили до втрое большего объема, а затем изобарно сжали до первоначального объема. Чему равно изменение энтропии газа за весь процесс?
+31. Идеальный одноатомный газ (ν = 2 моль) сначала изобарно нагревали, так что объем газа увеличился вn1= 2 раза, а затем изохорно охладили, так что давление его уменьшилось вn2 = 2 раза. Определить приращение энтропии в ходе указанных процессов.
+32. Давлениеvмолей газа в некотором процессе изменяется прямо пропорционально его объему. Найти изменение энтропии газа при увеличении его объема вnраз, если его показатель адиабаты равен γ.
+33. Процесс расширения двух молей аргона происходит так, что давление газа увеличивается прямо пропорционально его объему. Найти изменение энтропии газа при увеличении его объема в два раза.
34.Найти изменение энтропии ΔSпри переходе массыm= 8 г кислорода от объемаV1= 10 л к объемуV2= 40 л при температуреТ= 353 К.
+35.Найти изменение энтропии ΔSпри переходе массыm = 8 г кислорода от объёмаV1 = 10 л при температуреt1=80ºC к объёмуV2 = 40 л при температуреt2 = 300ºC.
+36.Чему равно изменение энтропии 8 г кислорода при расширении от объема 10 л до объема 40 л, если начальная температура равна 30°С, а конечная – 300°С?
+37. Найти изменение энтропии ΔSпри превращении массыm = 10 г льда (t = – 20ºС) в пар (t = 100ºС).Сл= 2100 Дж/кг·К, λ = 335 кДж/кг,Св = 4200 Дж/кг·К, τ = 2,3 МДж/кг.
+38.Лед массой 2 кг, находящийся при температуре -130С, нагрели до 00С и расплавили. Определить изменение энтропии. (λ=3,35.105Дж/кг, Сльда=2,1.103Дж/(кг.К))
+39.Лед массой при температуре
при температуре был превращен в воду той же температуры
с помощью пара, имеющего температуру
был превращен в воду той же температуры
с помощью пара, имеющего температуру .
Определить массу
.
Определить массу израсходованного пара. Каково изменение
израсходованного пара. Каково изменение энтропии системы лед-пар?
энтропии системы лед-пар? ,
, ,
,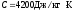 .
.
+40.Кусочек меди массы 300 г,
имеющий температуру ,
поместили в калориметр, в котором
находится 100 г воды при
,
поместили в калориметр, в котором
находится 100 г воды при .
Найти изменение энтропии системы за
время выравнивания температуры.
Теплоемкостью калориметра можно
пренебречь.
.
Найти изменение энтропии системы за
время выравнивания температуры.
Теплоемкостью калориметра можно
пренебречь. ,
, .
.
+41. Смешали воду массойm1= 5 кг при температуреТ1= 280 К с водойm2= 8кг при температуреТ2= 350 К. найти: 1) температуруТсмеси; 2) изменение энтропии ΔS, произошедшее при смешивании. Удельная теплоемкость водыс= 4200 Дж/кг.
+42.Определить удельную теплоемкостьСРсмеси кислорода и гелия, если количество вещества ν1первого компонента равно 2 моль, а количество вещества ν2второго равно 4 моль.
+43.Чему равна удельная теплоемкость при постоянном объеме смеси из 3-х молей неона и2-х молей гелия, молярные массы которых равны соответственно 20 г/моль и 4 г/моль?
+44.Вычислить удельную теплоёмкостьСVсмеси неона и водорода. Массовые доли газов соответственно равныw1 = 0,8 иw2 = 0,2.М1= 20·10-3кг/моль,М2= 2·10-3кг/моль.
+45. В баллоне находятся гелий и азот. Определить удельную теплоемкость сV смеси этих газов, если массовые доли гелия и азота одинаковы и равны 0,5. Молярные массы гелия и азота равны соответственно 4 г/моль и 28 г/моль
+46. Газовая смесь состоит из азота массой 2 кг и аргона массой 1 кг. Принимая газы за идеальные, определить удельные теплоемкостиСV и СРгазовой смеси. Мазота = 28·10-3кг/моль, Маргона = 40·10-3кг/моль.
+47.Вычислить постоянную Пуассона для газовой смеси, состоящей из двух молей кислорода и трех молейуглекислого газа.М1 = 32·10-3кг/моль, М2 = 44·10-3кг/моль.
+48.Определите коэффициент Пуассона γ для смеси газов, содержащей гелий массойm1 = 8 г иводород массой m2 = 2 г.М1 = 4·10-3кг/моль, М2 = 2·10-3кг/моль.
+49. Чему равен коэффициент Пуассона для газовой смеси, состоящей из 7 г азота и 20 г гелия. Маз = 28·10-3кг/моль, Мг = 4·10-3кг/моль.
