
- •Лекция 8. Химические свойства алканов. Ациклические непредельные углеводороды.
- •1. Химические свойства.
- •1.2. Сульфонохлорирование.
- •1.3. Нитрование.
- •1.4. Окисление алканов.
- •1.5. Вторичная переработка нефти. Крекинг.
- •2. Алкены.
- •Номенклатура.
- •3. Изомерия структурная и геометрическая.
- •Е, z-номенклатура.
1.2. Сульфонохлорирование.
Сульфонохлорирование алканов при УФ-облучении, при комнатной температуре, протекает как цепной радикальный процесс (реакция Руффа). В качестве продуктов образуются хлорангидриды алкансульфоновых кислот. Особенностью реакции является следующее: при наличии в молекуле углеводорода первичных, вторичных и третичных атомов углерода замещению не подвергаются атомы водорода при третичном атоме углерода:

1.3. Нитрование.
Атомы водорода в углеводородах могут быть замещены нитрогруппой -NO2. Соответствующая реакция называется реакцией нитрования. Протекает реакция также по цепному радикальному механизму. Нитрование алканов впервые провел М.И.Коновалов действием 10-20% азотной кислоты при 120-1500С. (реакция Коновалова, 1888г.):

Данная реакция протекает в жидкой (по Коновалову) при 100-150 0С, и в газовой фазе при 250-5000С.
В реакцию жидкофазного нитрования вступают все углеводороды, однако продукты образуются с низкими выходами. Наиболее высокие выхода получаются для алканов, имеющих третичные углеродные атомы.
В газовой фазе реакция нитрования сопровождается окислением углеводородов и расщеплением углерод-углеродных связей. Поэтому в продуктах наряду с основными содержатся низкомолекулярные нитроалканы. Так, в случае нитрования пропана образуется 34 % 1-нитропропана СН3-СН2-СН2-NO2, 32 % 2-нитропропана СН3-СНNO2-СН3, 26 % нитроэтана СН3-СН2-NO2, и 8 % нитрометана СН3-NO2.
1.4. Окисление алканов.
Наиболее распространенным процессом в химии алканов является их окисление. Как известно алканы составляют основные виды энергоносителей: бензин, дизельное топливо, авиационный керосин, топочный мазут. Сгорание алканов происходит до углекисло газа и воды. Но двуокись углерода и вода это конечные продукты реакции со сложным механизмом, протекающим через стадии образования радикалов и их распада.
В процессе окисления предельных углеводородов в качестве промежуточных продуктов образуются органические гидропероксиды:
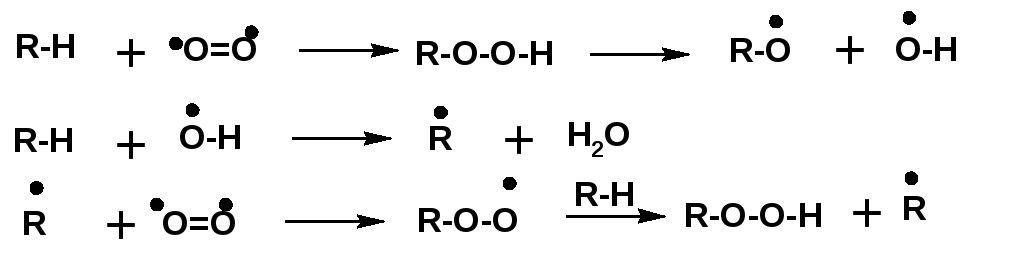
Образующиеся в результате распада гидропероксида радикалы вступают в две реакции.
1. Отрывают радикалы водорода от других молекул алканов и образуют спирты.
2. Распадаются по β-связи (β по отношению к атому углерода с неспаренным электроном) с образованием альдегидов и кетонов.
Радикалы третичных гидропероксидов распадаются с образованием третичного спирта или кетона, по схеме:

Радикалы вторичных гидропероксидов в зависимости от температуры распадаются по двум схемам. При низких температурах образуются, преимущественно, спирты и кетоны:

При высоких температурах преимущественно образуются спирты и альдегиды:

Радикалы первичных гидропероксидов распадаются с образованием первичного спирта, альдегида и формальдегида:

1.5. Вторичная переработка нефти. Крекинг.
Значительный рост потребления легких фракций, особенно бензина, все более жесткие требования к их качеству, потребности органического синтеза вызвали необходимость вторичной переработки нефти. Она связана, во-первых, с получением более легких углеводородов из тяжелых, во-вторых, с изменением структуры углеродного скелета. К вторичным процессам переработки нефти относятся различные типы крекинга, алкилирования, изомеризации, пиролиз, коксование и т.д.
В результате вторичных процессов переработки нефти наряду с моторными топливами получают исходные вещества для производства важнейших продуктов – синтетических каучуков, синтетических волокон, пластических масс, синтетических моющих средств, поверхностно-активных веществ, пластификаторов, красителей, присадок и др.
При температурах 300-7000С предельные углеводороды образуют сложную смесь предельных, непредельных и ароматических углеводородов. Основными процессами при крекинге являются дегидрогенизация и разрыв углеродной цепи. Эти процессы протекают через стадию образования свободных радикалов.
Свободные радикалы, образующиеся в процессе крекинга, способны к следующим превращениям:


При температуре выше 1000 0С протекает распад углеводородов до углерода (сажа) и водорода. Если при этих условиях время контакта с высокой температурой резко умень-шить, то происходит образование ацетилена. В настоящее время ацетилен для органичес-кого синтеза получают в плазматронах при 50000С со временем контакта 10-4сек.
