
Ароматика Галогенпроизводные
.pdf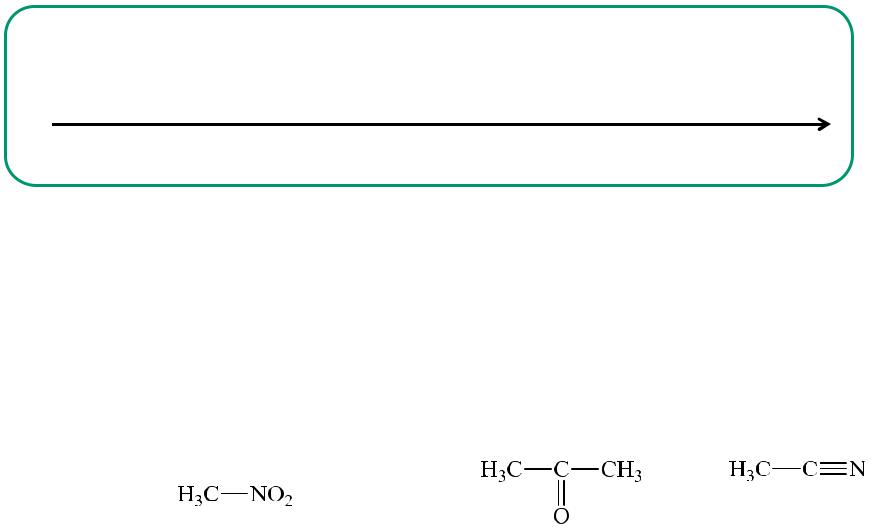
Факторы влияющие на протекание реакции SN по бимолекулярному механизму SN2
1. Строение галогеналкана
|
|
|
CH3 |
|
||
|
|
|
|
|
|
|
CH3CH2-X; |
CH3-CH-CH3; |
CH3-C-CH3 |
|
|||
|
|
|
|
|
|
|
|
X |
X |
|
|||
Уменьшается реакционная способность в SN2-реакциях |
|
|||||
2. Нуклеофильность реагента |
|
|
|
|
||
H2O > RO- > HO- > R2NH > NH3 > H2O > F-; |
|
|||||
HO- > H2O; |
H2N- > NH3; RO- |
> ROH; |
|
|||
I- |
> Br- > Cl- > F- |
|
|
|
|
|
3. Природа растворителя |
|
|
|
|
|
|
Диполярные апротонные растворители: |
ацетон, |
ацетонитрил, |
||||
нитрометан
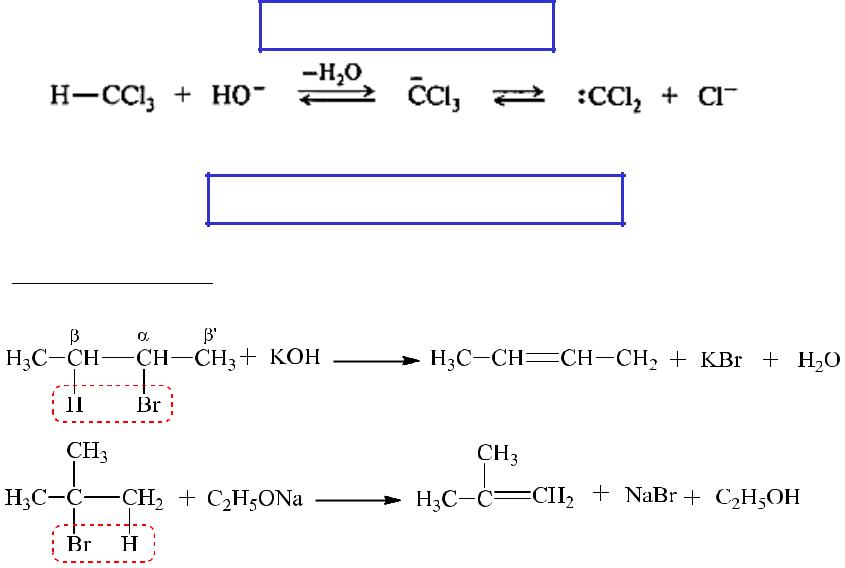
II. Реакции элиминирования (отщепления) Е (реакции дегидрогалогенирования)
α - элиминирование
хлороформ |
дихлоркарбен |
β - элиминирование
Протон водорода отщепляется от β-углеродного атома по правилу Зайцева
спирт
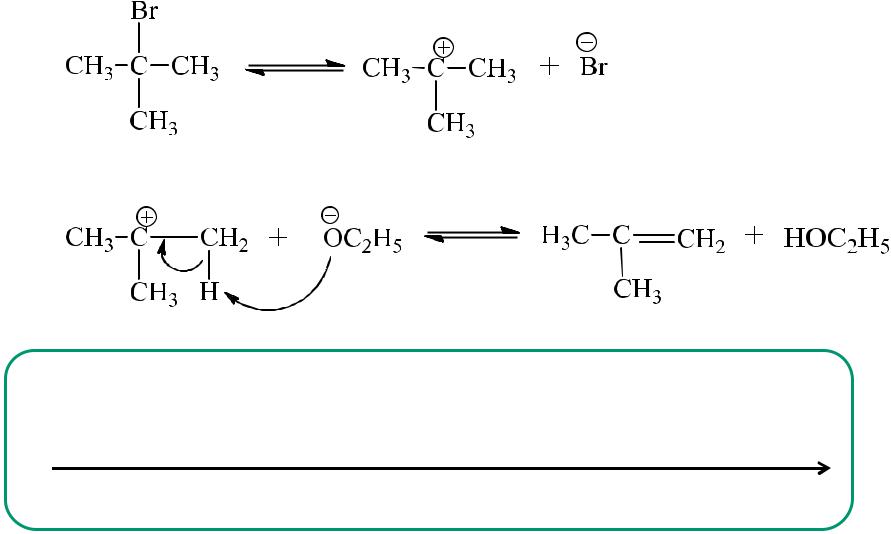
Механизм мономолекулярного элиминирования Е1
V=k[RHlg]
1. медленно
2. |
быстро |
|
|
|
CH3 |
||
|
|
|
|
|
CH3CH2-X; CH3-CH-CH3; |
CH3-C-CH3 |
|||
|
|
|
|
|
X |
X |
|||
Увеличивается реакционная способность в Е1-реакциях

Механизм бимолекулярного элиминирования Е2
V=k[RHlg][:B-]
медленно |
|
|
|
|
|
|
|
|
|
|
|
|
быстро |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||
|
|
|
|
|
CH3CH2-X; CH3-CH-CH3; |
CH3-C-CH3 |
|||
|
|
|
|
|
X |
X |
|||
Уменьшается реакционная способность в Е2-реакциях
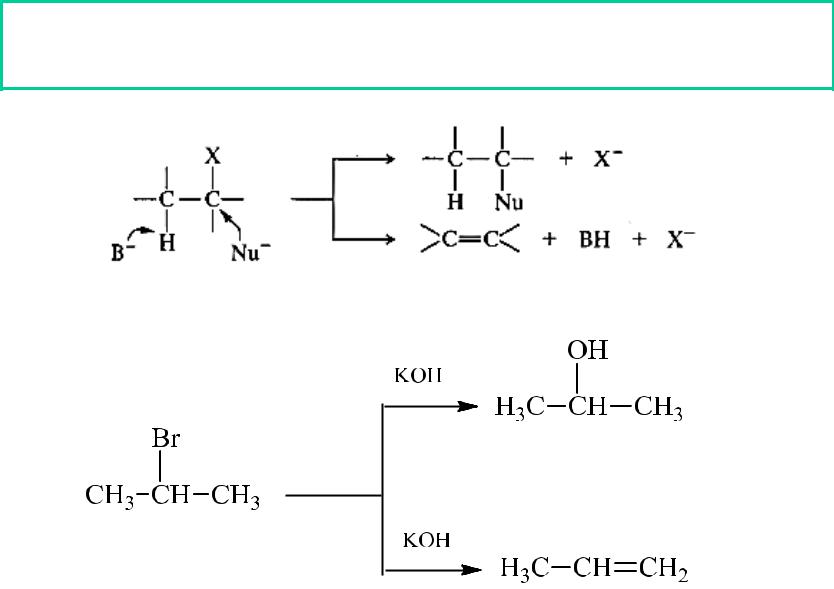
Конкурентность реакций нуклеофильного замещения и элиминирования
вода
спирт
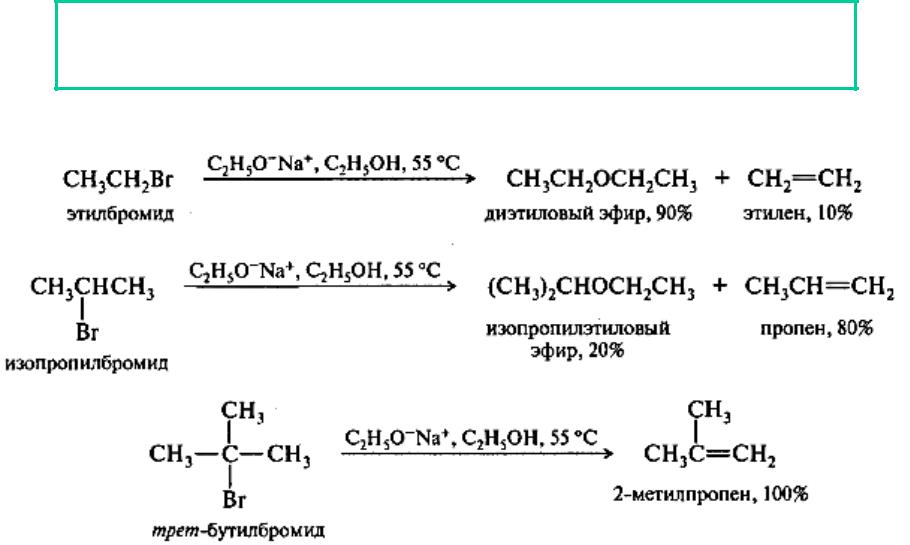
Влияние строения галогеналканов на конкурентность реакций нуклеофильного замещения и элиминирования
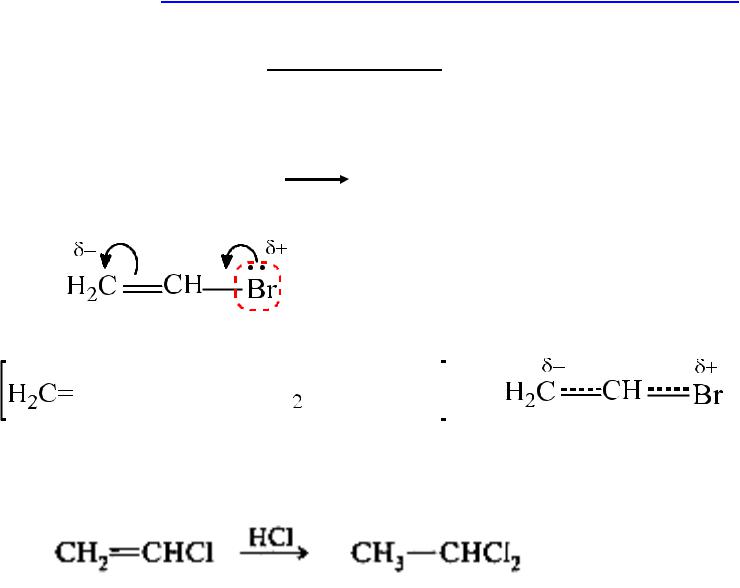
Непредельные галогенпроизводные
1.CH2=CH-Cl – винильные
а) HC≡CH + HCl H2C=CH-Cl
б) H2CСl-CH2-Cl KOH H2C=CH-Cl+KCl+H2O
сп.р-р
+М
p, - сопряжение
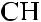



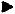
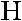



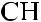
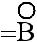

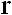
 ≡
≡
резонансные (граничные) |
гибридная структура |
|
|
структуры |
|
хлорэтилен |
1,1-дихлорэтан |
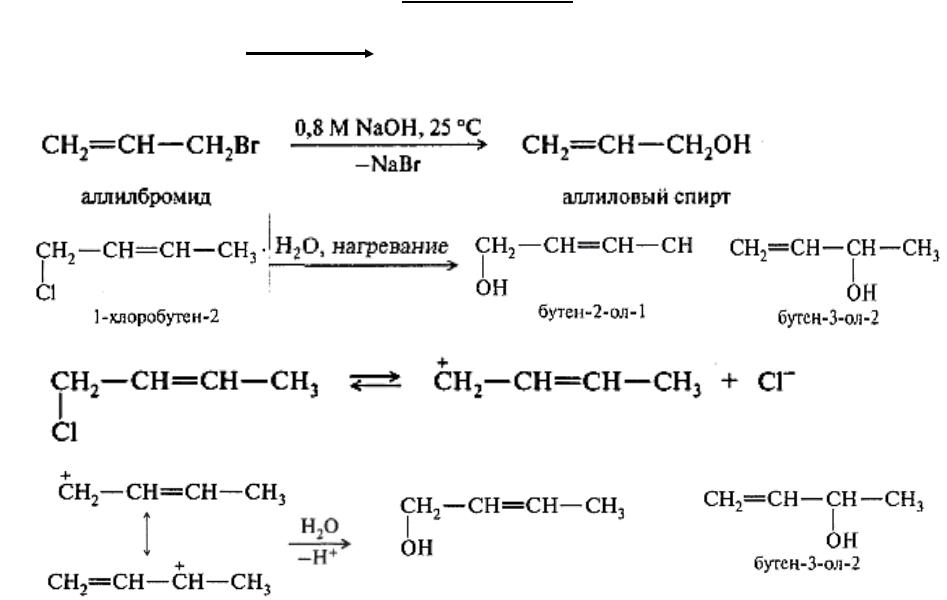
2. CH2=CH-CH2-Cl – аллильные
Cl2 |
|
H3C CH=CH2 400° |
Cl–CH2–CH=CH2 |
+
+
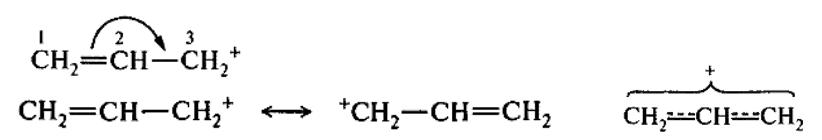
Аллилный карбкатион
|
≡ |
|
резонансные (граничные) |
гибридная структура |
|
структуры |
||
|

|
Cl2 |
CH2Cl-CH CH2 |
|
||
CH3-CH CH2+HCl h , 400° |
||
SN1
H2C CH-CH2
-J
|
медл |
|
+ - |
+ |
|
|
|
|
|
|
Cl |
|
H2C CH-CH2 |
+ |
|
|
|||||
|
|
|
||||||||
|
|
|
РС I |
|
|
|
|
NaOH |
||
|
|
|
|
|
|
|
||||
|
|
|
|
+Cl |
H2C=CH-CH2OH |
|||||
|
|
|
+ |
|
||||||
|
|
|
|
|
|
|
|
|
аллиловый |
|
|
|
H C-CH |
|
CH |
|
|
||||
|
|
|
||||||||
|
|
2 |
РС II |
2 |
|
|
|
|
спирт |
|
H2C  CH
CH  CH2+Сl
CH2+Сl
+
H2C=CH-CH2Cl 5% NaHCO3H2C CH-CH2OH
H2O
HC |
|
C-CH CH2+HCl |
H2C |
|
C-CH CH2 |
||
|
|||||||
|
|
||||||
|
|
||||||
|
|
|
|
|
|||
|
|
|
|
|
Cl |
хлоропрен |
|
