
Лекции «Молекулярная Фотоника»
Лекция 7. Окислительно-восстановительные фотохимические реакции (реакции фотопереноса электрона)
1. Реакция … перенос электрона от молекулы восстановителя (донор е-) к молекуле окислителя (акцептор е-) - окислительно-восстановительная (ОВР).
 е-
е-
D + A
D+.
+ A-.
+ A
D+.
+ A-.
2. Окислительно-восстановительной фотореакция … перенос электрона поисходит с участием ЭВ состояния партнера (реагент)
е-
 hD
hD

 D*
+ A (1)
D*
+ A (1)
 е-
D+.
+ A-.
е-
D+.
+ A-.
 hA
hA
 A*
+ D
(2)
A*
+ D
(2)
Реакция (1) – фотоокисление (окисление возбужденной молекулы)
Реакция (2) – фотовосстановление (восстановление возбужденной молекулы).
Проблемы, требующие ответа:
-
Почему протекает фотоОВР. Движущая сила фотореакции.
-
Как быстро протекает фотоОВР. Факторы, определяющие скорость реакции.
-
Влияние среды на протекание фотоОВР.
-
Эффективность фотоОВР.
Почему протекает фотоОВР. Движущая сила
фотореакции.
-
Качественное описание. Рассматривается схема
граничных МО


E






















D* A D+. A-.
-
Количественное описание. (газовая фаза)
 D+.
+ е-
+ А
D+.
+ е-
+ А


- ПИ + h
Dg* + Ag - СЭ


 - ПИ
- ПИ
(Gg*)


h D+.g + A-.g
Gg

Dg + Ag
Темновая реакция не протекает, т.к. Gg > 0
Фотореакция протекает, т.к. (Gg*) < 0
(Gg*) = (ПИ - h -СЭ) < 0
Раствор
Выражение для Gs* через E1/2(D/D+.) и E1/2(А/А-.) имеет вид
![]()
фотореакция протекает при Gs* < 0, что и является условием протекания фотоОВР.
Как быстро протекает фотоОВР.
Факторы, определяющие скорость реакции.
Бимолекулярная реакцию фотопереноса электрона
D* + A D+. + A-., kнабл
Реакция … через промежуточные стадии
k12 k23 k34




 D*
+ A D*...A
D+....A-.
D+.
+ A-.
D*
+ A D*...A
D+....A-.
D+.
+ A-.

 k21
k32
k21
k32
h k30

 D
+ A D...A
D
+ A D...A
kнабл выражается через ki (метод стационарных концентраций)
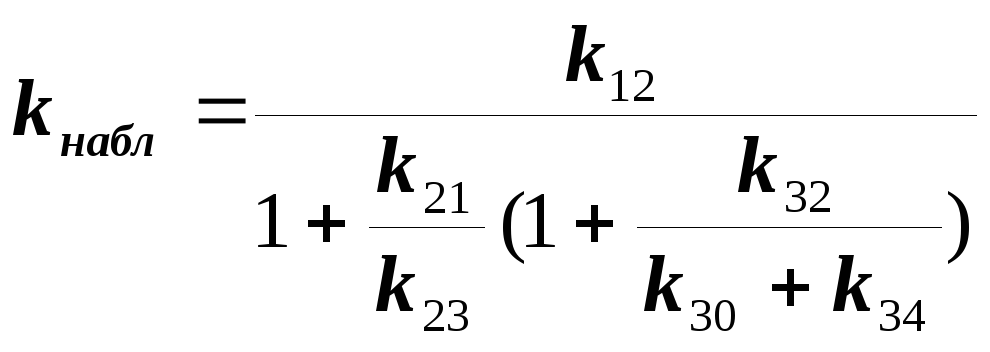 (1)
(1)
Случай, когда ИРП (D+....A-.) практически не претерпевает обратной реакции, т.е. (k30 + k34)>>k32.
(1) имеет вид

Частные случаи
1) k23 >> k21 (случай высокой скорости переноса электрона), тогда
kнабл k12
2) k23 << k21 (случай низкой скорости переноса электрона), тогда
kнабл K12 k23
