
- •Лекция 7.1.
- •1.Химия как наука.
- •1.Химия как наука.
- •1.Химия как наука.
- •1.Химия как наука.
- •1.Химия как наука.
- •2. Эволюция химических знаний
- •2. Эволюция химических знаний
- •2. Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний
- •2.Эволюция химических знаний

Лекция 7.1.
Химические концепции естествознания
1.Химия как наука.
2.Эволюция химических знаний.
04.07.19 |
1 |

1.Химия как наука.
Важнейшим разделом современного естествознания является химия – наука о веществах и превращениях их друг в друга.
Химия, как известно, изучает
химическую форму движения.
Признаком химической формы движения является превращение одних веществ в другие в результате перераспределения связей атомов и перестройки электронных оболочек атомов.
04.07.19 |
2 |

1.Химия как наука.
Вещество – это каждый отдельный вид материи, обладающий при определенных условиях постоянными физическими свойствами, такими как удельный вес, температура плавления, температура кипения, растворимость, теплоемкость, теплопроводность и многое другое.
Только чистое вещество обладает определенными, постоянными свойствами.
Вбольшинстве случаев природные вещества –
смеси.
Абсолютно чистые вещества – не известны.
04.07.19 |
3 |

1.Химия как наука.
Каждое чистое вещество состоит из одного или нескольких химических элементов.
Элемент -совокупность атомов с одинаковым зарядом ядра.
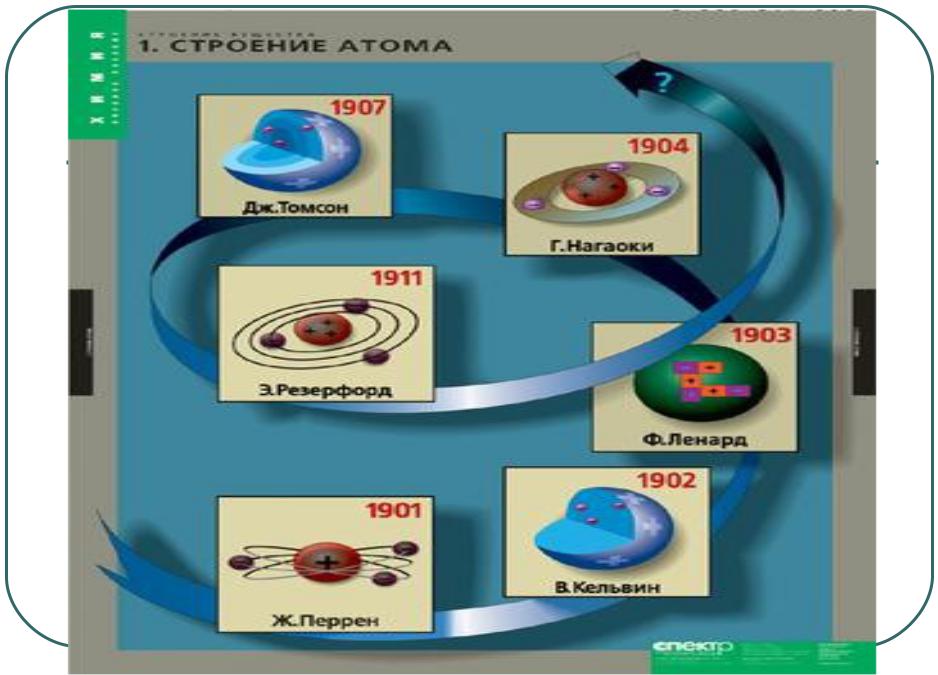
Атом представляет собой электронейтральную частицу, состоящую из положительно заряженного атомного ядра (протоны), отрицательно заряженных электронов и нейтральных нейтронов.
04.07.19 |
4 |

04.07.19 |
6 |
04.07.19 |
7 |

1.Химия как наука.
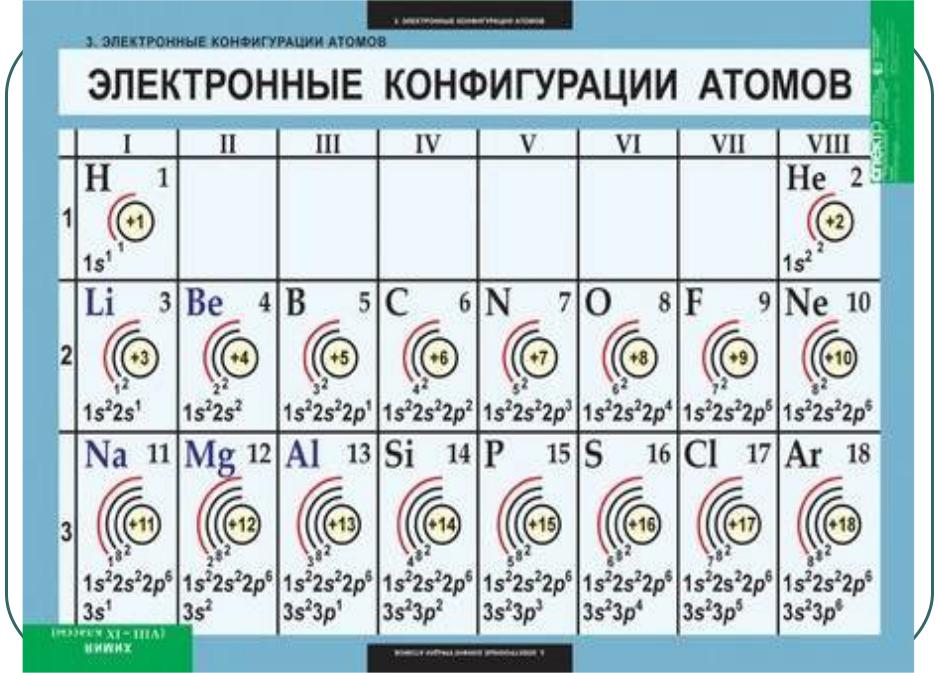
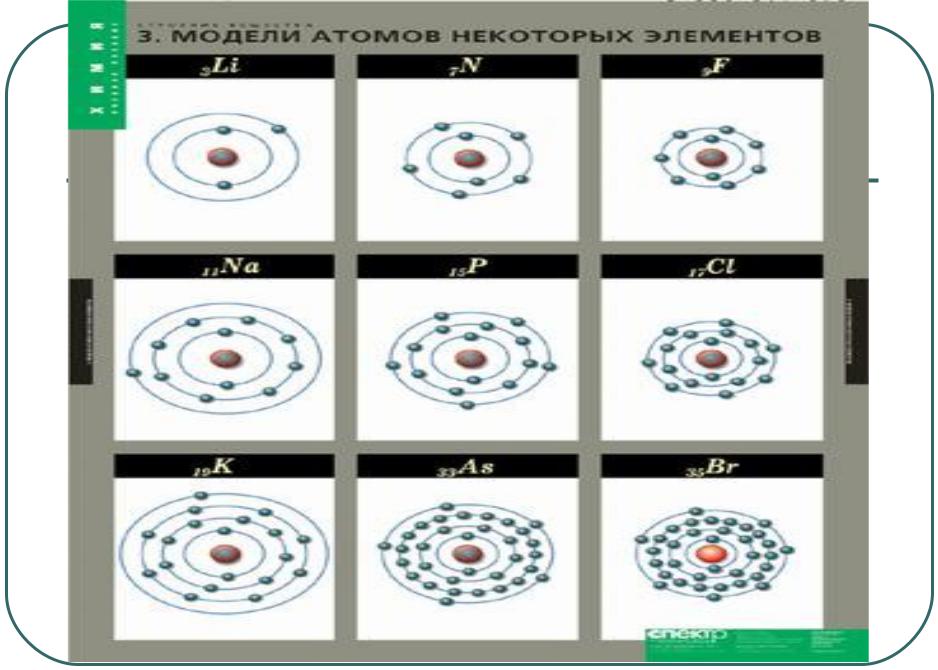
Электроны находятся в электронных оболочках. Атом может иметь семь оболочек таких как: K, L, M, N, ….,Q. Эти оболочки
состоят из 4-х типов уровней: s, p, d и f,
которые могут содержать 1, 3, 5, или 7 электронных орбит.
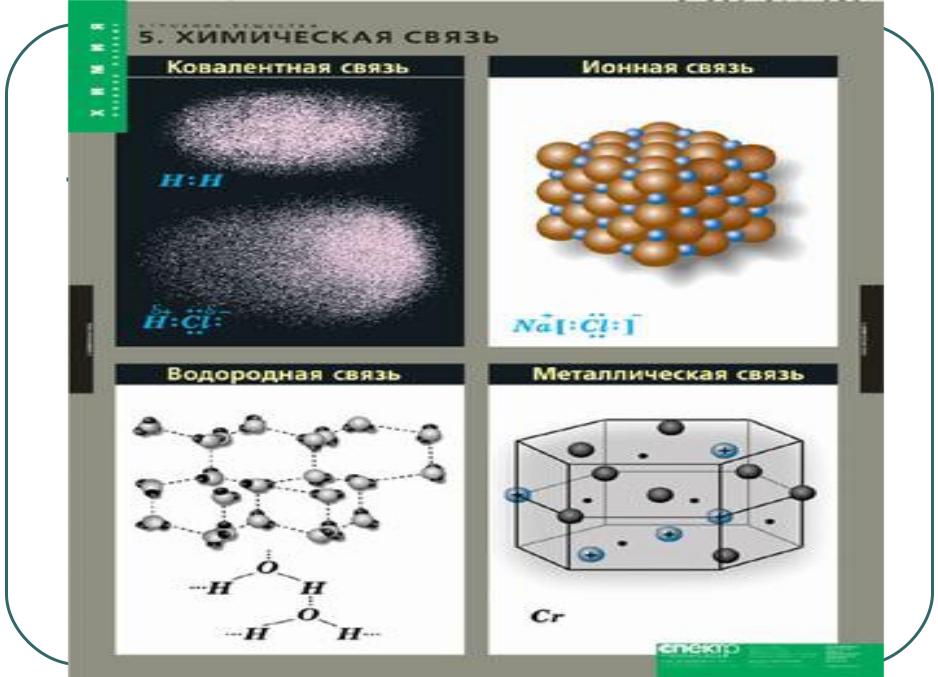
Внешние электроны (на внешних электронных орбитах) слабее связаны с ядром, чем
внутренние . Эти электроны по существу и обуславливают свойства тех или иных веществ: окислов, оснований , кислот, солей.
04.07.19 |
8 |
04.07.19 |
9 |

04.07.19 |
10 |

04.07.19 |
11 |

04.07.19 |
12 |
04.07.19 |
13 |
