
- •Оглавление
- •ВВЕДЕНИЕ
- •ЛАБОРАТОРНАЯ РАБОТА 1. КЛАССЫ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
- •ЛАБОРАТОРНАЯ РАБОТА 2. ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТОВ ЭЛЕМЕНТА И СЛОЖНОГО СОЕДИНЕНИЯ
- •ЛАБОРАТОРНАЯ РАБОТА 3. РАСТВОРЫ
- •ЛАБОРАТОРНАЯ РАБОТА 4. ЖЕСТКОСТЬ ВОДЫ И МЕТОДЫ ЕЕ УМЯГЧЕНИЯ
- •ЛАБОРАТОРНАЯ РАБОТА 5. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ
- •Ионообменные реакции
- •ЛАБОРАТОРНАЯ РАБОТА 6. ГИДРОЛИЗ СОЛЕЙ
- •ЛАБОРАТОРНАЯ РАБОТА 7.ТЕПЛОВЫЕ ЭФФЕКТЫ, НАПРАВЛЕНИЕ ХИМИЧЕСКИХ РЕАКЦИЙ
- •ЛАБОРАТОРНАЯ РАБОТА 8. ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
- •ЛАБОРАТОРНАЯ РАБОТА 10. ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ
- •ЛАБОРАТОРНАЯ РАБОТА 11. ЭЛЕКТРОЛИЗ РАСТВОРОВ ЭЛЕКТРОЛИТОВ
- •ЛАБОРАТОРНАЯ РАБОТА 12. КОРРОЗИЯ МЕТАЛЛОВ. ЗАЩИТА ОТ КОРРОЗИИ
- •ЛАБОРАТОРНАЯ РАБОТА 14. ПОЛУЧЕНИЕ ДИСПЕРСНЫХ СИСТЕМ. УСТОЙЧИВОСТЬ КОЛЛОИДНЫХ РАСТВОРОВ
- •ЛАБОРАТОРНАЯ РАБОТА 15. ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА МЕТАЛЛОВ
- •ЛАБОРАТОРНАЯ РАБОТА 17. ЛЕГИРУЮЩИЕ МЕТАЛЛЫ (ХРОМ, МАРГАНЕЦ)
- •ЛАБОРАТОРНАЯ РАБОТА 18. ТЯЖЕЛЫЕ КОНСТРУКЦИОННЫЕ МЕТАЛЛЫ ПОДГРУППЫ ЖЕЛЕЗА (ЖЕЛЕЗО, КОБАЛЬТ, НИКЕЛЬ)
- •ЛАБОРАТОРНАЯ РАБОТА 19. ЦИНК
- •ЛАБОРАТОРНАЯ РАБОТА 20. ОЛОВО И ЕГО КИСЛОРОДНЫЕ СОЕДИНЕНИЯ
- •ЛАБОРАТОРНАЯ РАБОТА 21. СВИНЕЦ И ЕГО КИСЛОРОДНЫЕ СОЕДИНЕНИЯ
- •ЛАБОРАТОРНАЯ РАБОТА 22. СВОЙСТВА МЕДИ И ЕЕ СОЕДИНЕНИЙ
- •БИБЛИОГРАФИЧЕСКИЙ СПИСОК
- •ПРИЛОЖЕНИЕ

БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1.Глинка, Н. Л. Общая химия : учеб. пособие для вузов / Н. Л. Глинка; под ред. А. И. Ермакова. – 29-е изд., исправленное. – М. : Интеграл-Пресс, 2001. – 728 с.
2.Теоретические основы общей химии / А. И. Горбунов, А. А. Гуров, Г. Г. Филиппов, В. Н. Шаповал. – М. : Изд-во МГУ, 2003. – 720 с.
3.Суворов, А. В. Общая химия / А. В. Суворов, А. Б. Никольский. –
СПб. : Химиздат, 2000. – 624 с.
4.Коровин. Н. В. Общая химия / Н. В. Коровин. – М. : Высш. шк., 2001. – 743 с.
5.Гельфман, М. И. Химия / М. И. Гельфман, В. П. Юстратов. – СПб. :
Лань, 2000. – 480 с.
6.Ахметов, Н. С. Общая и неорганическая химия / Н. С. Ахметов. –
М. : Высш. шк., 2002. – 743 с.
7.Дибров, И. А. Неорганическая химия / И. А. Дибров. – СПб. : Лань, 2001. – 432 с.
8.Егоров, В. В. Теоретические основы неорганической химии / В. В.
Егоров. – СПб. : Лань, 2005. – 192 с.
9.Зайцев, О. С. Химия. Современный краткий курс / О. С. Зайцев. –
М. : НЦ Энас, 2001. – 415 с.
10.Хаусткрофт, К. Современный курс общей химии : в 2 т. / К. Хаусткрофт, Э. Констебл. – М. : Мир, 2002. – 813 с.
11.Задачи и упражнения по общей химии : учеб. пособие / Б. И. Адамсон, О. Н. Гончарук, В. Н. Камышова [и др.]; под ред. Н. В. Коровина. – М. :
Высш. шк., 2003. – 255 с.
12.Гольбрайх, З. Е. Сборник задач и упражнений по химии : учеб. пособие для студентов / З. Е. Гольбрайх, Е. И. Маслов. – М. : ООО Астрель, 2004. – 383 с.
Химия. Лаб. практикум |
-197- |

ПРИЛОЖЕНИЕ
Таблица 1
Орбитальный атомный радиус, первый потенциал ионизации, сродство к электрону,
относительная электроотрицательность элементов
Элемент |
Rорб, нм |
J, кДж/моль |
ω, кДж/моль |
Е, отн. ед. |
Н |
0,053 |
1 310 |
73 |
2,1 |
He |
0,029 |
2 370 |
–21 |
0 |
Li |
0,159 |
520 |
57 |
1,0 |
Be |
0,104 |
900 |
–18 |
1,5 |
B |
0,078 |
800 |
29 |
2,0 |
C |
0,062 |
1 090 |
123 |
2,5 |
N |
0,052 |
1 400 |
–20 |
3,0 |
O |
0,045 |
1 310 |
142 |
3,5 |
F |
0,040 |
1 680 |
333 |
4,0 |
Ne |
0,035 |
2 080 |
123 |
0 |
Na |
0,171 |
496 |
33 |
0,9 |
Mg |
0,128 |
738 |
–21 |
1,2 |
Al |
0,131 |
578 |
48 |
1,5 |
Si |
0,107 |
768 |
178 |
1,8 |
P |
0,092 |
1 010 |
71 |
2,1 |
S |
0,081 |
1 000 |
200 |
2,5 |
Cl |
0,073 |
1 250 |
350 |
3,0 |
Ar |
0,066 |
1 520 |
–36 |
0 |
K |
0,216 |
419 |
48 |
0,8 |
Ca |
0,169 |
590 |
–186 |
1,0 |
Sc |
0,157 |
630 |
–70 |
1,3 |
Ti |
0,148 |
658 |
38 |
1,5 |
V |
0,140 |
650 |
63 |
1,6 |
Cr |
0,145 |
653 |
95 |
1,6 |
Mn |
0,128 |
717 |
–94 |
1,5 |
Fe |
0,123 |
762 |
56 |
1,8 |
Co |
0,118 |
759 |
91 |
1,8 |
Ni |
0,114 |
737 |
– |
1,8 |
Cu |
0,119 |
745 |
118 |
1,9 |
Химия. Лаб. практикум |
-198- |
ПРИЛОЖЕНИЕ
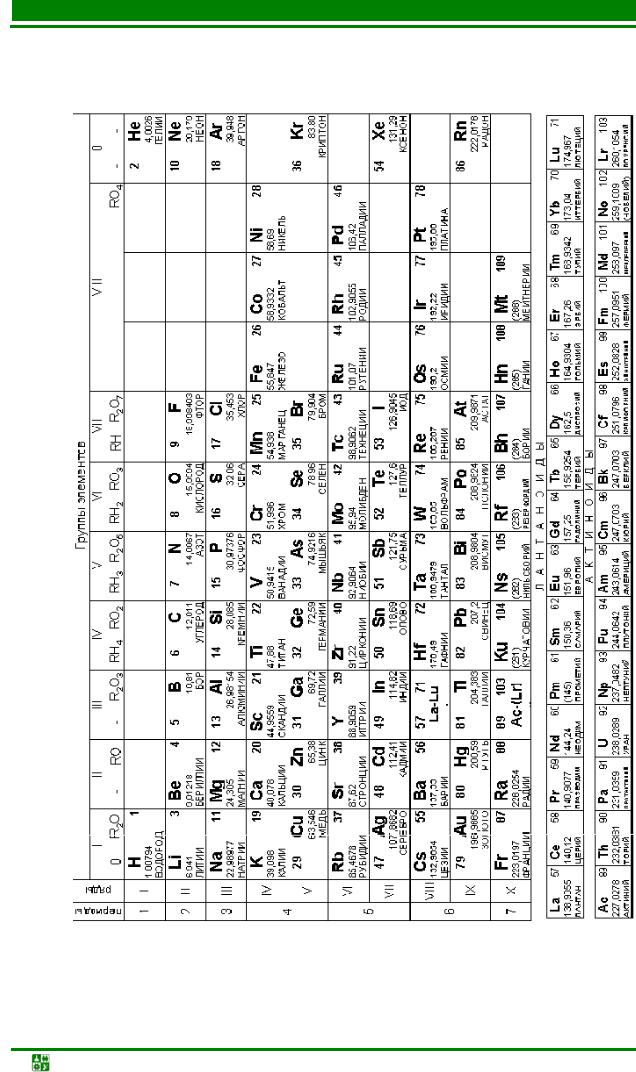
Таблица 2
Периодическая система элементов Д.И. Менделеева
Химия. Лаб. практикум |
-199- |

ПРИЛОЖЕНИЕ
|
|
|
|
|
|
Таблица 3 |
|
Стандартные энтальпии, энтропии и энергии Гиббса |
|
||||
|
|
образования некоторых веществ |
|
|||
|
|
|
|
|
|
|
Вещество |
|
Состояние |
Н°, |
S°, |
|
G°, |
|
кДж/моль |
Дж/(моль K) |
|
кДж/моль |
||
|
|
|
|
|||
Al |
|
к |
0 |
29,42 |
|
0 |
Al2O3 |
|
к |
−1676 |
50,92 |
|
−1582 |
С |
|
Графит |
0 |
5,7 |
|
0 |
CO |
|
г |
–110,5 |
197,5 |
|
–137,1 |
CO2 |
|
г |
−385,2 |
214,62 |
|
−394,38 |
CaCO3 |
|
к |
−1207,0 |
88,7 |
|
−1127,7 |
CaCl2 |
|
к |
–785,8 |
113,8 |
|
–750,2 |
CaF2 |
|
к |
–2114,6 |
68,9 |
|
–1161,9 |
Ca3N2 |
|
к |
–431,8 |
105 |
|
–368,6 |
CaO |
|
к |
−635,5 |
39,7 |
|
−604,2 |
Сa(OH)2 |
|
к |
–986,6 |
76,1 |
|
–896,8 |
Cl2 |
|
г |
0 |
222,9 |
|
0 |
Cl2O |
|
г |
76,6 |
266,2 |
|
94,2 |
ClO2 |
|
г |
105,0 |
257,0 |
|
122,3 |
HCl |
|
р |
−91,8 |
186,8 |
|
−94,8 |
Cr2O3 |
|
к |
−1440,6 |
81,2 |
|
−1050,0 |
Cu |
|
к |
0 |
33,15 |
|
0 |
Cu2+ |
|
р |
+64,3 |
−996,5 |
|
+64,9 |
CuSO4 |
|
к |
−770,9 |
109,0 |
|
−661,8 |
CuSO4·5H2O |
|
к |
−2 275,4 |
300 |
|
−1879,9 |
CuO |
|
к |
–162,0 |
42,6 |
|
–129,9 |
Cr2O3 |
|
к |
−1140 |
81,2 |
|
−1059,0 |
Fe |
|
к |
0 |
27,13 |
|
0 |
Fe2+ |
|
р |
−76,15 |
−50,2 |
|
−75,05 |
FeO |
|
к |
–264,8 |
60,8 |
|
–244,3 |
Fe2O3 |
|
к |
−822,2 |
87,4 |
|
−740,28 |
Fe3O4 |
|
к |
–1117,1 |
146,2 |
|
–1014,2 |
FeSO4 |
|
к |
−970,2 |
110,2 |
|
− 65,2 |
H2 |
|
г |
0 |
130,52 |
|
0 |
H+ |
|
р |
0 |
– |
|
0 |
OH– |
|
р |
−229,8 |
−2,52 |
|
−37,6 |
HBr |
|
г |
–36,3 |
198,6 |
|
–53,3 |
HCN |
|
г |
135,0 |
113,1 |
|
125,5 |
HF |
|
г |
–270,7 |
18,7 |
|
–272,8 |
HI |
|
г |
26,6 |
206,5 |
|
1,8 |
H2O |
|
ж |
−285,8 |
70,8 |
|
−237,24 |
H2O |
|
г |
−241,8 |
188,72 |
|
−228,6 |
H2S |
|
г |
−21,0 |
205,7 |
|
−33,8 |
Химия. Лаб. практикум |
-200- |

ПРИЛОЖЕНИЕ
Продолжение табл. 3
Вещество |
Состояние |
Н°, |
S°, |
G°, |
|
кДж/моль |
Дж/(моль K) |
кДж/моль |
|||
|
|
||||
KClO3 |
к |
–391,2 |
143,0 |
–289,9 |
|
MgCl2 |
к |
–641,1 |
89,9 |
–591,6 |
|
Mg3N2 |
к |
–461,1 |
87,9 |
–400,9 |
|
MgO |
к |
–601,8 |
26,9 |
–569,6 |
|
N2 |
г |
0 |
199,9 |
0 |
|
NO2 |
г |
+33,92 |
240,22 |
+51,5 |
|
N2O4 |
г |
+9,46 |
305,5 |
+97,39 |
|
NO |
г |
90,3 |
210,6 |
86,6 |
|
N2O |
г |
82,0 |
219,9 |
104,1 |
|
N2O3 |
г |
83,3 |
307,0 |
140,5 |
|
N2O5 |
к |
–42,7 |
1,8 |
114,1 |
|
NH3 |
г |
–46,2 |
192,6 |
–16,7 |
|
NH4NO3 |
к |
–365,4 |
151 |
–183,8 |
|
NH4Cl |
к |
–315,39 |
94,56 |
–343,64 |
|
NaOH |
к |
–426,6 |
64,18 |
–377,0 |
|
NaCl |
к |
–410,9 |
72,36 |
–384,0 |
|
NiO2 |
к |
–239,7 |
38,0 |
–211,6 |
|
O2 |
г |
0 |
204,82 |
0 |
|
F2 |
г |
0 |
202,7 |
0 |
|
OF2 |
г |
5,1 |
247,0 |
42,5 |
|
P2O3 |
к |
–820,0 |
173,5 |
– |
|
P2O5 |
к |
–1492,0 |
114,5 |
–1 348,8 |
|
PbO |
к |
–219,3 |
66,1 |
–189,1 |
|
PbO2 |
к |
–276,6 |
74,9 |
–218,3 |
|
S |
Ромб. |
0 |
31,88 |
0 |
|
SO2 |
г |
–296,9 |
248,1 |
–300,2 |
|
SO3 |
г |
–395,8 |
256,7 |
–371,2 |
|
H2SO4 |
р |
−81,42 |
156,9 |
−690,3 |
|
SiO2 |
к |
–859,3 |
42,9 |
–803,75 |
|
SnO |
к |
–286,0 |
56,5 |
–256,9 |
|
SnO2 |
к |
–580,8 |
52,3 |
–519,3 |
|
Cr2O3 |
к |
−1 140 |
81,2 |
−1 059,0 |
|
C2H6 |
г |
− 85,94 |
229,5 |
− 32,9 |
|
C2H5OH |
ж |
− 277,6 |
160,7 |
− 174,8 |
Химия. Лаб. практикум |
-201- |

ПРИЛОЖЕНИЕ
Таблица 4
Растворимость кислот, солей и оснований в воде
Катионы |
|
|
|
|
|
|
|
|
|
Анионы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
– |
Br |
– |
J |
– |
– |
– |
2– |
|
2– |
2– |
2– |
2– |
3– |
– |
|
|
|
|
|
NO3 |
CH3COO |
S |
|
SO3 |
SO4 |
CO3 |
SiO3 |
PO4 |
OH |
|||
Li+ |
Р |
Р |
Р |
Р |
Р |
Р |
|
Р |
Р |
Р |
Н |
Н |
Р |
|||
Na+, |
Р |
Р |
Р |
Р |
Р |
Р |
|
Р |
Р |
Р |
Р |
Р |
Р |
|||
K+ |
Р |
Р |
Р |
Р |
Р |
Р |
|
Р |
Р |
Р |
Р |
Р |
Р |
|||
NH4+ |
Р |
Р |
Р |
Р |
Р |
Р |
|
Р |
Р |
Р |
– |
Р |
Р |
|||
Cu2+ |
Р |
Р |
– |
Р |
Р |
Н |
Н |
Р |
– |
– |
Н |
Н |
||||
Ag+ |
Н |
Н |
Н |
Р |
Р |
Н |
Н |
М |
Н |
– |
Н |
– |
||||
Mg2+ |
Р |
Р |
Р |
Р |
Р |
– |
|
Н |
Р |
Н |
Н |
Н |
Н |
|||
Са2+ |
Р |
Р |
Р |
Р |
Р |
Р |
|
Н |
М |
Н |
Н |
Н |
М |
|||
Sr+ |
Р |
Р |
Р |
Р |
Р |
Р |
Н |
Н |
Н |
Н |
Н |
М |
||||
Ba2+ |
Р |
Р |
Р |
Р |
Р |
Р |
|
Н |
Н |
Н |
Н |
Н |
Р |
|||
Zn2+ |
Р |
Р |
Р |
Р |
Р |
Н |
Н |
Р |
Н |
Н |
Н |
Н |
||||
Hg2+ |
Р |
М |
Н |
Р |
Р |
Н |
– |
Р |
– |
– |
Н |
– |
||||
Al3+ |
Р |
Р |
Р |
Р |
Р |
– |
|
– |
Р |
– |
Н |
Н |
Н |
|||
Sn2+ |
Р |
Р |
Р |
– |
– |
Н |
|
– |
Р |
– |
– |
Н |
Н |
|||
Pb2+ |
М |
М |
Н |
Р |
Р |
Н |
Н |
Н |
Н |
Н |
Н |
Н |
||||
Bi3+ |
– |
|
– |
– |
Р |
– |
Н |
Н |
– |
Н |
– |
Н |
Н |
|||
Cr3+ |
Р |
Р |
Р |
Р |
– |
– |
|
– |
Р |
– |
– |
Н |
Н |
|||
Mn2+ |
Р |
Р |
Н |
– |
Р |
Н |
Н |
Р |
Н |
Н |
Н |
Н |
||||
Fe3+ |
Р |
Р |
– |
Р |
– |
Н |
|
– |
Р |
– |
Н |
Н |
Н |
|||
Fe2+ |
Р |
Р |
Р |
Р |
Р |
Н |
Н |
Р |
Н |
Н |
Н |
Н |
||||
Примечание. Р – растворимое вещество; М – малорастворимое вещество; Н – практически нерастворимое вещество; прочерк означает, что вещество не существует или разлагается водой.
Химия. Лаб. практикум |
-202- |

ПРИЛОЖЕНИЕ
|
|
Таблица 5 |
|
|
Константы нестойкости |
|
|
|
некоторых комплексных ионов |
|
|
|
|
|
|
Комплексо- |
Уравнение диссоциации комплексных ионов |
Кн |
|
образователь |
|||
|
|
||
|
|
|
|
|
[Ag(NH3)2]+ 'Ag+ + 2NH3 |
6,8 · 10–8 |
|
Ag+ |
[Ag(CN)2]– 'Ag+ + 2CN– |
1,0 · 10–21 |
|
|
[Ag(S2O3)2]3–'Ag+ + 2S2O 32− |
1,0 · 10–13 |
|
|
|
|
|
Cd2+ |
[Cd(NH3)4]2+ 'Cd2+ + 4NH3 |
1,0 · 10–7 |
|
[Cd(CN)4]2– 'Cd2+ + 4CN– |
1,4 · 10–17 |
||
|
|||
|
|
|
|
Co2+ |
[Co(NH3)6]2+ 'Co2+ + 6NH3 |
1,3 · 10–5 |
|
[Co(SCN)4]2– 'Co2+ + 4SCN– |
1,0 · 10–3 |
||
|
|||
|
|
|
|
Cu2+ |
[Cu(NH3)4]2+ 'Cu2+ + 4NH3 |
2,0 · 10–13 |
|
[Cu(CN)4]2– 'Cu2+ + 4CN– |
5,0 · 10–28 |
||
|
|||
|
|
|
|
Fe3+ |
[Fe(CN)6]3– 'Fe3+ + 6CN– |
1,0 · 10–44 |
|
|
|
|
|
Fe2+ |
[Fe(CN)6]4– 'Fe2+ + 6CN– |
1,0 · 10–37 |
|
|
|
|
|
|
[Hg(NH3)4]2+ 'Hg2+ + 4NH3 |
5,3 · 10–20 |
|
Hg2+ |
[Hg(Cl)4]2– 'Hg2+ + 4Cl– |
8,5 · 10–16 |
|
|
[Hg(CN)4]2– 'Hg2+ + 4CN– |
4,0 · 10–42 |
|
|
|
|
|
Ni2+ |
[Ni(NH3)4]2+ 'Ni2+ + 4NH3 |
1,1 · 10–8 |
|
[Ni(CN)4]2– 'Ni2+ + 4CN– |
1,8 · 10–14 |
||
|
|||
|
|
|
|
|
[Zn(NH3)4]2+ 'Zn2+ + 4NH3 |
3,5 · 10–10 |
|
Zn2+ |
[Zn(OH)4]2– 'Zn2+ + 4OH– |
3,6 · 10–16 |
|
|
[Zn(CN)4]2– 'Zn2+ + 4CN– |
1,3 · 10–17 |
|
|
|
|
Химия. Лаб. практикум |
-203- |

ПРИЛОЖЕНИЕ
Таблица 6
Произведение растворимости труднорастворимых в воде соединений (при 298 К)
Соединение |
ПР |
Соединение |
ПР |
|
|
|
|
AgCl |
1,6 · 10–10 |
SrSO4 |
3,2 · 10–7 |
AgBr |
4,4 · 10–13 |
PbCl2 |
2,1 · 10–5 |
AgI |
9,7 · 10–17 |
PbI2 |
9,8 · 10–9 |
Ag2SO4 |
7,7 · 10–5 |
PbSO4 |
1,6 · 10–8 |
Ag2S |
1,6 · 10–49 |
PbS |
3,6 · 10–29 |
BaCO3 |
8,1 · 10–9 |
ZnS |
7,4 · 10–27 |
BaSO4 |
1,1 · 10–10 |
HgS |
10–58 |
MgCO3 |
1,0 · 10–5 |
AgOH |
1,9 · 10–28 |
CaCO3 |
4,8 · 10–9 |
Al(OH)3 |
5,1 · 10–33 |
CaSO4 |
6,1 · 10–5 |
Cr(OH)3 |
6,7 · 10–31 |
CaF2 |
4,0 · 10–11 |
Fe(OH)3 |
3,8 · 10–38 |
CdS |
1,2 · 10–28 |
Mg(OH)2 |
5,5 · 10–12 |
CuS |
4,0 · 10–38 |
Ni(OH)2 |
1,6 · 10–14 |
Cu2S |
2,0 · 10–48 |
Cu(OH)2 |
5,0 · 10–19 |
FeS |
3,7 · 10–19 |
Pb(OH)2 |
1,0 · 10–15 |
MnS |
2,0 · 10–15 |
Zn(OH)2 |
1,3 · 10–17 |
|
|
|
|
Химия. Лаб. практикум |
-204- |

ПРИЛОЖЕНИЕ
Таблица 7
Способы выражения концентраций растворов
|
|
Количество, масса |
Способ выраже- |
||
Концентрация |
Обозна- |
или объем вещества |
ния концентра- |
||
чение |
|
|
|
ции или размер- |
|
|
раствори- |
раствора |
растворителя |
||
|
|
мого |
ность |
||
|
|
|
|
|
|
Молярная |
СМ |
х, моль |
м3, л |
До 1 м3, 1 л |
моль/м3, моль/л |
|
|
|
|
|
|
Молярная |
|
|
|
|
моль экв/м3, |
концентрация |
Сэкв (В) |
х, моль экв |
м3, л |
До 1 м3, 1 л |
|
эквивалентов |
|
|
|
|
моль экв/л |
(нормальная) |
|
|
|
|
|
Моляльность |
См (В) |
х, моль |
– |
1 кг |
моль/кг |
|
|
|
|
|
|
Массовая |
ρ В |
х, кг |
м3, л |
До 1 м3; до 1 л |
кг/м3, кг/л |
|
|
|
|
|
|
Титр |
ТВ |
х, г |
мл, см3 |
До 1 мл |
г/мл, г/см3 |
|
|
|
|
|
|
Молярная доля |
хВ |
х, моль |
(х + у), моль |
у, моль |
х/(х + у) |
|
|
|
|
|
|
Массовая доля |
ω |
х, кг |
(х + у), кг |
у, кг |
х/(х + у) |
|
|
|
|
|
|
Объемная доля |
ϕ |
х, м3 |
(х + у), м3 |
у, м3 |
у/(х + у) |
|
|
|
|
|
|
Химия. Лаб. практикум |
-205- |

ПРИЛОЖЕНИЕ
Таблица 8
Константы диссоциации некоторых слабых электролитов
Электролит |
Кд |
Азотистая кислота HNO2 |
4·10–4 |
Бромноватистая кислота HOBr |
2,1·10–9 |
Гидроксид аммония NH4OH |
1,8·10–5 |
Кремниевая кислота H2SiO3: |
|
K1 |
2,2·10–10 |
K2 |
1,6·10–12 |
Муравьиная кислота НСООН |
1,8·10–4 |
Ортофосфорная кислота Н3РО4: |
|
К1 |
7,5·10–3 |
К2 |
6,3·10–8 |
К3 |
1,3·10–12 |
Пероксид водорода Н2О2 |
2,6·10–12 |
Серная кислота H2SO4, K2 |
1,2·10–2 |
Вода Н2О |
1,8·10–16 |
Железа(II) гидроксидFe(OH)2, К2 |
1,3·10–4 |
Железа (III) гидроксид Fe(OH)3: |
|
K2 |
1,8·10–11 |
K3 |
1,4·10–12 |
Цинка гидроксид Zn(OH)2: |
|
K1 |
4,4·10–5 |
K2 |
1,5·10–9 |
Кадмия гидроксид, Cd(OH)2, K2 |
5,0·10–3 |
Сернистая кислота H2SO3, K1 |
1,6·10–2 |
Электролит |
Кд |
Сероводород H2S: |
|
K1 |
6·10–8 |
K2 |
1·10–14 |
Угольная кислота H2CO3: |
|
K1 |
4,5·10–7 |
K2 |
4,7·10–11 |
Уксусная кислота СН3СООН |
1,8·10–5 |
Хлорноватистая кислота HOCl |
5,0·10–8 |
Фтороводород HF |
6,6·10–4 |
Циановодород HCN |
7,9·10–9 |
Щавелевая кислота Н2С2О4: |
|
K1 |
5,4·10–2 |
K2 |
5,4·10–5 |
Алюминия гидроксид, К3 |
1,4·10–9 |
Меди (II) гидроксид Cu(OH)2, К2 |
3,4·10–7 |
Никеля гидроксид Ni(OH)2, K2 |
2,5·10–5 |
Серебра гидроксид AgOH |
1,1·10–4 |
Хрома(III) гидроксидCr(OH)3, K3 |
1,0·10–10 |
Свинца гидроксид Pb(OH)2: |
|
K1 |
9,6·10–4 |
K2 |
3,0·10–8 |
Марганца (II) гидроксид |
5,0·10–4 |
Mn(OH)2, K2 |
|
Химия. Лаб. практикум |
-206- |

ПРИЛОЖЕНИЕ
|
Стандартные потенциалы металлических |
||
|
|
и газовых электродов |
|
|
|
|
|
Электрод |
|
Электродная реакция |
|
|
|
|
|
Li+/Li |
|
Li+ + e 'Li |
|
Rb+/Rb |
|
Rb+ + e 'Rb |
|
K+/K |
|
K+ + e 'K |
|
Cs+/Cs |
|
Cs+ + e 'Cs |
|
Ra2+/Ra |
|
Ra2+ + 2 e 'Ra |
|
Ba2+/Ba |
|
Ba2+ + 2 e 'Ba |
|
Ca2+/Ca |
|
Ca2+ + 2 e 'Ca |
|
Na+/Na |
|
Na+ + e 'Na |
|
Mg2+/Mg |
|
Mg2+ + 2 e 'Mg |
|
Be2+/Be |
|
Be2+ + 2 e 'Be |
|
Al3+/Al |
|
Al3+ + 3 e 'Al |
|
Ti2+/Ti |
|
Ti2+ + 2 e 'Ti |
|
V2+/V |
|
V2+ + 2 e 'V |
|
Mn2+/Mn |
|
Mn2+ + 2 e 'Mn |
|
Cr2+/Cr |
|
Cr2+ + 2 e 'Cr |
|
Zn2+/Zn |
|
Zn2+ + 2 e 'Zn |
|
Cr3+/Cr |
|
Cr3+ + 3 e 'Cr |
|
Fe2+/Fe |
|
Fe2+ + 2 e 'Fe |
|
Cd2+/Cd |
|
Cd2+ + 2 e 'Cd |
|
Co2+/Co |
|
Co2+ + 2 e 'Cо |
|
Ni2+/Ni |
|
Ni2+ + 2 e 'Ni |
|
Таблица 9
Е0, В –3,045 –2,925 –2,925 –2,923 –2,916 –2,906 –2,866 –2,714 –2,363 –1,847 –1,662 –1,628 –1,186 –1,180 –0,913 –0,763 –0,744 –0,440 –0,403 –0,277 –0,250
Химия. Лаб. практикум |
-207- |

ПРИЛОЖЕНИЕ
Электрод |
Электродная реакция |
Sn2+/Sn |
Sn2+ + 2 e 'Sn |
Pb2+/Pb |
Pb2+ + 2 e 'Pb |
Fe3+/Fe |
Fe3+ + 3 e 'Fe |
H+/H |
H+ + e 'H |
Ge2+/Ge |
Ge2+ + 2 e 'Ge |
Cu2+/Cu |
Cu2+ + 2 e 'Cu |
O2/OH– |
1/2O2 + H2O + 2 e '2OH– |
Cu+/Cu |
Cu+ + e 'Cu |
Ag+/Ag |
Ag+ + e 'Ag |
Hg2+/Hg |
Hg2+ + 2 e 'Hg |
Pd2+/Pd |
Pd2+ + 2 e 'Pd |
Pt2+/Pt |
Pt2+ + 2 e 'Pt |
O2/H2O |
O2 + 4H+ + 4 e '2H2O |
Cl2/Cl– |
12 Cl2 + e 'Cl– |
Au3+/Au |
Au3+ + 3 e 'Au |
Au+/Au |
Au+ + e ' Au |
H2/H– |
12 H2 + e ' H– |
F2/F– |
12 F2 + e ' F– |
Продолжение табл. 9
Е0, В –0,136 –0,126 –0,036 +0,000 +0,010 +0,337 +0,401 +0,521 +0,799 +0,854 +0,987 +1,200 +1,229 +1,359 +1,498 +1,691 +2,200 +2,866
Химия. Лаб. практикум |
-208- |
