
Хронобиология
.pdf
генетические часы, отсчитывающие время суток. Транскрипцион- но-трансляционную петлю часового механизма принято делить на два блока: транскрипционный (положительный) и трансляционный (отрицательный).
Положительный блок. Гены Clk и Cyc являются транскрипционными факторами. Их белки CLK и CYC образуют в ядре транскрипционный комплекс из гетеродимеров CYC/CLK, которые активируют транскрипцию генов Per и Tim. Уровни матричной РНК генов Per и Tim поднимаются и транслируются затем в цитоплазме в протеины (рис. 58, 1).
Рис. 58. Модель циркадианных внутриклеточных часов у дрозофилы (1) и мыши (2). Стрелки показывают активацию или направление процесса, дуга, ограниченная поперечной черточкой, – ингибирование
Отрицательный блок. В цитоплазме белки PER и TIM накапливаются и формируют вместе с белком DBT гетеродимеры (DBT/TIM/PER). Гетеродимеризация служит двум функциям: стабилизирует PER, который в отсутствие TIM является нестабильным, и способствует входу комплекса в ядро. Белок DBT регулирует накопление PER, влияя на его фосфорилирование. После достижения гетеродимерами в цитоплазме пороговой концентрации, они направляются в ядро. В ядре DBT/TIM/PER ингибирует транскрипционную активность белкового комплекса CYC/CLK, отрицательно воздействуя на транскрипцию собственных генов этих белков.
В темноте оба белка PER/TIM фосфорилируются и постепенно деградируют, в результате блокировка транскрипционного ком-
201
плекса CYC/CLK снимается. Восстанавливаются функции генов Сyc и Сlk, и вновь запускается синтез мРНК генов Per и Tim.
Генетическая модель циркадианных часов у млекопитаю-
щих. Знание часового механизма у дрозофилы сильно помогло формированию модели часового механизма у млекопитающих. Гомологи большинства генов, работающих в часовом механизме дрозофилы, были найдены и у млекопитающих.
Положительный блок. Два гена Clock и Bmal1 кодируют транскрипционные факторы CLOCK и BMAL1. Эта пара циркадианных белков-активаторов формирует транскрипционный гетеродимерный комплекс CLOCK/BMAL1, который распознает последовательность CACGTG (так называемую «E-box») и, связываясь с ней, запускает транскрипцию «часовых» генов Реr1/Реr2 и Cry1/Cry2, кодирующих соответствующие белки PER и CRY (рис. 58, 2).
Отрицательный блок. Когда содержание белков PER и CRY в цитоплазме достигает определенного уровня, они образуют комплекс между собой и с казеинкиназами CK1 / и входят в ядро. В ядре белковый комплекс выступает в роли репрессора активности транскрипционного комплекса CLOCK/BMAL1, в результате блокируется транскрипция собственных генов Реr1/Реr2 и Cry1/Cry2. Одновременно казеинкиназы дельта и эпсилон фосфорилируют белки PER и CRY, что приводит к их деградации. Когда снижающийся уровень белков PER и CRY в клетке достигает базового, транскрипционный димер CLOCK/BMAL1 высвобождается, чтобы начать новый суточный цикл в клетке – активировать экспрессию «часовых» генов Per и Cry. Эти события повторяются в клетке ритмически с периодом около 24 ч.
Для четкой работы внутриклеточных часов необходимо, чтобы максимально точно контролировалось время задержки перемещения белков из цитоплазмы в ядро. Как осуществляется контроль этого процесса, до конца не изучено. Однако показано, что регуляция перемещения белковых комплексов осуществляется на посттрансляционном уровне, как указывалось выше, за счет фосфорилирования белков. Этот процесс, влияя на стабильность ключевых циркадных белков, поддерживает точность работы часов. Напри-
202
мер, фосфорилирование PER изменяет его стабильность и тормозит скорость перемещения как этого белка, так и CRY в ядро клетки (для попадания в ядро CRY должен связаться с PER). Основными ферментами, ответственными за фосфорилирование этих белков, являются казеинкиназы дельта и эпсилон. Показано, что их мутации могут вызывать значительные изменения суточных ритмов.
Таким образом, циркадианные часы представляют собой моле- кулярно-генетическую систему регуляции синтеза белка с отрицательной обратной связью, осуществляемой этим же белком (являющимся репрессором собственного гена). Солнечный свет активизирует светочувствительные рецепторы, возбуждение передается группе нейронов мозга с работающими «часовыми» генами. При транскрипции «часового» гена образуется мРНК «часового» белка, который синтезируется в цитоплазме, а затем диффундирует в ядро и блокирует транскрипцию «часового» гена. После распада мРНК и «часового» белка работа «часовых» генов возобновляется, процесс повторяется.
Суточный ритм – это лишь одна из составляющих широкого спектра ритмов организма. Следовательно, должны существовать либо дополнительные «часовые» устройства, либо преобразователи циркадианного ритма в низко- и высокочастотные ритмы. В этом направлении ведутся интенсивные поиски. В 2009 г. генетики из медицинской школы университета Пенсильвании
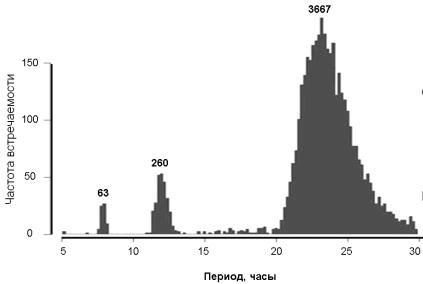
(University of Pennsylvania School of Medicine) и института Солка (Salk Institute for Biological Studies) обнаружили в клетках печени мышей два кластера генов, которые осциллировали с периодами равными второй ( 12 ч) и третьей гармоникам ( 8 ч) циркадианного ритма (рис. 59).
Эксперименты показали, что 12-часовые осцилляции транскрипции генов происходят не только в клетках печени, но и в некоторых других тканях, включая сердце, почки, надпочечники, легкие, гипоталамус. Так как пик активности 12-часовых генов в тканях мышей приходился на сумеречные и рассветные часы, было высказано предположение, что функция этих генов может за-
203
ключаться в физиологической подготовке организма к суточной смене освещения. Среди 12-часовых оказались гены, вовлеченные в регуляцию клеточного деления и синтеза белка, а среди 8- часовых – гены, участвующие в клеточных сигнальных процессах и обмене липидов.
Рис. 59. Гистограмма ритмичности генов из клеток печени.
Длина периода транскрипции около трёх с половиной тысяч генов печени (это порядка 4% всех носителей наследственной информации) примерно сутки, еще 260 генов – 12 часов, 63 генов – 8 ч
Эксперименты с инверсией суточного режима питания (доступ к пище только днем) показали, что из восьми 12-часовых генов семь изменили свой режим работы. Эти результаты дали основания предполагать, что физиологическим синхронизатором этого генного ритма может быть, например, пищевой метаболизм
(рис. 60).
Связь 8-часовых генов с физиологическими процессами обнаружить пока не удалось.
204

|
|
активность |
|
активность |
|||
|
|
,у.е |
|
|
|
,у.е |
|
|
|
|
|
|
|
|
|
|
активность |
|
|
активность |
|
|
|||
|
|
|
|
|
|
,у.е ,у.е
мышей. |
|
часовыхгенов гепатоцитов печени |
извосьми исследованных генов |
ритмапитания сдвинуло фазу активности 12- |
транскрипционный профиль только четырех |
Изменение |
Показан |
Рис. 60. |
|
205
Кроме того, есть серьезные успехи в выяснении самого трудного вопроса – температурной независимости часов. Аминокислотные цепи PER- и TIM-белков образуют петли – складываются при взаимодействии аминокислот друг с другом. В то же время отдельные молекулы белков PER и TIM образуют димеры, соединяясь друг с другом. Процессы внутримолекулярного и межмолекулярного взаимодействия в точности противоположным образом зависят от температуры. В результате повышение температуры приводит к уменьшению активности одного процесса и увеличению активности другого таким образом, что итоговая «активная поверхность» белка остается постоянной и часы идут независимо от температуры.
Контрольные вопросы и задания
1.Зачем нужны часы живым организмам?
2.Назовите основные аргументы сторонников теории внешних
ивнутренних часов.
3.Чем циркадианный ритм отличается от суточного?
4.Какие требования предъявляются к механизму биологических часов?
5.Расскажите об этапах поиска внутриклеточных биологических часов (ход научной мысли).
6.Кто и на каком объекте получил первые доказательства генетической природы биологических часов?
7.Перечислите основные «часовые» гены, найденные у дрозофилы и мыши?
8.В чем заключается сходство работы часового механизма у разных организмов?
9.Чем различаются генетические модели часов у Drosophila melanogaster и млекопитающих?
10.Опишите распределение отдельных этапов работы внутриклеточных часов в течение суток.
11.Какие периоды транскрипции генов, кроме циркадианных, обнаружены?
12.Что показали эксперименты с инверсией суточного режима питания мышей?
206
9. РЕГУЛЯТОРЫ ЦИРКАДИАННЫХ БИОЛОГИЧЕСКИХ РИТМОВ
Вкаждой клетке живых организмов существуют молекулярногенетические циркадианные часы, которые работают согласованно между собой и с периодическими изменениями физических факторов окружающей среды, связанными с вращением Земли. Тем самым обеспечивается иерархическая и упорядоченная в течение суток последовательность поведенческих, физиологических и биохимических процессов в организме. Каким образом осуществляется согласование работы множества внутриклеточных часов? Тонкие нейрохимические механизмы этого процесса в настоящее время еще не известны, однако о некоторых физиологических и биохимических механизмах регуляции циркадных ритмов научное сообщество уже имеет представление.
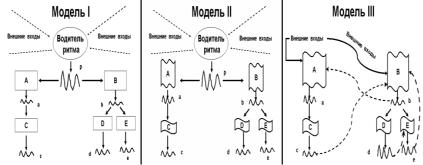
В70-х гг. прошлого столетия группой биоритмологов (М. МурИд с соавт., 1984) были предложены три модели организации циркадианных систем: одна – моноосцилляторная и две – мультиосцилляторные (рис. 61).
Рис. 61. Три модели циркадианной системы млекопитающих. Модель I – система с одним осциллятором, модели II и III относятся к системам с множественными осцилляторами, образующими (модель II) или не образующими (модель III) иерархическую структуру
207
Модель I (моноосцилляторная). Эта модель подразумевалась во многих исследованиях примерно до середины ХХ в. Она представляет собой совокупность связанных клеточных систем (А, В, С и т.д.), пассивно колеблющихся под воздействием одного автономного ведущего осциллятора – водителя ритма (ВР). Если эти клеточные системы обособлены друг от друга, связь между ними осуществляется с помощью посредников (а, b, с и т.д.), изменяющих свою активность с тем же периодом, что и ВР, но не обязательно с совпадением по фазе. Такие посредники, предположительно нейромедиаторы или гормоны, передают колебания ВР различным пассивно реагирующим клеточным системам. Циркадианная система в целом может захватываться внешними сигналами через экстероцептивные сенсорные пути к ведущему осциллятору.
Модель II (мультиосцилляторная). Согласно этой модели в различных органах и тканях организма существует система автономных осцилляторов (или пейсмекеров), способных поддерживать колебания и без периодических внешних сигналов. Один из осцилляторов является ведущим. Через него осуществляется связь со средой. При 24-часовом периоде светотемнового режима работа всех осцилляторов более или менее синхронизируется, и вся система ведет себя как единый осциллятор. Как и в модели I, здесь предполагается наличие нервных и эндокринных посредников, поддерживающих связи и синхронизацию между осцилляторами. Однако в этой модели посредники активно захватывают ритмы автономных клеточных осцилляторов, контролируя их фазу.
Модель III (мультиосцилляторная). В этой модели отсутствует постоянно закрепленная за каким-либо осциллятором функция ведущего. Существует система из объединенных в группы осцилляторов. В каждой группе имеется свой ВР. ВР отдельных групп связаны между собой через нервные и эндокринные посредники, которые обеспечивают обратную связь между осцилляторами. Как и в модели II, они синхронизируют осцилляторы путем активного захватывания. Каждая из групп проявляет наибольшую чувствительность к различным воздействиям среды. Одним из следствий такой организации может быть неодинаковая чувствительность
208
физиологических ритмов к воздействию различных факторов среды. Эти модели были предложены более 30 лет назад.
Согласно современным представлениям согласование множества ритмических процессов, протекающих в организме, в единый ритм происходит потому, что эукариоты обладают мощной иерархической функциональной системой, синхронизирующей ритмы между собой и с факторами среды. В ее состав входят и нервные элементы, действующие наподобие генератора колебаний в электронных системах, и огромный гуморальный отдел. Нервная система обеспечивает быстрое управление ритмами, а гуморальная – медленный и длительный. Эту систему в зависимости от типа ритма – циркадианного (околосуточного) или цирканнуального (окологодового) – называют в первом случае циркадианной, а во втором – цирканнуальной.
Однако в организме эти системы взаимосвязаны. Для восприятия и захвата внешних ритмов, а также синхронизации и управления осцилляторами в периферических тканях они используют практически одни и те же структуры нервной и эндокринной систем независимо от типа ритма. В современной хронобиологии предлагается эти две системы рассматривать как общую функциональную систему регуляции биоритмами, а для ее названия использовать один термин – фотопериодическая система. Однако требования к циркадианной и цирканнуальной частям системы разные.
Основным датчиком времени (внешним синхронизирующим фактором) для гомойотермных животных, в том числе и для человека, является фотопериод (длительность суточной или сезонной освещенности). Он – самый стабильный и надежный из всех остальных параметров среды, самый стойкий к действию помех, фотопериод полностью совпадает с главными внешними периодическими факторами – вращением Земли вокруг собственной оси и обращением ее вокруг Солнца.
Циркадианная часть фотопериодической системы должна ежедневно реагировать на фотопериод для ежесуточной синхронизации собственных циркадианных ритмов с длительностью фотопериода.
209
Цирканнуальная часть должна реагировать на динамику изменения фотопериода, т.е. сравнивать наличную длительность фотопериода с предыдущей, в результате чего распознавать, убывает или прибывает день.
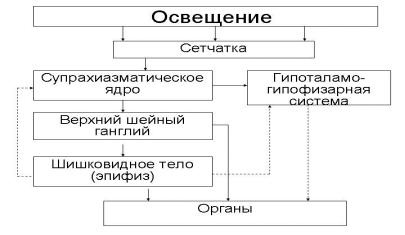
Рис. 62. Основные компоненты циркадианной части фотопериодической системы. Пунктирными линиями показаны гуморальные влияния
Рассмотрим основные компоненты циркадианной части фотопериодической системы (см. рис. 62), так как она является наиболее изученной. Циркадианная часть фотопериодической системы головного мозга млекопитающих включает следующие основные элементы: сетчатку глаза как орган, воспринимающий внешний времязадатель; супрахиазматические ядра (СХЯ) – центральные часы организма (их молекулярный механизм у млекопитающих образует «часовые» гены); симпатическую нервную систему как нервную эффекторную цепь, передающую синхронизированные ритмы от СХЯ к подчиненным молекулярным часам в других областях мозга и в периферических органах и тканях; нейросекреторные ядра гипоталамуса как гуморальные эффекторные элементы; эпифиз (шишковидное тело) как орган, вырабатывающий
210
