
1 Общие положения
Контрольная работа должна выполняться студентом после изучения определенного объема дисциплины или всего курса.
Студенту выдается индивидуальное задание, согласно которому он должен выполнить работу в соответствии с методическими указаниями и оформить контрольную работу в соответствии с требованиями ГОСТа.
При выполнении работы необходимо соблюдать следующие требования:
Обязательно записать условие индивидуального задания;
Расчеты сопровождать кратким пояснительным текстом, в котором должно быть указано, какая величина определяется и по какой формуле, какие величины подставляют в формулу (из условия работы, из справочника, определена ранее и т.д.);
Вычисления давать в развернутом виде;
Обязательно проставлять размерности всех заданных и расчетных величин в международной системе СИ;
Графический материал должен быть выполнен четко в масштабе на миллиметровой бумаге.
После решения должен быть произведен краткий анализ полученных результатов и сделаны соответствующие выводы.
В конце работы дать перечень использованной литературы.
2 Задания к контрольной работе Задача №1.
В процессе изменения состояния 1 кг газа внутренняя энергия его увеличивается на и. При этом над газом совершается работа, равная l. Начальная температура газа t1, конечное давление р2.
Определить для заданного газа показатель политропы п, начальные и конечные параметры, изменение энтропии s и изменение энтальпии h. Представить процесс в р и Тs - диаграммах. Изобразить также (без расчета) изобарный, изохорный, изотермический и адиабатный процессы, проходящие через ту же начальную точку, и дать их сравнительный анализ.
Контрольный вопрос. Какова общая формулировка и математическое выражение первого закона термодинамики?
Рекомендации к решению задачи №1
Закрепление теоретического материала по термодинамическим процессам производится решением задачи №1 индивидуального задания.
Для определения температуры в конце политропного процесса сжатия можно воспользоваться формулой:
![]() ,
(1)
,
(1)
где
![]()
изменение внутренней энергии в процессе,
изменение внутренней энергии в процессе,
![]() (из условия задачи);
(из условия задачи);
![]() массовая
теплоемкость газа при =const,
массовая
теплоемкость газа при =const,
![]() ;
;
![]() определяемая
температура, С.
определяемая
температура, С.
![]() температура
из условия задачи, С;
температура
из условия задачи, С;
Массовая теплоемкость c в формуле (1) может быть определена одним из следующих способов:
- по таблице теплоемкостей при 0С, если теплоемкость считать независимой от температуры (таблицы В2-В4 (см. Приложение В));
- из соотношения:
![]() или
или
![]() (2)
(2)
где
![]()
мольная теплоемкость при
мольная теплоемкость при
![]() (таблицы В2-В4 (см. Приложение В));
(таблицы В2-В4 (см. Приложение В));
![]() киломоль
газа,
киломоль
газа,
![]() ,
(например, для кислорода
,
(например, для кислорода![]() (таблица
Б1 (см. Приложение Б));
(таблица
Б1 (см. Приложение Б));
![]() газовая
постоянная,
газовая
постоянная,
![]()
![]() показатель
адиабаты (одноатомные газы: к=1,67;
двухатомные газы: к=1,4; трехатомные и
многоатомные газы: к=1,3)
показатель
адиабаты (одноатомные газы: к=1,67;
двухатомные газы: к=1,4; трехатомные и
многоатомные газы: к=1,3)
Величина постоянной R в формуле (2) определяется либо по табличным данным (таблица Б1 (см. Приложение Б)), либо по формуле:
![]() ,
(3)
,
(3)
где
![]()
универсальная газовая постоянная,
универсальная газовая постоянная,
![]() ;
;
Например, для кислорода газовая постоянная составит
![]()
![]()
Значение массовой теплоемкости c в соответствии с формулой (2) можно на примере кислорода О2 составит:
![]()
Показатель политропного процесса определяется из формулы:
![]() ,
(4)
,
(4)
Отсюда:
![]() ,
(5)
,
(5)
где
![]()
работа, затраченная на сжатие (
работа, затраченная на сжатие (![]() ),
),![]() (значение
(значение![]() дано
в условиях задачи);
дано
в условиях задачи);
![]() показатель
политропного процесса.
показатель
политропного процесса.
Давление
![]() в начале процесса сжатия определяется
из формулы:
в начале процесса сжатия определяется
из формулы:
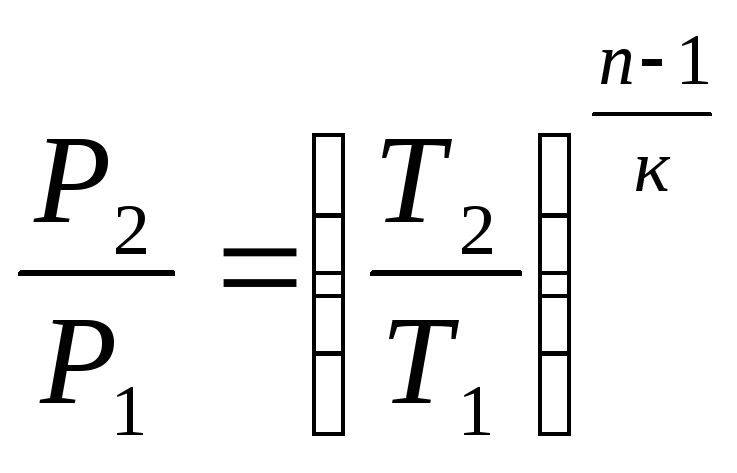 (6)
(6)
Отсюда:
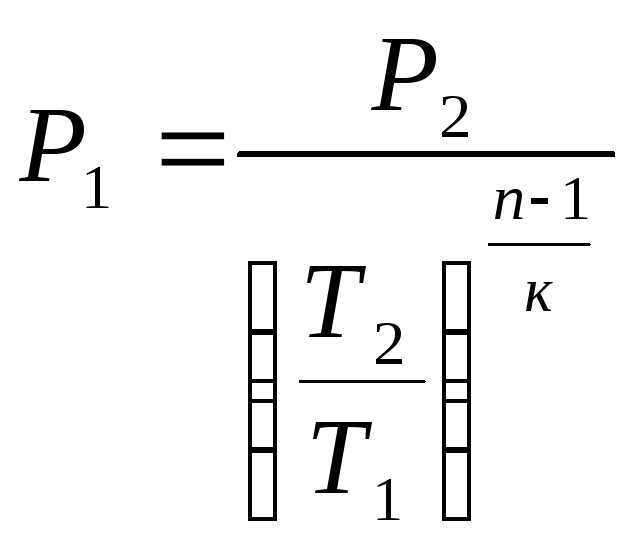 ,
(7)
,
(7)
где
![]()
давление в конце процесса,
давление в конце процесса,
![]() (дано в условии задачи);
(дано в условии задачи);
![]() температура,
температура,
![]()
Начальный и конечный удельный объем определяется из уравнения состояния вида:
![]() и
и
![]() (8)
(8)
Изменение энтропии (s, Дж/кг.К) и энтальпии (h, Дж/кг) определяется соответственно по формулам:
![]() ,
(9)
,
(9)
![]() ,
(10)
,
(10)
где
![]()
массовая теплоемкость газа при постоянном
давлении,
массовая теплоемкость газа при постоянном
давлении,
![]()
Оценить правильность расчетов следует с применением первого закона термодинамики:
![]() ,
(11)
,
(11)
где
![]()
удельная теплота политропного процесса,
удельная теплота политропного процесса,
![]()
Графическое
изображение процесса в
![]() и
и![]() - диаграммах выполняется в масштабе на
миллиметровой бумаге с учетом рекомендаций.
- диаграммах выполняется в масштабе на
миллиметровой бумаге с учетом рекомендаций.
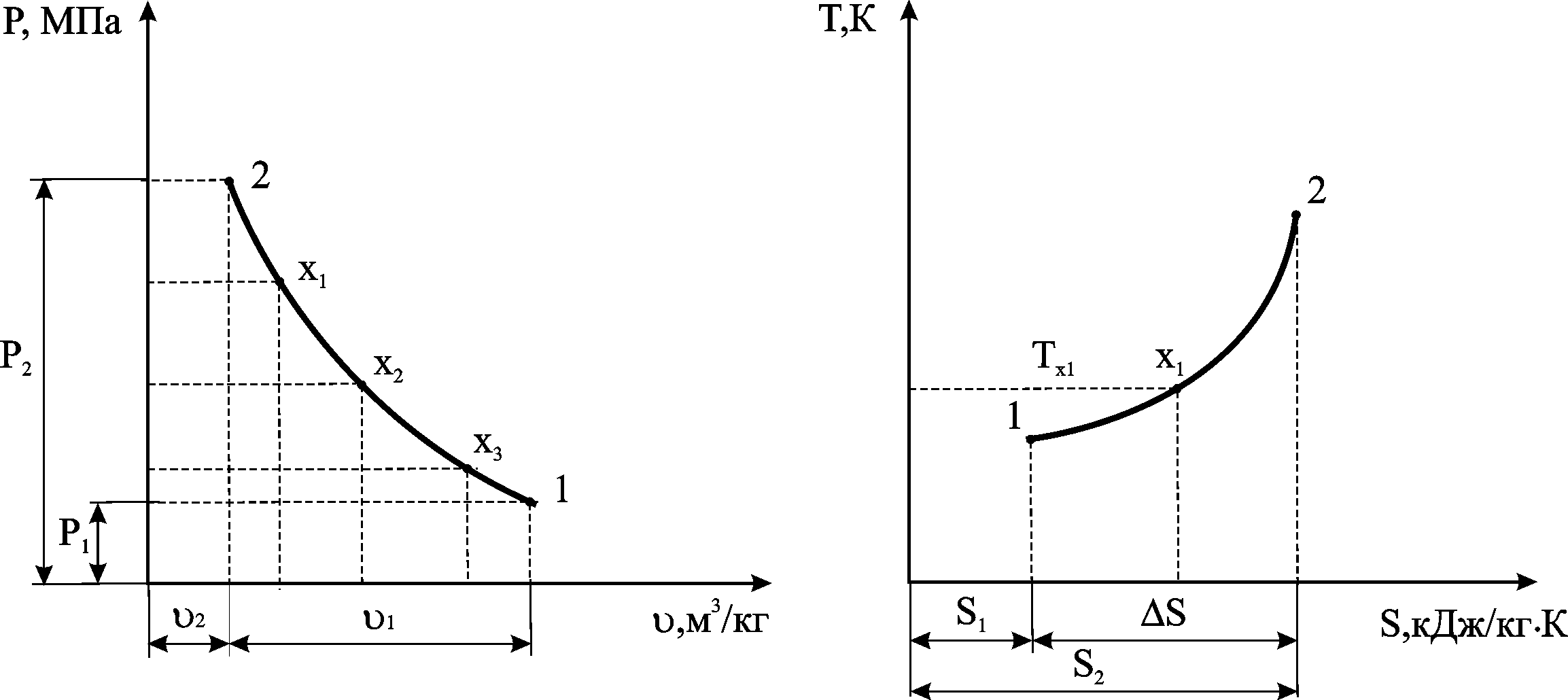
Рисунок
1 - Рекомендации по построению процессов
в
![]() и
и![]() - диаграммах
- диаграммах
Промежуточные
точки для
![]() - диаграммы определяются из уравнения
политропы:
- диаграммы определяются из уравнения
политропы:
![]() ,
(12)
,
(12)
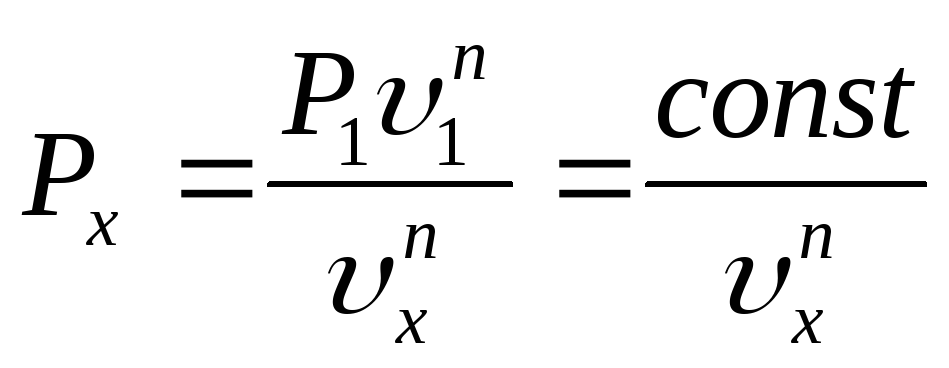 ,
(13)
,
(13)
где
![]() произвольные
значения удельного объема в пределах
от
произвольные
значения удельного объема в пределах
от
![]() до
до![]() ,
,![]()
Для
построения процесса в
![]() -
диаграмме можно принять
-
диаграмме можно принять![]() или определить по формуле:
или определить по формуле:
![]() ,
(14)
,
(14)
где
![]() и
и![]()
параметры температуры и давления,
определяемые при начальных физических
условиях (НФУ) (принимаются To=273,15К,
Po=760
мм.рт.ст.)
параметры температуры и давления,
определяемые при начальных физических
условиях (НФУ) (принимаются To=273,15К,
Po=760
мм.рт.ст.)
Тогда:
![]() ,
(15)
,
(15)
![]() ,
(16)
,
(16)
где
![]()
произвольно взятая промежуточная
температура между точками
произвольно взятая промежуточная
температура между точками
![]() и
и![]() ,
К
,
К
Данный
характер кривой справедлив для случая,
когда
![]()
![]() .
.
