
Чернов Влияние легирования 2007
.pdf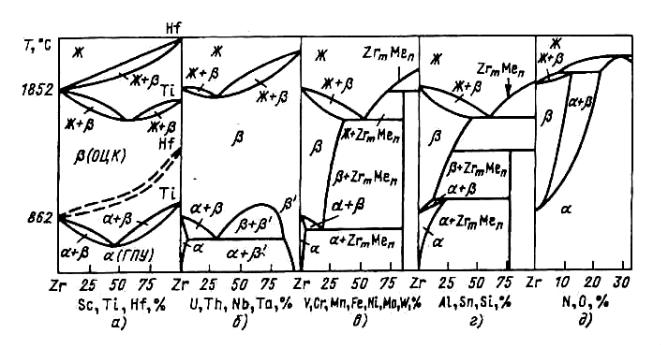
Рис. 2.1. Типы двойных диаграмм состояния сплавов циркония с переходными металлами (а−в) и элементами главных подгрупп (г, д) (по оси абсцисс указано атомное содержание элементов)
Из других соседей − тугоплавких металлов Va- и VIaподгрупп, имеющих ОЦК решетку, неограниченно растворимы в изоморфной им β-фазе циркония лишь Nb, Та, Th и U, атомные радиусы которых отличаются от атомного радиуса циркония не более чем на 10 %; остальные тугоплавкие металлы, для которых это различие составляет 12−17 %, ограниченно растворимы как в α-, так и в β-модификациях циркония. Растворимость более 10 % в α-Zr имеют только А1, N и О, а в β-Zr − 15 химических элементов, среди которых V, Мо, Sn, Mn и алюминий. Растворимость более 1 % в α-Zr имеют Y, Fе, В, Sn, Bi и другие элементы, а менее 1 % − Be, V, Та, Cr, Mo, W, Ni, Cu, Si и др. По мере изменения растворимости тип диаграмм состояния изменяется от сравнительно простого − с монотектоидом (для Nb и Та) − до более сложного, характеризующегося наличием эвтектики, эвтектоида и промежуточных соединений, та-
ких, как V2Zr, Cr2Zr, Mo2Zr, W2Zr (см. рис. 2.1, б и в). Диаграммы состояния последнего типа характерны и для большинства других переходных металлов: Mn, Re, Fe, Co, Ni, у которых атомный радиус меньше, чем у циркония, на 15−25 %.
Элементы главных подгрупп III и VI групп Периодической системы образуют с Zr диаграммы состояния либо перитектоидного типа (см. рис. 2.1, г), либо перитектического типа (см. рис. 2.1, д). Эти диаграммы характеризуются повышением температуры полиморфного превращения Zr и наличием большого числа промежуточных фаз. Например, в системе Zr−Al девять таких фаз. Цирконий образует соединения более чем с 20 химическими элементами, включая имеющие значения с точки зрения легирования: А1, Fe, В,
С, Sn, Be, V, Cr, Mo, Mn, Ni, Cu, Si.
Легирование повышает прочностные свойства циркония как при нормальной, так и при высокой температуре, и получение циркониевых сплавов, обладающих достаточной прочностью, не представляет особо сложной задачи (рис. 2.2). Упрочняющие элементы располагаются по эффективности своего действия в следующем по-
рядке (убывания): W, Та, Мо, Nb, Сг, Al, Sn, Fe, Ti при 20 °С и W,
Мо, Та, Nb, Cr, Fe, A1, Sn, Ti при 500 °С. Поскольку образцы перед механическими испытаниями подвергались закалке и отпуску, то упрочнение во всех случаях, представленных на рис. 2.2, достигнуто
12

за счет дисперсных интерметаллических соединений, за исключением Ti, образующего непрерывный ряд твердых растворов с Zr (см. рис. 2.1, а) и поэтому лишь слабо упрочняющего его. То обстоятельство, что тугоплавкие W, Та, Мо и Nb упрочняют α-фазу циркония наиболее сильно, можно объяснить их сравнительно большим атомным радиусом, в силу чего диффузионная подвижность мала и образуемые ими интерметаллические фазы долго сохраняют дисперсность. Элементы Cr, A1, Sn и Fe имеют меньший атомный радиус, более подвижны в Zr, и поэтому их интерметаллические соединения легче коагулируют и упрочнение менее выражено.
Рис. 2.2. Механические свойства сплавов системы Zr−Nb: а − холоднокатанный лист, отожженный в вакууме при 750 °С, 1,5 ч (температура испы-
тания Тисп = 20 °С); б − закалка из β-области + отпуск при 500 °С, 24 ч (Тисп = 500 °С )
Превращение β → α в чистом Zr, как указывалось выше, происходит бездиффузионным путем с большой скоростью, и зафиксировать β-фазу при комнатной температуре даже при больших скоростях охлаждения не удается. Температура превращения β → α снижается в зависимости от скорости охлаждения (на 10−100 °С при
3000−10 000 град/с).
13
В присутствии небольшого количества неметаллических или металлических примесей (десятые доли процента) образуются игольчатые структуры α-фазы (обычно обозначаемые α′-фазами), служащие критерием мартенситного превращения.
Зафиксировать β-модификацию Zr при комнатной температуре можно только путем легирования значительным количеством β- стабилизирующих элементов, обладающих большой растворимостью в β-Zr и параметром решетки, близким к параметру решетки β- Zr. К таким элементам относятся Nb, Мо, Та. При введении в сплав относительно небольших количеств указанных элементов или некоторых других (например Fe, Re) закаленные из β-области сплавы приобретают структуру метастабильной ω-фазы, являющейся переходной между β- и α-фазами. Метастабильная ω-фаза имеет гексагональную кристаллическую решетку.
Старение циркониевых сплавов, имеющих метастабильные β- и ω-фазы, при температуре 250−600 °С приводит к структурным преобразованиям, в результате которых возможно их превращение в α-фазу. Процесс этот сложен и может осуществляться путем превращения как β → α, так и β → ω → α. При известных условиях возможно только частичное преобразование структуры β→ω. Если указанные превращения протекают не до конца, то образуются гетерогенные структуры, обычно обладающие более высокими прочностными характеристиками.
Среди элементов Vа группы только Nb может рассматриваться в качестве легирующего элемента, так как ванадий даже в малых количествах усиливает коррозию циркония; тантал имеет высокое сечение захвата тепловых нейтронов. В VIа группе могут быть использованы Cr и Mo с относительно небольшими σа, а у W большое сечение захвата нейтронов. Из элементов VIII группы только Fe привлекает внимание, так как Ni способствует поглощению цирконием водорода.
Таким образом, Nb почти единственный элемент из V, VI и VIII групп, подходящий для легирования циркония применительно к водяному и пароводяному теплоносителю для использования до
300−350 °С.
14
Ниобий, как легирующий элемент в цирконии, обладает следующими положительными свойствами:
1) сечение захвата тепловых нейтронов небольшое (1,1 10-28 м2), и он может быть добавлен в количестве нескольких процентов без существенного повышения σа;
2)стабилизирует коррозионную стойкость нелегированного циркония, т. е. устраняет вредное влияние малых количеств таких примесей, как углерод, алюминий, титан, имеющихся в реактор- но-чистом цирконии;
3)эффективно снижает долю водорода, поглощаемую циркониевым сплавом;
4)образует с β-фазой циркония ряд твердых растворов, что объясняется одинаковыми кристаллическими решетками и очень
близкими атомными радиусами; в α-фазе ниобий растворяется при монотектоидной температуре в количестве до (1−1,1) % (по другим данным − до 1,5 %).
Реакторные циркониевые сплавы циркалой изготавливаются на основе загрязненного губчатого Zr, поэтому стоит задача повышения их коррозионной стойкости (основой отечественных сплавов является чистый иодидный Zr, и такой острой проблемы нет). Поэтому для парализации вредного действия примесей, в первую очередь − азота, наиболее логично использование для легирования элементов IV группы. В этой группе кроме Sn ни один элемент не может быть использован для легирования циркония: Ti резко снижает коррозионную стойкость; Hf имеет очень высокое значение σа; Pb летуч и усиливает коррозию; атомные радиусы Si и Ge сильно отличаются от радиуса атома Zr и они практически нерастворимы как в
α-, так и β-Zr.
На рис. 2.3 и 2.4 представлены диаграммы состояний наиболее важных систем Zr−Nb и Zr−Sn, нашедших широкое применение в реакторостроении. Первая является базовой для отечественных реакторных циркониевых сплавов, а вторая − для сплавов, используемых в США и применяемых в активной зоне реакторов на тепловых нейтронах (ВВЭР, РБМК, BWR, PWR).
15

Рис. 2.3. Диаграмма состояния системы Zr−Nb
Рис. 2.4. Диаграмма состояния системы Zr−Sn
16
Ниобий снижает температуру α'β превращения (см. рис. 2.3). Максимальная растворимость Nb в α-Zr составляет 1 % (разные исследователи приводят данные с разбросом от 0,6 до 1,7 % Nb, что определяется чистотой циркония и методами исследования). Система Zr−Nb характеризуется непрерывной взаимной растворимостью при высоких температурах в жидком и твердом (β-фаза) состояниях. На кривой ликвидуса существует минимум при 1740 °С и около 21,7 ат. % Nb. При понижении температуры происходит расслоение твердого раствора β на два: βZr и βNb, представляющие собой соответственно твердый раствор Nb в β-Zr и твердый раствор β-Zr в ниобии. Вершина купола расслоения соответствует примерно 988 °С и 60,6 ат. % Nb. Монотектоидная реакция βZr ' βNb + α протекает при 610 °С (620 °С по другим данным). Загрязнение сплавов системы примесями О2 и N2 стабилизирует α-фазу при температурах выше монотектоидной и расширяет двухфазную βZr + βNb-область.
Олово повышает температуру α'β превращения (см. рис. 2.4). Максимальная растворимость Sn в α-Zr составляет 9 %, в β-Zr − около 21 %. Система Zr−Sn характеризуется наличием соединения Zr4Sn и, возможно, еще двух соединений: Zr5Sn3 и ZrSn. Соединение Zr4Sn образуется в твердом состоянии по перетектоидной реакция при 1140 °С. Максимальная растворимость Sn в β-Zr достигает около 21 %, а в α-Zr − 9 % при температуре 980 °С и существенно снижается с уменьшением температуры − при 300−350 °С (рабочая температура в активной зоне реакторов на тепловых нейтронах) его растворимость в α-Zr ничтожна. В интересующем «циркониевом угле» диаграммы при температурах от комнатной до рабочих присутствует лишь одна интерметаллидная упрочняющая фаза − Zr4Sn.
Вследствие относительно низкой температуры эвтектоидного превращения в системе Zr−Nb (см. рис. 2.3) при охлаждении из области β-фазы возникают неравновесные структуры. Обобщая данные по сплавам Zr−Nb после закалки, можно отметить следующие концентрационные зависимости образования метастабильных фаз: от 0 до 3−5 % Nb − α′-фаза (пересыщенный твердый раствор Nb в α- Zr), имеющая ГПУ кристаллическую решетку; от 5−7 до 14−15 % Nb − β + ω; свыше 14−15 % Nb − метастабильная β-фаза.
17

Однако при закалке из α + β-области в образцах может произойти β → ω-превращение и в сплавах с меньшей концентрацией Nb (например, сплав Zr + 2,5 % Nb), обусловленное перераспределением Nb между α и β составляющими структуры в процессе выдержки при температуре, соответствующей двухфазной области, и возникновением участков, обогащенных ниобием, в которых и осуществляется β → ω-превращение. Таким образом, в зависимости от условий гомогенизации в двухфазной α + β-области и скорости охлаждения, в структуре сплава могут присутствовать α-, α′-, ω-фазы и даже остатки β-фазы, если последняя обогатится ниобием в процессе предварительной гомогенизации в α + β-области.
В сплавах с содержанием Nb менее 5 % при отпуске происходит распад пересыщенного твердого раствора α′, и в соответствии с равновесной диаграммой состояния (см. рис. 2.3) выделяется богатая ниобием фаза βNb с ОЦК решеткой: α′ → α + βNb. Частицы гомогенно выделяющейся βNb-фазы имеют форму тонких удлиненных пластинок.
Метастабильная ω-фаза при отпуске превращается в стабиль-
ные α- и βNb -фазы по схеме
ωзакал → ωотп (обедненная) + βZr (обогащенная). $ α + βNb
Максимальное количество ω-фазы, образующейся при закалке в результате превращения β → β + ω, наблюдается в сплавах при содержании Nb около 8 %, что подтверждается скачком твердости (рис. 2.5). Сама ω-фаза имеет высокую твердость (HV ≈ 4300 МПа).
Рис. 2.5. Твердость закаленных сплавов Zr−Nb
18

В результате легирования циркония ниобием упрочнение при кратковременных испытаниях при температуре 20 °С достигает максимума при концентрациях 3−8 % Nb; при 500 °С максимальное упрочнение наблюдается в сплавах с 3−5 % Nb (см. рис. 2.2). Возрастание прочности малолегированных сплавов при нормальной температуре обусловлено мартенситным превращением β → α′, а при более высокой концентрации Nb − в ω-фазу. С дальнейшим увеличением содержания Nb фиксируется все большее количество мягкой β- фазы и прочность снижается.
Существенным является то, что повышение прочности сплавов сопровождается значительным снижением пластичности; особо низкую пластичность имеют сплавы, имеющие в структуре ω-фазу
(см. рис. 2.2).
При длительных испытаниях жаропрочные характеристики сплавов циркония с ниобием имеют сложную зависимость от состава (рис. 2.6). Минимальной скоростью ползучести при 400−500 °С обладают сплавы с 3−5 % Nb (сплавы мартенcитного класса, у которых растворимость ниобия в α-Zr превышает предельную). Повышение длительной прочности у отпущенных сплавов связано с наличием гетерогенной структуры, состоящей из α-твердого раствора с включениями дисперсных частиц β-Nb.
Рис. 2.6. Скорость ползучести (за 100 ч) сплавов системы Zr−Nb (закалка из β-области + отпуск при 500 °С, 24 ч)
при разных значениях температуры и приложенного напряжения
19

Анализ механических свойств и жаропрочности (см. рис. 2.2 и 2.6) сплавов системы Zr−Nb показывает, что они должны содержать не более 3 % Nb для обеспечения прочности и жаропрочности при сохранении достаточной пластичности (сплавы Э110 и Э125).
Рис. 2.7. Механические свойства сплавов системы Zr−Sn: а − холоднокатанный лист, отожженный в вакууме при 750 °С в течение 1,5 ч
(Тисп = 20 °С); б − закалка из β-области + отпуск при 500 °С в течение 24 ч (Тисп = 500 °С)
Повышение прочности и соответствующее снижение пластичности в сплавах системы Zr−Sn обусловлены наличием гетерогенной структуры − металлической α-матрицы и интерметаллидного соединения Zr4Sn. Объемная доля интерметаллида возрастает по мере увеличения концентрации олова. В этой системе, как следует из рис. 2.7, наблюдаются более низкие значения кратковременной
20
