
- •Предисловие
- •Введение
- •1 Предмет курса "поверхностные явления
- •2 Классификация поверхностных явлений
- •3 Дисперсность, удельная поверхность
- •4 Классификация дисперсных систем
- •4.1 Классификация дисперсных систем по размерам частиц дисперсной фазы
- •4. 2 Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •4.3 Классификация по интенсивности взаимодействия дисперсной фазы и дисперсионной среды
- •4.4 Классификация по интенсивности взаимодействия
- •5 Поверхностные явления на границе раздела фаз
- •5.1 Поверхностная энергия, поверхностное натяжение
- •5.2 Термодинамика поверхности раздела фаз
- •5.3 Пути понижения энергии Гиббса на границе раздела фаз
- •5.4 Когезия. Работа когезии
- •5.5 Адгезия, работа адгезии, термодинамические основы адгезии
- •5.6 Смачивание, краевой угол смачивания, теплота смачивания, гидрофилизация и гидрофобизация поверхностей.
- •5.7 Растекание, критерий растекания, поверхностные пленки, двумерный газ
- •5.8 Адсорбция
- •5.8.1 Общие положения, классификация изотерм адсорбции
- •5.8.2 Фундаментальное термодинамическое уравнение адсорбции Гиббса
- •5.8.3 Адсорбция газов и паров на поверхности твердых тел
- •5.8.4 Уравнение адсорбции Фрейндлиха. Его анализ и решение
- •5.8.5 Мономолекулярная теория (теория Ленгмюра)
- •5.8.6 Полимолекулярная теория (теория Поляни)
- •5.8.7 Теория полимолекулярной адсорбции бэт
- •Пористые адсорбенты, классификация пористых тел по Дубинину
- •5.8.10 Влияние природы и структуры адсорбента, природы и свойств газов и паров на адсорбцию. Адсорбция из смеси газов.
- •5.9 Адсорбция из раствора на границе с газом
- •5.8.10.1. Молекулярная адсорбция
- •5.8.11.2. Ионная адсорбция (адсорбция электролитов)
- •5.8.12 Ионобменная адсорбция
5.8.2 Фундаментальное термодинамическое уравнение адсорбции Гиббса
Процесс адсорбции приводит к понижению поверхностной энергии. Запишем объединенное уравнение первого и второго законов термодинамики для внутренней энергии поверхности раздела фаз:
dU = TdS+ σds + Σμidni
Это уравнение является дифференциальной формой объединенного уравнения первого и второго законов термодинамики
U= ST + σs + Σμini
Запишем полный дифференциал этой функции состояния системы
dU = TdS + σds + Σμidni + SdT + sdσ + Σnidμi .
Приравняем выражения, полученные для dU. После преобразованийполучим:
SdT + sdσ + Σnidμi =0
При Т = const величина dT = 0 и sdσ + Σnidμi =0
Разделим обе части уравнения на величину площади s:
dσ = Σnidμi /s = ΣГidμi , (V.18)
где Гi = ni /s – величина гиббсовской адсорбции, под которой понимают избыток вещества в поверхностном слое по сравнению с объемом фазы. Единицы измерения гиббсовской адсорбции [кмоль/м2] .
Таким образом, адсорбционное уравнение Гиббса - это термодинамически строгое соотношение, которое описывает адсорбцию на любой границе раздела фаз.
5.8.3 Адсорбция газов и паров на поверхности твердых тел
Поверхность твердых тел по сравнению с идеально гладкой поверхностью жидкости энергетически неравноценна. Наличие неровностей на поверхности, пор и капилляров не позволяет непосредственно замерить удельную поверхность адсорбента. Поэтому величину адсорбции определяют в расчете на массу адсорбента (т.е. A и V), а изотермы адсорбции газов на твердом теле строят в координатах A - P или V – P (рис. V.10, V.11).
Адсорбция газов на твердой поверхности настолько сложна, что изотермы адсорбции имеют различный вид (рис. V.10, V.11), а для их описания исторически сложилось два направления: мономолекулярная и полимолекулярная теории адсорбции.
5.8.4 Уравнение адсорбции Фрейндлиха. Его анализ и решение
Для описания 1 типа изотерм адсорбции было предложено эмпирическое уравнение Фрейндлиха.
А = kP1/n или А = kC1/n, (V.19)
где А - величина адсорбции;
Р и С – равновесное давление или концентрация;
k и 1/n – постоянные величины.
Это уравнение описывает только часть изотермы адсорбции, соответствующей области средних величин давлений или концентрации. Действительно, при Р 0 для описания первого прямолинейного участка изотермы 1/n должна изменяться и приближаться к 1. Уравнение должно перейти в уравнение Генри А = kP. При Р→ ∞ величина 1/n должна изменяться и приближаться к 0, т.е А = Р. Для полного описания изотермы величина 1/n должна быть переменной и зависеть от значения Р. Поскольку величина 1/n принимается постоянной величиной, то уравнение пригодно только для описания изотермы адсорбции в области средних давлений.
Для решения уравнение переводят в логарифмическую форму:
![]() .
(V.19а)
.
(V.19а)
Это уравнение прямой, не проходящей через начало координат y=b+ax. Его решают (то есть определяют постоянные k и 1/n) либо через систему уравнений, либо графическим способом. При графическом способе на основании экспериментальных данных строят график в координатах lgA =f(lgP) (рисV.14).
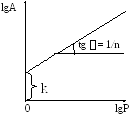
Рисунок
V.14
- Решение уравнения Фрейндлиха
Тангенс угла наклона прямой равен 1/n , а на оси ординат отсекается отрезок, равный величине lg k.
В области низких давлений первый прямолинейный участок изотермы адсорбции описывается уравнением Генри
А = kР
