
- •Предисловие
- •Введение
- •1 Предмет курса "поверхностные явления
- •2 Классификация поверхностных явлений
- •3 Дисперсность, удельная поверхность
- •4 Классификация дисперсных систем
- •4.1 Классификация дисперсных систем по размерам частиц дисперсной фазы
- •4. 2 Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •4.3 Классификация по интенсивности взаимодействия дисперсной фазы и дисперсионной среды
- •4.4 Классификация по интенсивности взаимодействия
- •5 Поверхностные явления на границе раздела фаз
- •5.1 Поверхностная энергия, поверхностное натяжение
- •5.2 Термодинамика поверхности раздела фаз
- •5.3 Пути понижения энергии Гиббса на границе раздела фаз
- •5.4 Когезия. Работа когезии
- •5.5 Адгезия, работа адгезии, термодинамические основы адгезии
- •5.6 Смачивание, краевой угол смачивания, теплота смачивания, гидрофилизация и гидрофобизация поверхностей.
- •5.7 Растекание, критерий растекания, поверхностные пленки, двумерный газ
- •5.8 Адсорбция
- •5.8.1 Общие положения, классификация изотерм адсорбции
- •5.8.2 Фундаментальное термодинамическое уравнение адсорбции Гиббса
- •5.8.3 Адсорбция газов и паров на поверхности твердых тел
- •5.8.4 Уравнение адсорбции Фрейндлиха. Его анализ и решение
- •5.8.5 Мономолекулярная теория (теория Ленгмюра)
- •5.8.6 Полимолекулярная теория (теория Поляни)
- •5.8.7 Теория полимолекулярной адсорбции бэт
- •Пористые адсорбенты, классификация пористых тел по Дубинину
- •5.8.10 Влияние природы и структуры адсорбента, природы и свойств газов и паров на адсорбцию. Адсорбция из смеси газов.
- •5.9 Адсорбция из раствора на границе с газом
- •5.8.10.1. Молекулярная адсорбция
- •5.8.11.2. Ионная адсорбция (адсорбция электролитов)
- •5.8.12 Ионобменная адсорбция
5.2 Термодинамика поверхности раздела фаз
Процесс увеличения площади поверхности при постоянном объеме фазы выводит молекулы из объема фазы в поверхностный слой. При этом совершается работа против сил межмолекулярного сцепления. Эта работа в изотермических условиях равна увеличению свободной поверхностной энергии системы (ΔGs):
- W = ΔGs.
В результате на границе раздела фаз появляется избыток (сгущение) свободной энергии. Этот вывод об увеличении свободной энергии с увеличением границы раздела фаз можно обобщить для любой границы раздела фаз: твердое тело – газ, твердое тело – жидкость, жидкость - газ, жидкость – жидкость.
Разделяющая сосуществующие фазы поверхность S называется поверхностью раздела фаз и представляет собой тонкий слой конечной толщины δ (рис. V.4), в пределах которого свойства вещества отличаются от свойств вещества в объеме фазы.
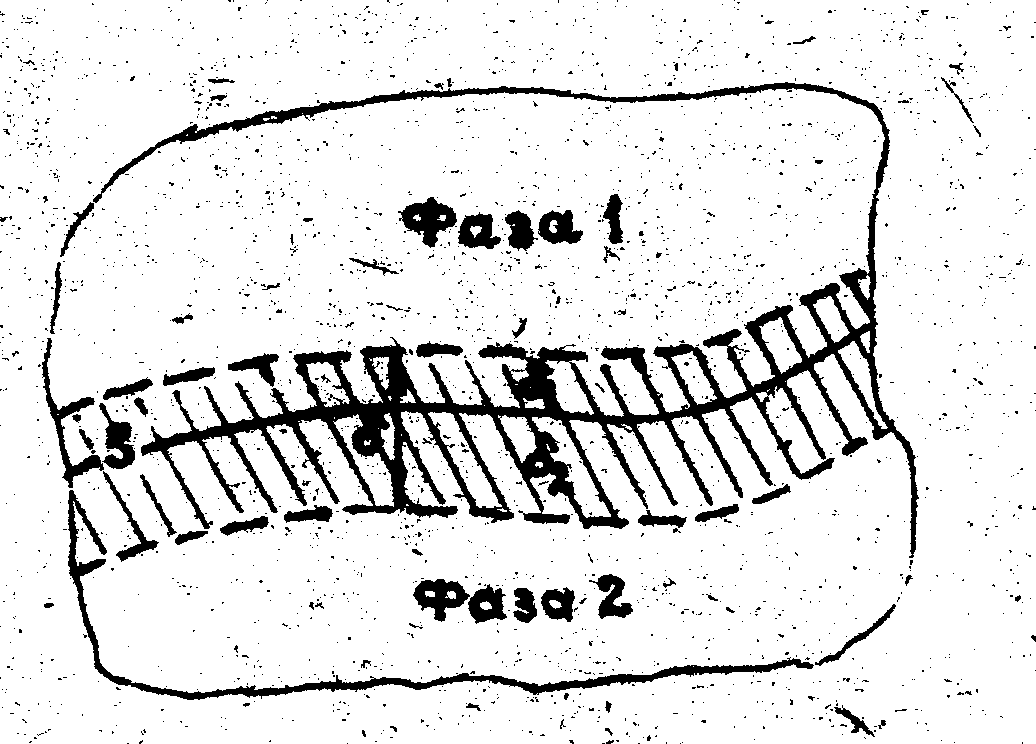
Рисунок V.4 - Поверхность раздела фаз
Это значит, что влияние соседней фазы распространяется не на все вещество, а только на тонкий слой толщиной всего несколько молекул. Именно в этом слое и сосредоточен весь избыток свободной поверхностной энергии. Толщину δ определить трудно, поэтому для описания термодинамического состояния системы часто используют метод избыточных термодинамических величин Гиббса. Гиббс называет поверхностный слой поверхностью разрыва. Это неоднородный тонкий слой, разделяющий объемные фазы и имеющий конечную толщину и объем. Избыточные свойства относятся к поверхности, не имеющей толщины. Они могут иметь знаки “+ “ и “ - ”. Слой имеет избыток массы, энтальпии, энтропии, но не имеет избытка объема. Под избытком экстенсивных свойств Гиббс понимал разницу между величиной свойства в данной объемной фазе и значением того же свойства в реальной системе в поверхностном слое. Поверхностный избыток свойства – это разность между экстенсивными величинами в реальной и идеализированной системах.
Внутренняя энергия поверхностного слоя по этому методу запишется следующим образом:
US = U – (UI +UII),
в то время как полная внутренняя энергия системы-
U = UI +UII + US.
В этих выражениях U – внутренняя энергия реальной системы, UI +UII – внутренняя энергия идеализированной системы, которая равна сумме внутренних энергий двух объемных фаз, US – поверхностный избыток.
Такие же выражения можно записать для других термодинамических функций: энтальпии, энтропии, свободной энергии Гельмгольца и Гиббса и т.д.
Процессы на межфазной поверхности выражаются уравнением
dUS = TdSS+ σds + ΣμidniS .
В этом выражении слагаемое ΣμidniS – отражает химическую работу по изменению состава поверхностного слоя, а слагаемое σds – механическую работу по созданию поверхностного слоя, TdSS –тепловой эффект образования поверхностного слоя. Различие в знаках слагаемых, выражающих механическую работу в выражениях для объемных фаз и поверхности раздела связано с тем, что совершаемая над системой механическая работа приводит в объемных фазах к уменьшению объема V, а в поверхностном слое – к увеличению поверхности раздела фаз s (ds > 0).
С учетом этого объединенное уравнение первого и второго законов термодинамики для любой гетерогенной двухфазной системы имеет вид:
dU = dUI + dUII + dUS =
= TdSI – PdVI + ΣμidniI + TdSII – PdVII + ΣμidniII + TdSS + σds + ΣμidniS .
Аналогично можно также записать:
dНS = - TdSS+ σds + ΣμidniS ;
dGS = - SSdT+ σds + ΣμidniS ;
dFS = - SSdT+ σds + ΣμidniS .
При этом в состоянии равновесия по Гиббсу
ТI = TII = TS ; μiI =μiII = μis .
Из этих выражений следует, что коэффициент σ можно выразить как через различные термодинамические функции системы:
σ = (∂F/∂s)V,T.n = (∂G /∂s)P,T.n = (∂U/∂s)V,S.n = (∂H /∂s)P,S.n , (V.3)
так и термодинамические функции поверхностного слоя:
σ = (∂FS/∂s)V,T,.n = (∂GS /∂s)P,T,.n = (∂US/∂s)V,,S.,n = (∂HS /∂s)P,S,.n . (V.4)
Следовательно, по физическому смыслу величина поверхностного натяжения σ соответствует запасу свободной поверхностной энергии единицы поверхности раздела фаз. Для границы жидкость – газ свободная поверхностная энергия единицы поверхности равна силе, отнесенной к единице длины.
