
Карцев В.Г.Избранные методы с-за и модифик. гетероциклов т.1 , 2003
.pdf
|
|
|
|
|
|
Схема 3 |
|
|
|
|
O |
NHAlk |
|
|
|
|
|
|
|
|
|
|
|
|
S |
X |
9 |
|
|
|
|
|
|
|
|
|
|
|
O |
NHAr |
|
|
|
|
|
|
|
|
O |
OH |
O |
Cl |
|
X |
10 |
|
|
S |
||||
|
|
|
|
|
|
|
|
X |
|
X |
O |
N3 |
|
|
S |
|
|
|||
S |
|
|
|
|||
|
|
|
|
|||
7 |
|
8 |
|
|
X |
11 |
|
|
|
|
S |
||
|
|
|
|
|
|
|
|
|
|
|
O |
|
OMe |
|
X = H, Br |
|
|
S |
X |
12 |
|
|
|
|
|
||
Мы попытались осуществить внутримолекулярную циклизацию соединения 12 (Х = Br) взаимодействием его с Bu3SnH по методике [8]. Однако, вместо ожидаемого гетероцикла 13 был выделен только продукт восстановительного дегалогенирования 14 (схема 4).
|
|
|
|
Схема 4 |
|
|
|
O |
OMe |
|
O |
OMe |
H |
|
|
|
|
S |
|
|
|
Bu3SnH |
14 |
|
H |
Br |
O |
|
|
толуол |
|
|||
|
S |
|
|
|
|
12 |
т.кип. |
|
|
|
|
H |
|
|
|
|
|
OMe |
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
13 |
|
Аналогично протекает реакция и для анилида 15 (R = Br) (схема 5). Вероятно, |
||||
для получения продуктов 16 необходимо применять реакцию Пшорра. |
|
|||
Генеральный спонсор и организатор – InterBioScreen Ltd. |
377 |
|||


Интересно протекает реакция изоцианата 19 с дигидроизохинолином 26: продукт монокарбамоилирования 28 можно получить только при проведении реакции в кипящем ксилоле. При комнатной температуре образуется только продукт дикарбамоилирования 27, как это отмечалось в [8] (схема 8).
Схема 8
|
|
|
NCO |
|
|
|
N |
+ 2 |
H |
S |
|
NH |
|
|
|
|
|
|||
|
|
|
H |
H |
H |
|
|
|
|
H |
|||
|
|
|
|
N |
N |
|
|
|
|
S |
|
O O |
S |
26 |
|
19 |
|
|
27 |
|
|
130°C |
2 |
|
|
|
|
|
26 |
NH |
|
|
|
|
|
|
|
|
|
||
|
|
|
H |
|
H |
|
|
|
|
N |
|
|
|
O 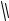 S
S
28
Разумеется, при использовании 2,3,3-триметил-1-метилиден-1,2,3,4-тетрагид- роизохинолина 29 образование продуктов моно- 30 или ди- 31 карбамоилирования зависит только от соотношения реагентов (схема 9).
Схема 9
|
|
|
1 экв. |
|
|
|
|
|
|
N |
|
|
|
NCO |
|
H |
H |
|
|
|
|
N |
|
N |
+ |
H |
30 |
O |
S |
|
S |
|
|||
29 |
|
19 |
2 экв. |
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
H |
H |
|
|
|
|
N |
2 |
|
|
|
|
O |
|
|
|
|
31 |
S |
|
Генеральный спонсор и организатор – InterBioScreen Ltd. |
|
379 |
|||


Литература
1.Гевальд К., ХГС 1976 (10) 1299.
2.Sabnis R.W., Sulfur Reports 1994 16 1.
3.Бабичев Ф.С., Шаранин Ю.А., Литвинов В.П. и др., в кн. Внутримолекулярное взаимодействие нитрильной и С-Н-, О-Н- и S-H-групп, Киев: Наукова думка, 1985, с. 200.
4.Sibor J., Pazdera P., Moleсules 1996 1 157.
5.Хрипак С.М., Добош А.А., Смаланка И.В., Микитчин А.С., ХГС 1973 (3) 326.
6.Шведов В.И., Рыжикова В.К., Гринев А.Н., ХГС 1997 (7) 972.
7.Физер Л., Физер М., Реагенты для органического синтеза, М.: Мир, 1978, с. 515.
8.Бороненкова Е.А., Сыропятов Б.Я., Горбунов А.А. и др., Хим.-фарм. журн.
1994 (8) 18.
9.Колла В.Э., Бердинский И.С., Фармакология и химия производных гидразина,
Йошкар-Ола, 1976, с. 264.
Генеральный спонсор и организатор – InterBioScreen Ltd. |
381 |

|
|
|
|
|
|
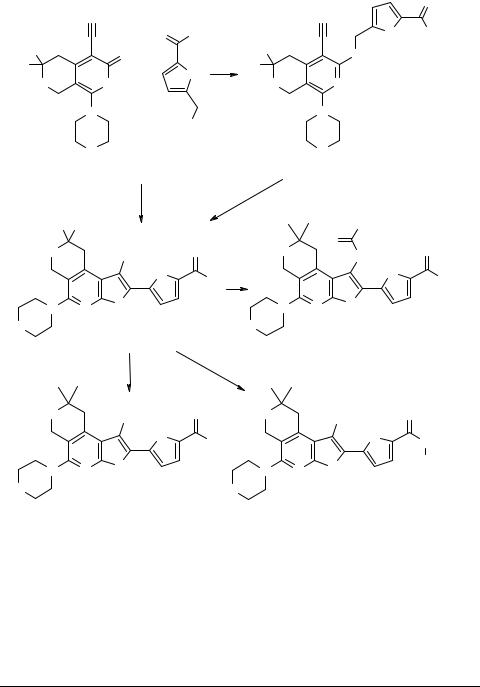
Схема 1 |
N |
|
|
|
|
N |
O |
|
|
|
|
|
||
R |
|
O R' |
|
R |
O |
R' |
S |
|
|
S |
|
||
R |
|
|
R |
|
||
NH + |
O |
|
|
|
||
X |
|
X |
N |
|
||
|
|
|
||||
N |
|
Cl |
|
|
N |
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
1a, b |
|
2 |
|
|
4a, b |
|
R R |
|
|
|
|
R" |
|
X |
NH2 |
O |
|
O |
O |
O |
|
NH |
|||||
|
O |
|
|
|
||
|
|
R' |
|
O |
OMe |
|
|
|
|
|
|
||
N N |
S |
|
|
N |
N S |
|
O |
|
|
|
O |
|
|
3a-j |
|
|
|
|
5a, b |
|
O |
NH2 |
O |
O |
O |
NH2 |
O |
O |
|
|
OH |
|
|
NH |
||
|
|
|
|
|
|
||
N N |
S |
|
|
N N |
S |
|
NH2 |
|
|
|
|
||||
O |
|
|
|
O |
|
|
|
6 |
|
|
|
7 |
|
|
|
1a X = О, R = Me; 1b X = СН2, R = Н; 3а X = О, R = Me, R' = ОMe; 3b X = О, R = Me, R' = ОEt; 3c X = О, R = Me, R' = MeNН;
3d X = О, R = Me, R' = PhNН; 3e X = СН2, R = Н, R' = ОMe; 3f X = СН2, R = Н, R' = ОEt; 3j X = СН2, R = Н, R' = MeNН; 4a X = О, R = Me, R' = ОMe; 4b X = СН2, R = Н, R' = ОMe; 5a R" = Ph; 5b R" = 2-фурил
Генеральный спонсор и организатор – InterBioScreen Ltd. |
383 |


Многоканальные флуоресцентные зонды на основе 3-гидроксифлавонов: дизайн, синтез и применение
Пивоваренко В.Г.
Киевский национальный университет им. Тараса Шевченко Химический факультет 01033, Украина, Киев, ул. Владимирская, 64
Введение
Флуоресцентная спектроскопия находит широкое применение в исследованиях природы и состояния сложных субмолекулярных объектов, таких как мицеллы, липосомы, биологические клетки и их компоненты [1]. По своим аналитическим возможностям она во многом лидирует, позволяя регистрировать излучение одного кванта в объеме менее 1 мкм3, а также фиксировать молекулярные явления в фемтосекундной шкале времени. В исследованиях субмолекулярных объектов часто используются вспомогательные инструменты – флуоресцентные зонды. Флуоресцентный зонд – это молекула, способная при поглощении кванта света оптического диапазона испускать новый квант света. Характеристики излучения подобных молекулярных устройств (его интенсивность, положение и полуширина полосы в спектре и пр.) всегда несут определенную информацию об объекте. Задача исследователя состоит в адекватной интерпретации полученной информации. Однако часто интерпретация информации представляется сложной задачей, поскольку излучение молекулы зонда, как правило, отражает состояние сразу нескольких физических параметров микроокружения. Поэтому к химической архитектуре зонда и его флуоресцентным свойствам существует ряд жестких требований. В частности, важным требованием (если не основным) является экстракция информации об изучаемом параметре микроокружения. Эта задача решается путем фильтрации информации, а также увеличения количества каналов ее получения.
Конструкция и свойства зонда зависят не только от параметров объекта, на измерение которых он настроен, но и от типа прибора, в паре с которым он работает. Наибольшее распространение получили флуоресцентные зонды для стационарной флуориметрии и флуоресцентной микроскопии. По принципу передачи информации такие зонды следует поделить на три группы: флуоресцентные метки, интенсометрические зонды и рациометрические зонды. Флуоресцентные метки (рис. 1а) информируют только о местоположении объекта исследования, о его количестве и/или о его геометрических размерах. В этой связи к ним предъявляют лишь одно важное требование: они должны как можно ярче светиться при контакте с объектом. Яркость свечения определяется высокими значениями молярного коэффициента поглощения и квантового выхода флуоресценции.
Принцип передачи информации интенсометрическими зондами (рис. 1b) состоит в изменении интенсивности флуоресценции. На этом принципе основана
работа большинства современных флуоресцентных зондов для измерения микровязкости, рН, концентрации катионов (Ca2+, Mg2+, Na+, K+, NH4+, Zn2+, Fe3+), либо
анионов (Cl−, PO43−, AcO−), окислителей и множества других молекулярных компонентов клетки более сложного строения [1].
Генеральный спонсор и организатор – InterBioScreen Ltd. |
385 |

