Карцев В.Г.Избранные методы с-за и модифик. гетероциклов т.1 , 2003
.pdf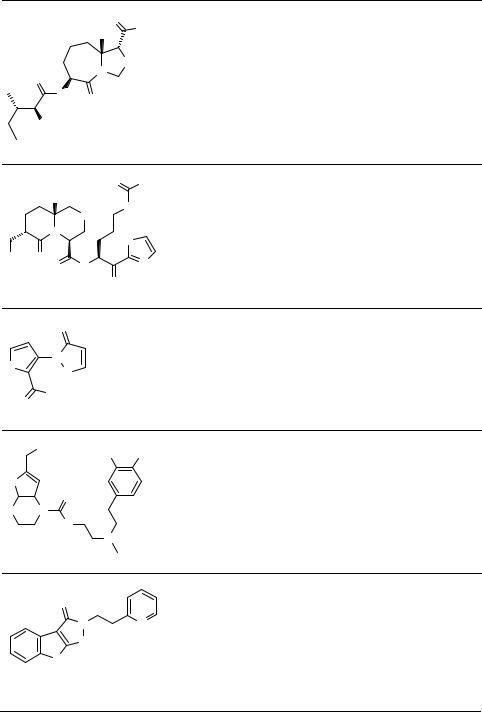
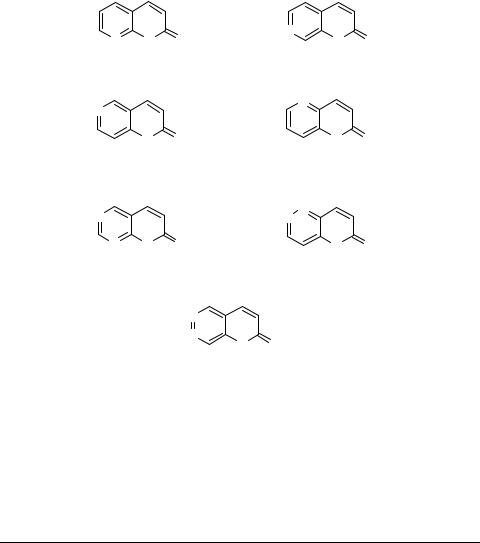
Таблица 1. Продолжение
|
|
|
O |
OH |
Hypotensive, |
ACE-inhibitor, |
ER-32935 |
[16] |
|
|
|
H |
diuretic |
neutral- |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
S |
|
endopeptidase- |
|
|
|
O |
|
N |
|
inhibitor |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
N |
O |
|
|
|
|
|
|
|
H |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
SH |
|
|
|
|
|
|
|
|
|
|
HN |
NH2 |
Anticoagulant |
Thrombin- |
WD-97- |
[17] |
|
H |
|
|
NH |
|
inhibitor |
012035 |
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
Ph |
O O |
N |
|
N |
|
|
|
|
|
|
H |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
Immuno- |
Tyrosine- |
WD-98- |
[18] |
|
|
|
|
|
suppressive |
kinase- |
011590 |
|
S |
N |
|
|
|
|
inhibitor |
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
OMe |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ph |
|
MeO |
OMe |
Cardiovascular, |
Calcium- |
Ho-7 |
[19] |
|
|
|
|
|
inotropic |
antagonist |
|
|
S |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
S |
N |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
H |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
Endocrine-Gen. |
Tyrosine- |
WD-97- |
[20] |
|
|
|
|
|
kinase- |
001705 |
|
|
|
|
|
|
|
|
|
||
|
|
N |
|
N |
|
inhibitor |
|
|
S
S
Генеральный спонсор и организатор – InterBioScreen Ltd. |
277 |
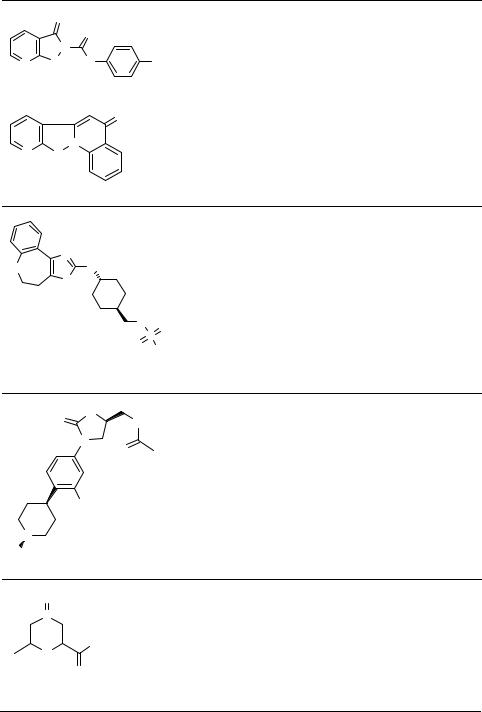
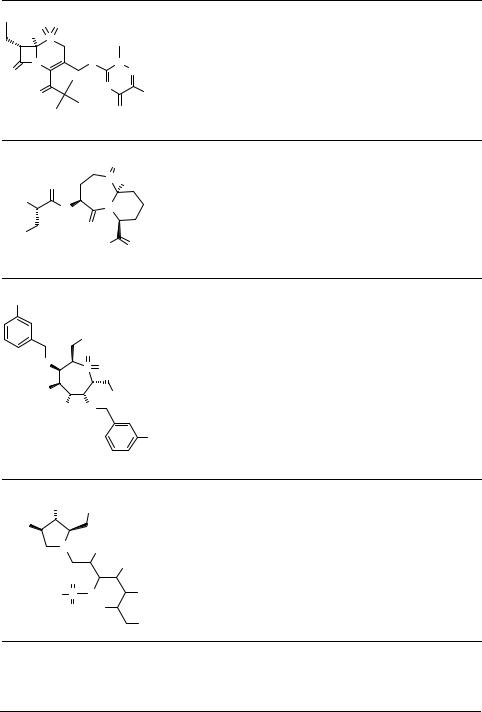
Таблица 1. Продолжение
|
H |
O |
O |
|
|
|
Anti-inflam- |
Elastase- |
PNU- |
[26] |
|
|
S |
|
|
|
matory |
inhibitor |
156575 |
|
|
O |
N |
|
S |
N |
N N |
|
|
|
|
|
|
O |
|
|
|
OH |
|
|
|
||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
Cardiant, |
Vasopepti- |
BMS- |
[27] |
|
|
|
|
O |
|
S |
H |
hypotensive |
dase-inhibitor |
198433, |
|
HS |
|
|
|
|
N |
|
|
BMS- |
|
|
|
|
N |
|
|
|
253653 |
|
|||
|
|
|
|
|
|
|
||||
Ph |
|
|
H |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
HO |
O |
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
NH2 |
|
|
|
|
|
Anti-HIV |
HIV-Protease- |
GS-4234, |
[28] |
|
|
|
|
|
|
|
|
|
inhibitor-1 |
GS-4263 |
|
|
|
|
|
Ph |
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
S |
O |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||
|
HO |
|
|
Ph |
|
|
|
|
||
|
|
|
HO |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
OH |
OH |
|
Antidiabetic |
Hypoglycemic |
Kotalanol |
[29] |
|
HO |
|
|
|
|
|
|
|
|||
|
+S |
|
|
|
|
|
|
|
||
|
|
|
OH |
OH |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O− S |
O |
|
OH |
|
|
|
|
|
|
|
O HO |
|
OH |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Доклад |
сделан |
по |
материалам обзора, |
полный текст которого опубликован: |
||||||
в кн. "Избранные методы синтеза и модификации гетероциклов", под ред.
Карцева В.Г., М.: IBS PRESS, 2003, т. 2, с. 206.
Генеральный спонсор и организатор – InterBioScreen Ltd. |
279 |

Производные [1,3,4]тиадиазоло[2,3-c][1,2,4]триазина – новый класс противовирусных препаратов
Кислый В.В.1, Демченко А.М.1, Квачева З.Б.2, Лозинский М.О.3
1Черниговский педагогический университет 14027, Украина, Чернигов, ул. Гетьмана Полуботка, 53
2ГУ НИИ эпидемиологии и вирусологии НАН Беларуси 220001, Минск, ул. К. Цеткин, 14 3Институт органической химии НАН Украины 02094, Киев, ул. Мурманская, 5
Соединения, содержащие 1,2,4-триазиновый цикл, проявляют широкий спектр биологической активности. Известны противомикробные препараты [1–3], вещества с высокой противовоспалительной и анальгезирующей активностью [4, 5], действующие на центральную нервную систему [6], активные против ВИЧ [7]. Исходными соединениями наших исследований являлись бифункциональные 4-амино- 6-R-3-метилтио-4,5-дигидро-1,2,4-триазин-5-оны 1, полученные [8] конденсацией серии α-кетокарбоновых кислот с тиокарбогидразидом и последующим алкилированием промежуточных 4-амино-6-R-3-меркапто-4,5-дигидро-1,2,4-триазин-5-онов иодметаном в метанольном растворе метилата натрия.
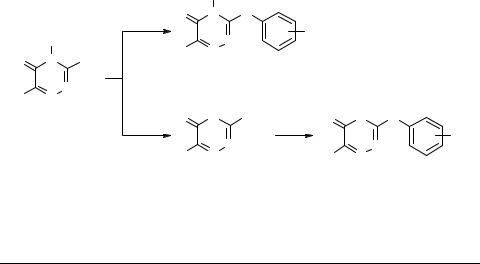
Мы синтезировали ряд 4-амино-6-R-3-ариламино-4,5-дигидро-1,2,4-триазин- 5-онов 2 (схема 1) нуклеофильным замещением метилтиогруппы на остаток ариламина при сплавлении эквимолярных количеств исходных реагентов при темпе-
ратуре 150–160°С.
|
|
|
|
|
|
|
|
|
Схема 1 |
|
|
|
O |
NH2 |
H |
|
|
|
|
|
|
ArNH2 |
N |
|
N |
R |
|
|
|
|
NH2 |
|
|
|
N |
|
|
|
|
|
SMe |
R |
N |
|
|
|
|
||
O |
N |
|
2 |
|
|
|
|||
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
R |
N N |
|
|
H |
|
|
|
H |
H |
|
1 |
HNO2 |
O |
|
SMe |
O |
|||
|
N |
|
N |
N |
|||||
|
|
|
|
|
|
|
Ar'NH2 |
|
R' |
|
|
|
|
N N |
|
|
N N |
||
|
|
|
R |
|
R |
|
|||
|
R = H, Me, t-Bu, Ph |
|
3 |
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
||
При нитрозировании (NaNO2 + HCl) аминотриазинонов 1 происходит дезаминирование с образованием триазинонов 3, которые также вступают в реакцию
Генеральный спонсор и организатор – InterBioScreen Ltd. |
281 |
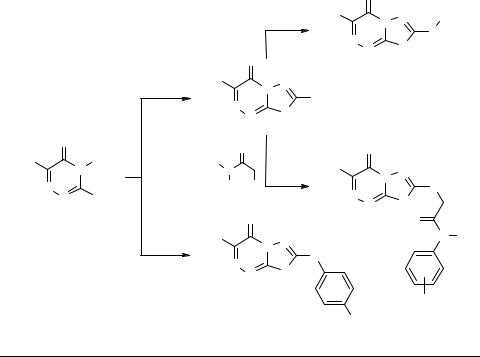
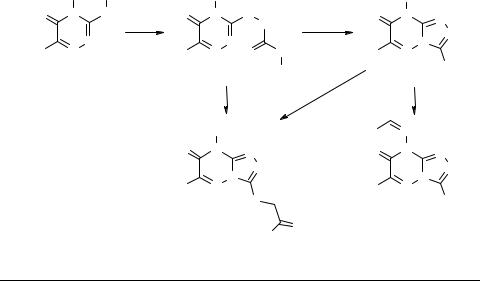
Взаимодействие эквимолярных количеств бифункционального амина 1 и соответствующего ароматического изотиоцианата в растворе сухого пиридина сопровождается интенсивным выделением метилмеркаптана и образованием 7-арила-
мино-3-(трет-бутил)-4Н-[1,3,4]тиадиазоло[2,3-c][1,2,4]триазин-4-онов 7 (схема 2).
В спектрах ПМР последних девятипротонный синглет трет-бутильной группы зарегистрирован при 1.41 м.д. Сигнал аминного протона находится в области 10.8–10.9 м.д. и исчезает при регистрации спектра ПМР с добавлением нескольких капель D2O.
При алкилировании тиолов 5 алкилгалогенидами в сухом ацетоне в присутствии безводного карбоната калия были получены соответствующие 3-(трет- бутил)-7-алкилсульфанил-4Н-[1,3,4]тиадиазоло[2,3-c][1,2,4]триазин-4-оны 8. Наличие алкилсульфанил групп в синтезированных веществах дало возможность предполагать о вероятном вступлении их в реакцию нуклеофильного замещения с ароматическими аминами и еще одном способе синтеза N-ариламидинов 7. Сплавление на масляной бане эквимолярных количеств 8 и пара-толуидина при 170°С сопровождалось бурным выделением метилмеркаптана с образованием кристалллического продукта. Но ПМР спектр полученного соединения содержал лишний протон и был идентичен спектру вышеупомянутого соединения 4 (R' = 4-Me). Таким образом, было установлено, что взаимодействие алкилмеркаптопроизводных 8 с ароматическими аминами приводит к распаду тиадиазольного цикла конденсированной системы и образованию 3-ариламино-6-R-4,5-дигидро-1,2,4-триазин-5- онов 4.
Кипячением 6-(трет-бутил)замещенного триазин-5-она 1 с 80%-ным гидразингидратом был получен 4-амино-6-(трет-бутил)-3-гидразино-4,5-дигидро-1,2,4- триазин-5-он 9 (схема 3), взаимодействие которого с арилизотиоцианатами позволило получить замещенные тиосемикарбазиды 10.
|
|
|
|
|
|
|
|
|
|
|
Схема 3 |
O |
NH2 |
NH2 |
|
NH2 |
H |
|
|
|
|
NH2 |
|
N |
NH |
O |
N |
N |
NH |
|
BuOH |
O |
N |
N |
|
|
|
|
|
|
|
|
|
|
N |
||
t-Bu |
N N |
|
|
N N S NH |
−Ar'NH2 |
|
N N |
||||
|
t-Bu |
t-Bu |
SH |
||||||||
|
9 |
|
|
10 |
|
Ar' |
|
|
|
11 |
|
|
|
|
O |
NH2 |
|
|
|
|
Ar |
N |
|
|
|
|
N |
N |
N |
|
|
O |
N |
N |
|
|
|
|
|
N N |
|
|
|
|
N N |
N |
|
|
|
|
t-Bu |
S |
|
|
t-Bu |
SH |
|||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
12 |
|
R |
O |
|
|
13 |
|
|
|
|
|
|
|
|
|
|
|||
Генеральный спонсор и организатор – InterBioScreen Ltd. |
|
|
283 |
||||||||


Литература
1.Hideki M., Isao A., Koichi I., Jpn. Patent 09 124 617, 1995; Chem. Abstr. 1997 127 342253r.
2.Abd El-Samii, Zakaria K., El-Feky S.A., J. Chem. Technol. Biotechnol. 1995 63
(2) 135; Chem. Abstr. 1995 123 256602k.
3.Mohan J.K., Indian J. Chem., Sect. B 1990 29 (7) 645.
4.Hisashi T., Hiroyoshi S., Akito T., Takatoshi I., PCT Int. Appl. WO 92 02 513, 1992; Chem. Abstr. 1992 116 235661u.
5.Sztanke K., Tkaczynski T., Acta Pol. Pharm. 1997 54 (2) 147.
6.Antoni T.J., Jordi F.C., PCT Int. Appl. WO 9 720 827, 1997; Chem. Abstr. 1997 127 81468z.
7.El-Gendy Z., Abdel Rahman R.M., Indian J. Heterocycl. Chem. 1995 4 (4) 293.
8.Dornow A., Menzel H., Marx P., Chem. Ber. 1964 57 (8) 2173.
Генеральный спонсор и организатор – InterBioScreen Ltd. |
285 |