
- •Часть 1
- •Часть 1
- •Программа
- •Адаптивного курса по физике для студентов,
- •Начинающих изучение курса общей физики в дгту
- •Механика
- •Статика
- •Гидростатика
- •Механические колебания и волны
- •Основы молекулярно-кинетической теории (мкт)
- •Термодинамика
- •Электростатика
- •Постоянный электрический ток
- •1. Механика
- •1.1. Кинематика
- •1.1.1. Траектория, путь, перемещение
- •1.1.2. Скорость и ускорение
- •1.1.3. Кинематика вращательного движения
- •1.2. Динамика материальной точки
- •1.2.1. Масса, сила, принцип суперпозиции сил
- •Правила сложения векторов
- •1.2.2. Вес тела, сила реакции опоры,
- •1.2.3. Инертность и инерция. Инерциальные системы отсчета.
- •1.2.4. Второй закон Ньютона. Импульс тела и импульс силы.
- •1.2.5. Классификация сил. Гравитационные силы.
- •Гравитационные силы. Закон всемирного тяготения
- •9,8 М/с2.
- •Упругие силы
- •Силы трения
- •1.2.6. Энергия. Механическая работа. Мощность.
- •1.3. Статика. Момент силы
- •2. Механические колебания и волны
- •2.1. Уравнение гармонических колебаний. Характеристики колебаний
- •2.2. Виды колебаний. Пружинный и математический маятники
- •Пружинный маятник
- •Математический маятник
- •2.3. Энергия тела при гармонических колебаниях
- •3. Основы молекулярно-кинетической теории
- •3.1. Основные положения молекулярно-кинетической теории (мкт)
- •3.2. Температура
- •3.3. Масса молекул. Количество вещества
- •3.4. Основное уравнение молекулярно-кинетической теории идеальных газов и уравнение состояния идеального газа
- •3.5. Изопроцессы в газах
- •4. Термодинамика
- •4.1. Внутренняя энергия. Работа газа. Первый закон термодинамики
- •Первое начало термодинамики:
- •4.2. Изопроцессы в термодинамике
- •4.3. Тепловой двигатель
- •5. Электростатика
- •5.1. Электрический заряд и его свойства. Закон Кулона
- •5.2. Электростатическое поле. Напряженность электростатического поля
- •Принцип суперпозиции
- •5.3. Потенциал электростатического поля
- •Эквипотенциальные поверхности
- •5.4. Электрическая емкость. Конденсаторы. Энергия электростатического поля
- •Плоский конденсатор
- •5.5. Соединения конденсаторов
- •6. Постоянный электрический ток
- •6.1. Сила тока и плотность тока
- •6.2. Сопротивление проводников
- •6.3. Разность потенциалов. Эдс. Напряжение
- •6.4. Закон Ома для участка цепи. Закон Ома для замкнутой цепи
- •6.5. Соединения резисторов
- •6.6. Работа и мощность тока
- •Образцы решения типовых задач
- •Задача №6
- •Задача №13
- •Решение
- •Задача №14
- •Задача №24
- •Часть 1
3.4. Основное уравнение молекулярно-кинетической теории идеальных газов и уравнение состояния идеального газа
В молекулярно-кинетической теории используется модель идеального газа, в которой считают:
1) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
2) между молекулами газа отсутствуют силы взаимодействия;
3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
4) время столкновения молекул много меньше времени пробега молекулы между столкновениями.
Реальные газы при низких давлениях и высоких температурах близки по своим свойствам к идеальному газу.
Рассмотрим
идеальный газ, который в объеме
![]() содержит
содержит![]() молекул, движущихся со скоростями
молекул, движущихся со скоростями
![]() .
Соударения между молекулами газа
приводят к тому, что скорости молекул
непрерывно меняются по величине и
направлению. Средняя
кинетическая
энергия одной молекулы массы
.
Соударения между молекулами газа
приводят к тому, что скорости молекул
непрерывно меняются по величине и
направлению. Средняя
кинетическая
энергия одной молекулы массы
![]() :
:
 , (35)
, (35)
где
 -средняя
квадратичная скорость
теплового движения молекул. Она связана
с термодинамической температурой
-средняя
квадратичная скорость
теплового движения молекул. Она связана
с термодинамической температурой
![]() газа
соотношением:
газа
соотношением:
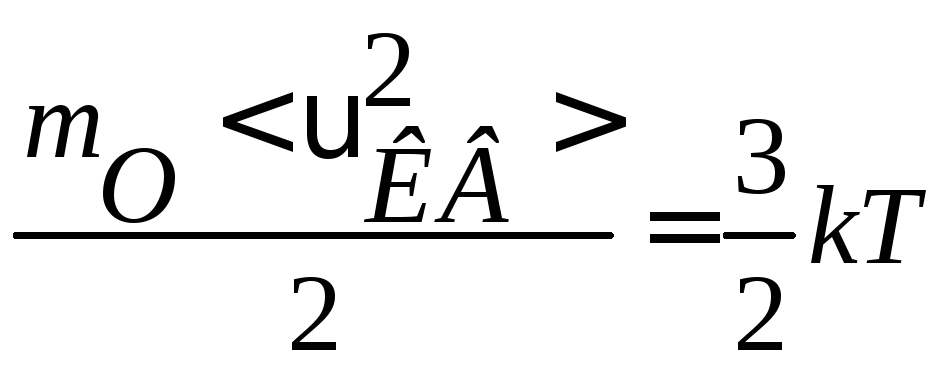 ,
,
где
![]() - постоянная Больцмана.
- постоянная Больцмана.
Отсюда:
 . (36)
. (36)
Учитывая,
что постоянная Больцмана ![]() ,
газовая постоянная
,
газовая постоянная
![]() и
число Авогадро
и
число Авогадро
![]() связаны соотношением
связаны соотношением![]() ,
а молярная масса
,
а молярная масса![]() ,
получаем формулу для вычисления средней
квадратичной скорости в виде:
,
получаем формулу для вычисления средней
квадратичной скорости в виде:
![]() . (37)
. (37)
Основное уравнение МКТ имеет вид:
![]() ,
(38)
,
(38)
где
![]() -
концентрация молекул. Откуда,
воспользовавшись формулой
-
концентрация молекул. Откуда,
воспользовавшись формулой
![]() ,
легко
получить полезное соотношение:
,
легко
получить полезное соотношение:
![]() . (39)
. (39)
Уравнение состояния идеального газа или уравнение Менделеева-Клапейрона:
![]() ,
(40)
,
(40)
где
![]() - универсальная газовая постоянная.
- универсальная газовая постоянная.
При
постоянной массе газа
![]() для двух различных состояний газа можно
записать
объединенный газовый закон:
для двух различных состояний газа можно
записать
объединенный газовый закон:
 . (41)
. (41)
3.5. Изопроцессы в газах
Изопроцессами называют процессы, протекающие в системе с неизменной массой при постоянном значении одного из параметров состояния системы.
1.
![]() –
изотермический
процесс
(закон Бойля – Мариотта:
–
изотермический
процесс
(закон Бойля – Мариотта:
![]() ).
).
2.
![]() -
изобарический
процесс
(закон Гей – Люссака:
-
изобарический
процесс
(закон Гей – Люссака:
 ).
).
3.
![]() –
изохорический
процесс
(закон Шарля:
–
изохорический
процесс
(закон Шарля:
 ).
).
Ниже
представлены графики всех изопроцессов
в координатах
![]() ;
;
![]() и
и
![]() (рис.
21).
(рис.
21).
Закон
Дальтона:
давление смеси газов равно сумме
парциальных давлений
![]() входящих в нее газов
входящих в нее газов
![]() . (42)
. (42)



Рис.21. Графики изотермического, изобарического
и изохорического процессов
Парциальное давление – это давление, которое производил бы газ, входящий в состав смеси газов, если бы только он один занимал весь объем, занимаемый смесью при той же температуре.
4. Термодинамика
Термодинамика – раздел физики, изучающий свойства макроскопических систем, находящихся в состоянии термодинамического равновесия, а также процессы перехода между этими состояниями. Термодинамика устанавливает связи между макроскопическими параметрами системы, не вдаваясь при этом в микроскопическую структуру вещества.
4.1. Внутренняя энергия. Работа газа. Первый закон термодинамики
Внутренняя
энергия
![]() – это энергия теплового движения
микрочастиц системы (молекул, атомов,
электронов, ядер и т.д.) и энергия
взаимодействия этих частиц. В термодинамике
практический интерес представляет не
само значение внутренней энергии, а ее
изменение
– это энергия теплового движения
микрочастиц системы (молекул, атомов,
электронов, ядер и т.д.) и энергия
взаимодействия этих частиц. В термодинамике
практический интерес представляет не
само значение внутренней энергии, а ее
изменение![]() .
Для одноатомного газа:
.
Для одноатомного газа:
![]() .
(43)
.
(43)
Внутренняя
энергия тела изменяется как при совершении
работы
![]() ,
так и при теплопередаче. Мера изменения
внутренней энергии тела при теплопередаче
называется количеством
теплоты
,
так и при теплопередаче. Мера изменения
внутренней энергии тела при теплопередаче
называется количеством
теплоты
![]() .
Количество теплоты, как и работа,
измеряется в джоулях (Дж).
.
Количество теплоты, как и работа,
измеряется в джоулях (Дж).
При
сообщении газу в изобарном процессе
некоторого количества теплоты он
совершает работу по перемещению поршня
на малое расстояние
![]() (рис. 22):
(рис. 22):
![]() ,
(44)
,
(44)
где
![]() - сила, действующая на поршень со стороны
молекул газа,
- сила, действующая на поршень со стороны
молекул газа,
![]() -
малое расстояние, на которое передвигается
поршень,
-
малое расстояние, на которое передвигается
поршень,
![]() -
давление газа,
-
давление газа,![]() -
изменение объема газа,
-
изменение объема газа,![]() - площадь поршня.
- площадь поршня.

Рис.22. Работа газа при расширении
Таким образом, работа расширения газа равна произведению давления газа на изменение его объема.
При
расширении газа
изменение
объема
![]() ,
и работа
,
и работа
![]() ,при
сжатии
газа
изменение
объема
,при
сжатии
газа
изменение
объема
![]() ,
и работа
,
и работа
![]() .
.
