
- •Расчетно-графическая работа по химии для направления подготовки бакалавров 250700 Ландшафтная архитектура Профиль подготовки – Садово-парковое и ландшафтное строительство
- •Основные понятия химии и простейшие стехиометрические расчеты
- •Периодический закон и реакционная способность веществ. Основные классы неорганических соединений
- •Элементы химической термодинамики и кинетики
- •Способы выражения состава раствора. Коллигативные свойства растворов
- •Равновесия в растворах электролитов: диссоциация, ионное произведение воды, рН, произведение растворимости, буферные растворы, гидролиз солей
- •Жесткость воды
- •Коллоидно-дисперсные системы
- •Окислительно-восстановительные и электрохимические системы
Способы выражения состава раствора. Коллигативные свойства растворов
Сколько граммов хлорида натрия нужно растворить в 300 мл воды для получения 14%-ного раствора? Плотность раствора равна 1,1009 г/см3. Рассчитайте также молярную, нормальную концентрацию и титр полученного раствора.
Какой объем 6%-ного раствора сульфата меди (II) (плотность 1,062 г/см3) требуется для взаимодействия с 90 мл 0,1 М раствора хлорида бария?
Определите массовую долю, молярную и моляльную концентрацию 2,64н. раствора серной кислоты плотностью 1,080 г/см3.
Сколько миллилитров 12%-ного раствора (плотность 1,1015 г/см3) и 2%-ного раствора (плотность 1,0148 г/см3) хлорида кальция нужно смешать для получения 120 мл 6%-ного раствора плотностью 1,0486 г/см3? Какова молярная концентрация полученного раствора?
На нейтрализацию 20 мл 0,2н. раствора соляной кислоты потребовалось 8,2 мл гидроксида натрия плотностью 1,020 г/см3. Определите процентную концентрацию по массе раствора гидроксида натрия.
Какова нормальная концентрация раствора, полученного при смешении 200 мл 2н. раствора серной кислоты и 300 мл 6%-ного раствора серной кислоты плотностью 1,040 г/см3?
Сколько миллилитров 14%-ного раствора хлорида кальция (плотность 1,1198 г/см3) нужно прибавить к одному литру 0,3н. раствора хлорида кальция, чтобы получить 0,8н. раствор соли?
К 60 мл 10%-ного раствора нитрата серебра (плотность 1,0882 г/см3) прибавили 20 мл 10%-ного раствора хлорида натрия (плотность 1,0707 г/см3). Какова молярная концентрация непрореагировавшего нитрата серебра?
Какой объем воды и 8%-ного раствора ортофосфорной кислоты (плотность 1,0420 г/см3) нужно взять для приготовления 200 мл 4%-ного раствора кислоты плотностью 1,0200 г/см3? Рассчитайте молярную концентрацию эквивалента кислоты (нормальность) и титр полученного раствора.
Какова молярная концентрация раствора гидроксида калия, полученного при смешении 300 мл 3 М раствора и 300 мл 11%-ного раствора щелочи плотностью 1,1 г/см3?
При одинаковой ли температуре будут замерзать 15%-ные водные растворы сахарозы (С12Н22О11) и глицерина (С3Н8О3)? Ответ обоснуйте соответствующими расчетами. Криоскопическая постоянная воды равна 1,86
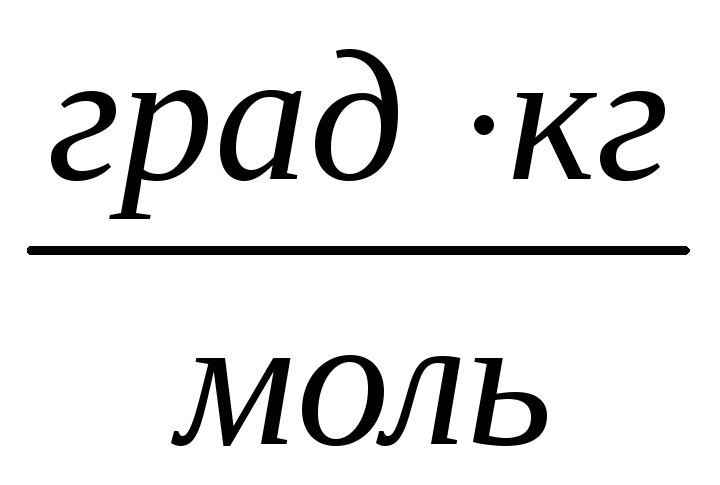 .
.При одинаковой ли температуре будут кипеть 20%-ные водные растворы глюкозы (С6Н12О6) и мочевины (СО(NH2)2)? Ответ обоснуйте соответствующими расчетами. Эбуллиоскопическая постоянная воды равна 0,52
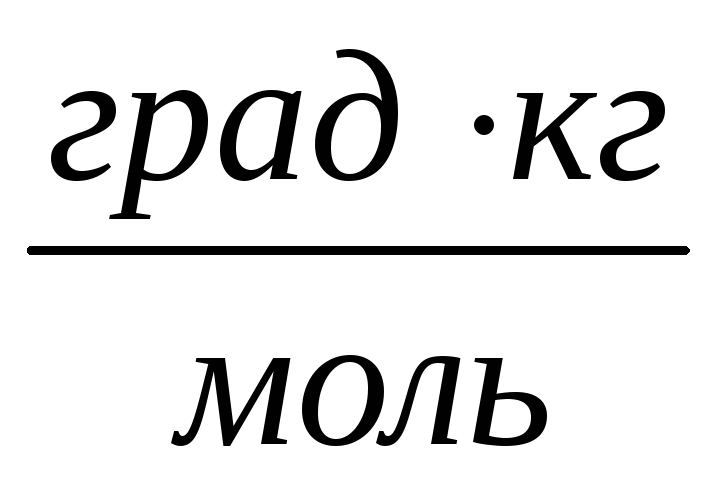 .
.Этиловый спирт кипит при 78,4 оС. При растворении 10,8 г некоторого неэлектролита в 200 г спирта температура кипения раствора стала равной 79,44 оС. Вычислите молярную массу растворенного вещества, если эбуллиоскопическая постоянная для этилового спирта равна 1,16
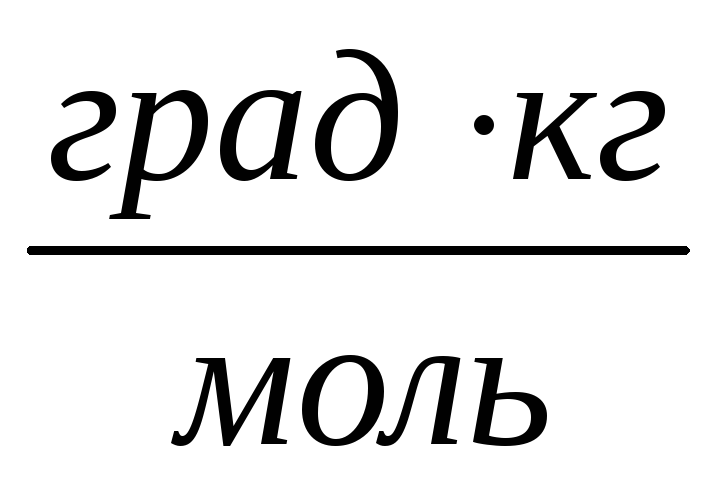 .Ответ: 60
г/моль
.Ответ: 60
г/мольДля приготовления антифриза (жидкость, замерзающая при низких температурах) смешали 2 л воды и 0,8 л глицерина (С3Н8О3). Плотность глицерина равна 1,26 г/cм3. Определите температуру замерзания полученной жидкости, если криоскопическая постоянная воды равна 1,86
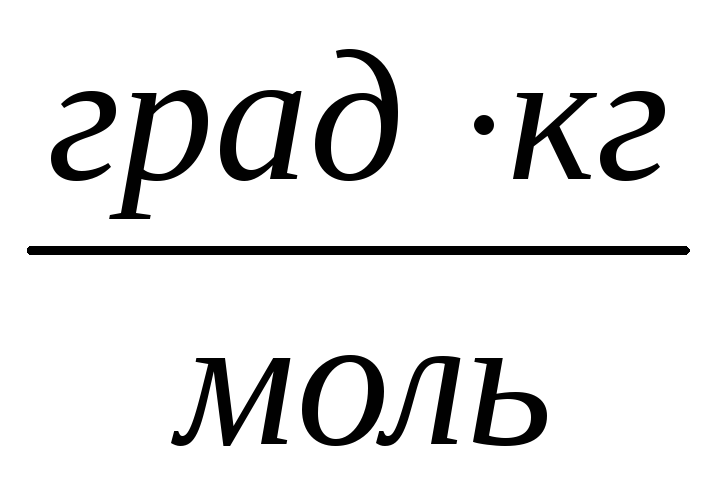 .
.Вычислите эбуллиоскопическую постоянную ацетона, если при растворении 0,5 моль некоторого неэлектролита в 150 г ацетона температура кипения последнего повысилась на 4,93 оС.
В каком объеме воды нужно растворить 50 г этиленгликоля (С2Н6О2), чтобы температура замерзания понизилась на 10 оС по сравнению с чистой водой? Криоскопическая постоянная воды равна 1,86
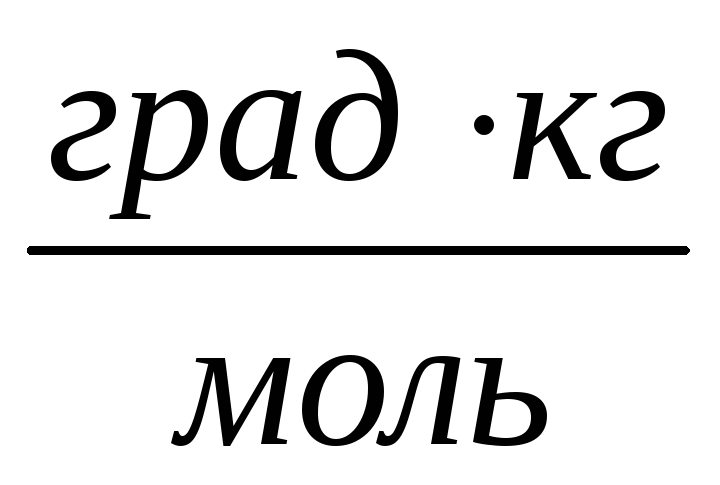 .
.Бензол кипит при 80,1 оС. В каком объеме бензола (плотность 0,879 г/см3, эбуллиоскопическая постоянная 2,57
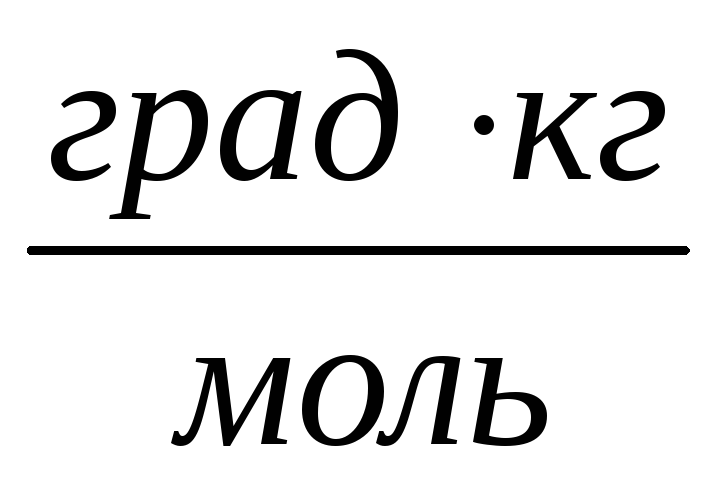 )
нужно растворить 10г
метилового спирта (СН3ОН),
чтобы температура кипения раствора
стала равной 82,1 оС?
)
нужно растворить 10г
метилового спирта (СН3ОН),
чтобы температура кипения раствора
стала равной 82,1 оС?Для какого из перечисленных растворов осмотическое давление будет максимально при заданной температуре?
а) в 800 мл раствора содержится 7,44 г анилина С6H5NH2;
б) в 600 мл раствора содержится 50 г сахарозы С12Н22О11;
в) в 200 мл раствора содержится 1,84 г глицерина С3Н8О3;
г) в 900 мл раствора содержится 48,6 г фруктозы С6Н12О6;.
Во сколько раз повысится осмотическое давление раствора при нагревании от 70С до 630С?
В 1 л воды растворили при заданной температуре 10 г неэлектролита. При растворении какого из перечисленных веществ давление насыщенного пара воды понизится максимально?
а) глюкоза С6Н12О6;
б) глицерин С3Н8О3;
в) сахароза С12Н22О11;
г) мочевина СО(NH2)2.
Какова при 2 0С величина осмотического давления раствора, содержащего 2 моль этиленгликоля в 10 л раствора?
Давление насыщенного пара над чистой водой при 29 0С составляет 4 кПа. Каково при той же температуре давление пара над раствором, содержащим 20 г глюкозы С6Н12О6 в 200 мл воды?
Давление насыщенного пара над чистой водой при 14 0С составляет 1,6 кПа. Каково при той же температуре давление пара над раствором, содержащим 40 г сахарозы С12Н22О11 в 1 л воды?
В каком объеме насыщенного раствора содержится 1 г PbBr2? Произведение растворимости PbBr2 составляет 9,1∙10-6.
Какой станет концентрация SrSO4 в насыщенном растворе после прибавления к нему Na2SO4 до концентрации Na2SO4 0,3 моль/л? Произведение растворимости SrSO4 равно 3,2∙10-7. Диссоциацию Na2SO4 считать полной, изменением ионной силы раствора пренебречь.
