
- •Биосинтез рнк
- •Структура рнк-полимеразы прокариот
- •Биосинтез белка
- •R Аминоацил-тРнк
- •Современные методы молекулярной биологии
- •Гормоны. Общий механизм действия гормонов
- •Механизм действия гормонов, взаимодействующих
- •Механизм действия гормонов, взаимодействующих с 1-тмс-рецепторами
- •Механизм действия гормонов, взаимодействующих с внутриклеточными (r)
- •Гормоны — производные белков, пептидов и аминокислот гормоны гипоталамуса
- •Гормоны аденогипофиза Это гормоны белково-пептидной природы.
- •Гормоны задней доли гипофиза
- •Гормоны поджелудочной железы
- •Стероидные гормоны
- •2.Окисление и изомеризация прегненолона в прогестерон. Прегненолон является предшественником всех стероидных гормонов.
- •Половые гормоны
- •Биохимия питания. Макро- и микроэлементы
- •Макроэлементы
- •Концентрация электролитов вне и внутри клетки существенно различается: натрий и кальций преобладают во внеклеточном пространстве, калий и магний — внутри клетки. Кальций
- •Кальцитонин
- •Паратирин (паратгормон)
- •Витамин д (кальциферол), антирахитический
- •Микроэлементы Железо
- •Биохимия питания. Витамины и другие незаменимые факторы питания. Синдром недостаточного питания
- •Витамины
- •Биохимия соединительных тканей и органов полости рта (костная, хрящевая ткани; зубы)
- •Неколлагеновые белки костной ткани и их роль в процессах минерализации
- •Химический состав тканей зуба и кости (весовые %)
- •Биохимия ротовой жидкости
- •Химический состав ротовой жидкости
- •Функции ротовой жидкости
- •1. Защитная.
- •3. Очищающая.
- •Ферменты ротовой жидкости и их роль
- •Поверхностные образования на эмали
- •Фтор (f) и его роль в организме
- •Биохимия печени
- •Функции печени
- •Миофибриллярные (сократительные) белки
- •Молекулярный механизм мышечного сокращения
- •Источники энергии мышечного сокращения
- •Механизмы энергообеспечения мышечного сокращения
Миофибриллярные (сократительные) белки
1. Миозин — основа толстых нитей. Молекулярная масса ≈ 500.000 Да. Молекула миозина имеет вытянутую часть, состоящую из двух спиралей, накрученных одна на другую. Каждая спираль имеет на одном конце глобулярную головку и называется тяжёлой цепью. Возле головок спиралей располагается по 2 лёгких цепи.

При обработке ферментами молекула миозина распадается на 2 больших фрагмента: тяжёлый меромиозин (обе головки и часть двойной спирали) и лёгкий меромиозин (остальная часть двойной спирали).
Функции миозина:
структурная — около 400 молекул миозина соединяются между собой «хвост» в «хвост» и образуют толстую нить;
каталитическая — головка миозина способна расщеплять АТФ;
контактная — соединяется с актином своими головками, которые в таком случае называются «поперечные мостики».
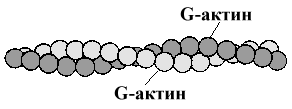
2. Актин — белок тонких нитей. Молекулярная масса — 42.000 Да. Форма молекул — шаровидная, поэтому он и называется G-актин (от англ. globular). Молекулы G-актина соединяются между собой и образуют F-актин (фибриллярный) в виде двойной спирали.
3. Тропомиозин — также белок тонких нитей. Молекулярная масса — 65.000 Да. Состоит из двух α-спиралей в форме палочки. Располагается в бороздках, идущих вдоль обеих сторон актина. Каждая его молекула лежит на 7 молекулах актина.
4. Тропонин — ещё один белок тонких нитей. Молекулярная масса — 80.000 Да. Состоит из 3 субъединиц: С — для связывания с ионами кальция; I — ингибиторная, которая блокирует преждевременное соединение головок миозина с актином; Т — для связывания с тропомиозином.

5. α-актинин. Входит в Z-линию и фиксирует там тонкие нити.
6. β-актинин. Регулирует длину тонких нитей.
7. М-белок. Входит в М-линию и фиксирует там толстые нити.
8. С-белок. Регулирует длину толстых нитей.
9. Десмин. Содержится между Z-линиями соседних миофибрилл, обеспечивая совпадение границ всех их саркомеров.
Белки саркоплазмы. К ним относятся миоглобин, ферменты гликолиза, тканевого дыхания, кальмодулин и кальсеквестрин, способные обратимо связываться с ионами кальция.
Белки стромы. Это коллаген и эластин.
Мышцы, помимо белков, содержат небелковые азотистые соединения — АТФ, КФ (креатинфосфат), фосфолипиды, глутамат, глутамин, карнозин и анзерин (два последних способны увеличивать амплитуду мышечного сокращения); безазотистые соединения — гликоген, лактат, пируват, нейтральные жиры, холестерол. Остальная масса — Н2О.
Молекулярный механизм мышечного сокращения
В ответ на нервный импульс происходит выброс ионов кальция из саркоплазматического ретикулума (СПР). Эти ионы связываются с лёгкими цепями миозина, при этом в головке расщепляется АТФ и головка готова присоединиться к актину. Ионы кальция затем связываются с тропонином С и меняют его конформацию. Эти изменения в силу эффекта кооперации передаются на субъединицу I и блокируют её. Далее изменения достигают субъединицы Т, которая и сдвигает в сторону молекулу тропомиозина, освобождая сразу 7 молекул актина. Головка миозина соединяется с актином, и образуется «поперечный мостик». Как только это произошло, АДФ и Фн уходят, головка наклоняется в сторону М-линии и тянет за собой тонкую нить. Затем к головке миозина присоединяется новая молекула АТФ, головка отделяется от нити актина, а гидролиз АТФ возвращает головку в вертикальное положение. Далее всё повторяется. Информацией о конце сокращения служит снижение концентрации ионов кальция в СПР. Тогда кальциевый насос и белок кальсеквестрин убирают избыток ионов кальция из цитоплазмы в СПР. Мышца переходит в состояние покоя.

Особенности гладких мышц:
их сократительный аппарат не содержит тропониновой системы, а содержит специальный белок кальдесмон, который выполняет функцию тропонина;
их миозиновая АТФазная активность в 10 раз ниже;
их миозин может соединяться с актином только при условии фосфорилирования лёгких цепей;
богаты белками стромы, но бедны фосфолипидами и макроэргами.
Гладкие мышцы — медленные, но способны длительно поддерживать напряжение.
Кроме того, они похожи на сердечную мышцу тем, что сокращаются непроизвольно.
