
Т.З. № 49-50-51
|
Физико-химический метод |
Величина, определяемая на приборе |
|
1. Фотоэлектроколориметрия 2. Поляриметрия 3. Рефрактометрия |
А. Оптическая плотность Б. Удельный показатель поглощения В. Угол вращения Г. Удельный угол вращения Д. Фактор преломления Е. Показатель преломления Ж. Молярный коэффициент поглощения |
Т.З.№ 52-53
|
Физико-химический метод |
Расчетная формула количественного содержания |
|
1. УФ-спектрофотометрия 2. Рефрактометрия |
А.
С% =
Б.
С% =
В.
С% =
Г.
С% =
|
Т.З.№ 54-55
Способ
расчета концентрации фотометрии
Расчетная формула![]()
по уравнению связи А. С%
 =
=
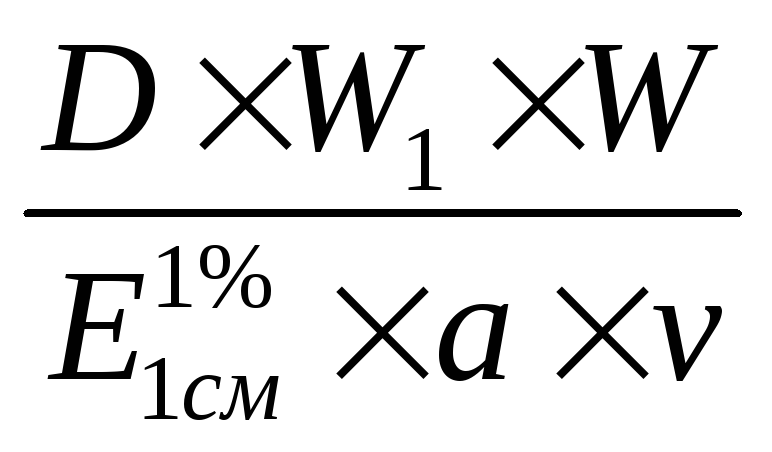
метод добавок
 Б. С% =
Б. С% =
В. С% =
![]() Г. С% =
Г. С% =![]()
Д.![]() С% =
С% =![]()
Т.З.№ 56 Показатель доброкачественности лекарственных средств «Прозрачность» подразумевает испытание
1.определение внешнего вида по форме кристаллов
2.определение растворимости
определение примесей кислотного и основного характера
нерастворимых примесей
обнаружение окрашенных примесей
Т.З.№ 57 Показатель доброкачественности лекарственных средств «Цветность» подразумевает испытание
определение внешнего вида по форме кристаллов
определение растворимости
определение примесей кислотного и основного характера
нерастворимых примесей
обнаружение окрашенных примесей
Т.З.№ 58 Показатель доброкачественности лекарственных средств «Кислотность или щелочность» подразумевает испытание
определение внешнего вида по форме кристаллов
определение растворимости
определение примесей кислотного и основного характера
кислотно-основное титрование лекарственного средства
обнаружение окрашенных примесей
Т.З.№ 59 Для определения общих допустимых примесей в лекарственных средствах ГФ регламентирует методику
1. в испытуемый раствор добавляются все реактивы, кроме основного, содержимое пробирки делится пополам, в одну пробирку добавляется основной реактив
в испытуемый раствор добавляются вспомогательный и основной растворы, содержимое пробирки делится пополам
в испытуемый и эталонный растворы одновременно, в равных количествах добавляются все реактивы
в испытуемый и эталонный растворы одновременно, в равных количествах добавляются все реактивы, кроме основного
в испытуемый раствор добавляется основной реактив, а в эталонный не добавляется.
Т.З. № 60. Для определения общих недопустимых примесей в ЛС ГФ регламентируются методики
в испытуемый раствор добавляются все реактивы, кроме основного, содержимое пробирки делится пополам, в одну пробирку добавляется основной реактив
в испытуемый раствор добавляются вспомогательный и основной растворы, содержимое пробирки делится пополам
в испытуемый и эталонный растворы одновременно, в равных количествах добавляются все реактивы
в испытуемый и эталонный растворы одновременно, в равных количествах добавляются все реактивы, кроме основного
в испытуемый раствор добавляется основной реактив, а в эталонный не добавляется.
Т.З. № 61. Для нитритометрического титрования ЛС создаются дополнительные условия
строгое соблюдение рН среды за счет прибавления буферного раствора
прибавление катализатора, медленное титрование охлаждении, солянокислая среда
добавление органического растворителя
минирализация в присутствии катализатора
кипячение с избытком титранта.
Т.З. № 62. Для комплексометрического титрования ЛС создаются дополнительные условия
строгое соблюдение рН среды за счет прибавления буферного раствора
прибавление катализатора, медленное титрование охлаждении, солянокислая среда
добавление органического растворителя
минерализация в присутствии катализатора
кипячение с избытком титранта.
Т.З. № 63. Для количественного определения ЛС по полному методу Кьельдаля проводится дополнительный процесс
строгое соблюдение рН среды за счет прибавления буферного раствора
прибавление катализатора, медленное титрование охлаждении, солянокислая среда
добавление органического растворителя
минерализация в присутствии катализатора
кипячение с избытком титранта.
Т.З. № 64. Для количественного определения ЛС по методу кислотного или щелочного гидролиза проводится дополнительный процесс
строгое соблюдение рН среды за счет прибавления буферного раствора
прибавление катализатора, медленное титрование охлаждении, солянокислая среда
добавление органического растворителя
минерализация в присутствии катализатора
кипячение с избытком титранта.
Т.З. № 65. Для алкалиметрического титрования солей слабых органических оснований и сильных кислот создается дополнительное условие
строгое соблюдение рН среды за счет прибавления буферного раствора
прибавление катализатора, медленное титрование охлаждении, солянокислая среда
добавление органического растворителя
минерализация в присутствии катализатора
кипячение с избытком титранта.
Т.3. №66. Для обнаружения мути и опалесценции при определении допустимых пределов общих примесей ГФ 11 регламентирует порядок наблюдения
Проходящий свет и темный фон
Проходящий свет и матово-белый фон
Отраженный свет и матово-белый фон
Отраженный свет и темный фон
Падающий свет и темный фон.
Т.3 № 67. Для обнаружения окраски растворов при определении допустимых пределов общих примесей ГФ 11 регламентирует порядок наблюдения
1.Проходящий свет и темный фон
2.Проходящий свет и матово-белый фон
Отраженный свет и матово-белый фон
Отраженный свет и темный фон
Падающий свет и темный фон.
Т.3 № 68. Для обнаружения допустимых пределов примеси мышьяка(3) и (5) в лекарственных средствах по методу Зангера-Блека используется реактив
Ртути дихлорид 4. Ртути дийодид
Кислота фосфорноватистая 5. Тетраиодомеркурат (2) калия
Кислота фосфористая
Т.3 № 69. Для обнаружения допустимых пределов примеси мышьяка(3) и(5) в лекарственных средствах по методц Буго-Тиле используется реактив
Ртути дихлорид 4. Ртути дийодид
Кислота фосфорноватистая 5. Тетраиодомеркурат (2) калия
Кислота фосфористая
Т.3. №70. В основе определения примеси мышьяка (3) и (5) в лекарственных средствах по методу Зангера-Блека лежит химическая реакция
1. Восстановление до металлического мышьяка
Окисление до металлического мышьяка
Восстановление до мышьяковистого водорода
Окисление до мышьяковистого водорода
Восстановление до мышьяковистого ангидрида
Т.3. №71. В основе определения примеси мышьяка (3)и (5) в лекарственных средствах по методу Буго-Тиле лежит химическая реакция
Восстановление до металлического мышьяка
Окисление до металлического мышьяка
Восстановление до мышьяковистого водорода
Окисление до мышьяковистого водорода
Восстановление до мышьяковистого ангидрида
Т.3. №72. Для обнаружения примеси железа (2)и (3) в лекарственных средствах используется реактив
Калия гексацианоферрат (II)
Калия гексацианоферрат (III)
Калия тетрайодомеркурат (II)
Кислота ацетисалициловая
Кислота сульфрсалициловая
Т.3. №73.Действие фактора внешней среды на эуфиллин обуславливает процесс и изменение его внешнего вида
Белый налет на кристаллах за счет выветривания кристаллизационной воды при повышении температуры
Изменение агрегатного состояния – переход из твердого в жидкое – за счет поглощения влаги воздуха
Появление желтого оттенка на белом порошке за счет окисления кислородом воздуха
Выделение маслянистых капель, переходящих в осадок, под действием щелочности стекла
Выделение слабой органической кислоты из соли под действием углекислоты воздуха
Т.3. №74.Действие фактора внешней среды на меди сульфат обуславливает процесс и изменение его внешнего вида
Белый налет на кристаллах за счет выветривания кристаллизационной воды при повышении температуры
Изменение агрегатного состояния – переход из твердого в жидкое – за счет поглощения влаги воздуха
Появление желтого оттенка на белом порошке за счет окисления кислородом воздуха
Выделение маслянистых капель, переходящих в осадок, под действием щелочности стекла
Выделение слабой органической кислоты из соли под действием углекислоты воздуха
Т.3. №75.Действие фактора внешней среды на кальция хлорид обуславливает процесс и изменение его внешнего вида
Белый налет на кристаллах за счет выветривания кристаллизационной воды при повышении температуры
Изменение агрегатного состояния – переход из твердого в жидкое – за счет поглощения влаги воздуха
Появление желтого оттенка на белом порошке за счет окисления кислородом воздуха
Выделение маслянистых капель, переходящих в осадок, под действием щелочности стекла
Выделение слабой органической кислоты из соли под действием углекислоты воздуха
Т.3. №76.Действие фактора внешней среды на калия йодид обуславливает процесс и изменение его внешнего вида
Белый налет на кристаллах за счет выветривания кристаллизационной воды при повышении температуры
Изменение агрегатного состояния – переход из твердого в жидкое – за счет поглощения влаги воздуха
Появление желтого оттенка на белом порошке за счет окисления кислородом воздуха
Выделение маслянистых капель, переходящих в осадок, под действием щелочности стекла
Выделение слабой органической кислоты из соли под действием углекислоты воздуха
Т.3. №77.Действие фактора внешней среды на новокаин в растворе для инъекций обуславливает процесс и изменение его внешнего вида
Белый налет на кристаллах за счет выветривания кристаллизационной воды при повышении температуры
Изменение агрегатного состояния – переход из твердого в жидкое – за счет поглощения влаги воздуха
Появление желтого оттенка на белом порошке за счет окисления кислородом воздуха
Выделение маслянистых капель, переходящих в осадок, под действием щелочности стекла
Выделение слабой органической кислоты из соли под действием углекислоты воздуха
Т.3. №78.Для определения растворимости у легко растворимых лекарственных веществ берется масса (в граммах)
0,0001 4. 0,1
0,001 5. 1
0,01
Т.3. №79.Для выражения растворимости лекарственных веществ ГФ ХI регламентирует два способа
в условных частях и терминах
в терминах и реальных частях
в реальных частях и в условных терминах
в условных терминах и частях
в частях и специфических терминах
№ 80 Контроль качества лекарственных форм, изготовляемых в аптеке, регламентирует приказ
№53 4. №214
№96 5. №305
№211
Т.3.№81 К обязательным относятся виды внутриаптечного контроля
письменный, органолептический, контроль при отпуске, приемочный, химический (кроме индивидуальных лекарственных форм)
опросный, физический, химический (индивидуальные лекарственные формы)
физический, химический, письменный
органолептический, опросный, письменный
приемочный, контроль при отпуске, опросный
Т.3.№82 К выборочным относятся виды внутриаптечного контроля
письменный, органолептический, контроль при отпуске, приемочный, химический (кроме индивидуальных лекарственных форм)
опросный, физический, химический (индивидуальные лекарственные формы)
физический, химический, письменный
органолептический, опросный, письменный
приемочный, контроль при отпуске, опросный
Т.3.№83 Вода очищенная подвергается неполному химическому контролю в аптеке на примеси
хлориды, сульфаты и кальций
аммиак, восстанавливающие вещества и углекислота
хлориды, сульфаты и аммиак
хлориды, кальций и аммиак
тяжелые металлы, нитраты и аммиак
Т.3.№84 Испытание на примеси нитратов и нитритов в воде для инъекций регламентируется требованием ФС
синяя окраска с дифениламином в конц. серной кислоте должна сохраняться
не должно появляться синей окраски с дифениламином в конц. серной кислоте
розовая окраска с калия перманганатом должна сохраняться
розовая окраска с калия перманганатом должна исчезнуть
при нагревании с конц. кислотой серной не должно выделятся бурых паров азота
Т.3.№85 Для доказательства подлинности ингредиентов в лекарственной смеси состава: калия йодид и кислота аскорбиновая используется общий реактив
серебра нитрат
натрия нитрит в солянокислой среде
меди сульфат
дифениламин в конц. серной кислоте
нингидрин
Т.3.№86 С кислотой хлороводородной одновременно на основе различного внешнего эффекта определяются ингредиенты в лекарственной смеси
натрия гидрокарбонат и натрия бензоат
натрия бензоат и натрия салицилат
натрия салицилат и новокаин
новокаин и резорцин
резорцин и тримекаин
Т.3.№87 Доказательство подлинности обоих ингредиентов в лекарственной смеси: гекасметилентетрамин и натрия гидрокарбонат, с кислотой хлороводородной проводится по образованию газообразных продуктов
аммиак и углекислый газ
углекислый газ и оксид азота
оксид азота и формальдегид
формальдегид и углекислый газ
углекислый газ и азот
Т.3.№88 Для раздельного определения в одной навеске двух ингредиентов в лекарственной смеси: йод и калия йодид используются методы
ацидиметрия и алкалиметрия
алкалиметрия и йодометрия
йодометрия и аргентометрия
аргентметрия и меркуриметрия
меркуриметрия и перманганатометрия
Т.3.№89 Для раздельного определения ингредиентов в лекарственной смеси: кислота аскорбиновая и глюкоза в одной навеске используется метод
ацидиметрия 4. йодометрия
алкалиметрия 5. трилонометрия
меркуриметрия
Т.3.№90 Для раздельного определения в одной навеске обоих ингредиентов в лекарственной смеси: натрия гидрокарбонат и натрия бензоат используется метод
ацидиметрия 4. йодометрия
алкалиметрия 5. трилонометрия
меркуриметрия
Т.3.№91 Уравнения химических реакций, лежащих в основе количественного определения HgО, обозначают метод
HgО+4KJ+H2O =K2HgJ4+2KOH
2KOH+2HCI = 2KCI +2H2O
косвенная алкалиметрия
косвенная ацидиметрия
обратная ацидиметрия
щелочной гидролиз
сочетание косвенной и обратной алкалиметрии
Т.3.№92 Уравнения химических реакций, лежащих в основе количественного определения МgО, обозначают метод
МgО + 2HCI =MgCI2+H2O
HCI + NaOH =NaCI +H2O
косвенная алкалиметрия
косвенная ацидиметрия
обратная ацидиметрия
щелочной гидролиз
сочетание косвенной и обратной алкалиметрии
Т.3.№93 Уравнения химических реакций, лежащих в основе количественного определения серы очищенной, обозначают метод
S +3Н2O2+ 2KOH =K2SO4 +4H2O
KOH + HCI = KCI + H2O
косвенная алкалиметрия
косвенная ацидиметрия
обратная ацидиметрия
щелочной гидролиз
сочетание косвенной и обратной алкалиметрии
Т.3.№94 Уравнения химических реакций, лежащих в основе количественного определения фенилсалицилата, обозначают метод
С6Н4ОНСООС6Н4ОН +NaOH = С6Н4ОНСООNa +C6H4OH
С6Н4ОНСООNa +HCI=С6Н4ОНСООH + NaCI
NaOH + HCI = NaCI + H2O
косвенная алкалиметрия 3. обратная ацидиметрия
косвенная ацидиметрия 4. щелочной гидролиз
5. сочетание косвенной и обратной алкалиметрии
Т.3.№95 Уравнения химических реакций, лежащих в основе количественного определения теофиллина, обозначают метод



 Теофиллин
(N7-H)
+ AgNO3
=
теофиллин(
N7-Ag)
+ HNO3
Теофиллин
(N7-H)
+ AgNO3
=
теофиллин(
N7-Ag)
+ HNO3
NaOH + HNO3 = NaNO3 + H2O
косвенная алкалиметрия
косвенная ацидиметрия
обратная ацидиметрия
обратная аргентометрия
сочетание косвенной и обратной алкалиметрии
Т.3.№96 Для установки титра 0,01 М растворов, калия йодата, калия бромата по ГФ ХI используется вещество
калия гидрофталат 4. натрия карбонат
натрия тиосульфат 5. калия дихромат
натрия хлорид
Т.3.№97 Для установки титра 0,5 М растворов кислоты хлорной, натрия гидроксида по ГФ ХI используется вещество
калия гидрофталат 4. натрия карбонат
натрия тиосульфат 5. калия дихромат
натрия хлорид
Т.3.№98 Титрованным растворам ртути окисной нитрата,кислоты серной по ГФ ХI соответствует величина условной частицы (УЧ)
1/2 4. 1/5
1/3 5. 1/6
1/4
Т.3.№99 Титрованным растворам калия йодата, калия бромата,калия бихромата по ГФ ХI соответствует величина условной частицы(УЧ) 1.1/2 4. 1/5
2.1/3 5. 1/6
3.1/4
Т.3.№100 При окислительно-восстановительном титровании лекарственных веществ используется индикатор
бромтимоловый синий 4.дифениламин
бромфеноловый синий 5.нейтральный красный
мурексид
Т.3.№101 При осадительном титровании лекарственных веществ используется индикатор
бромтимоловый синий 4. дифениламин
бромфеноловый синий 5. нейтральный красный
мурексид
