
- •Министерство здравоохранения украины
- •Iіі. Материалы для | самостоятельной работы.
- •3.2 Содержание темы занятия
- •3.1 Клиническая физиология почек
- •3.2 Анатомия почки
- •3.2.1. Кровообращение в почках
- •3.2.2 Транспорт растворенных веществ
- •5.3. Экскреция продуктов метаболизма
- •3.2.4. Почечная регуляция кислотно-основного состояния
- •5.5. Концентрирование и разведение мочи
- •5.6. Нейроэндокринная регуляция функции почек
- •5.6.1. Альдостерон
- •5.6.2. Антидиуретический гормон
- •5.6.3. Паратиреоидный гормон и кальцитонин
- •3.2.4. Катехоламины
- •5.7. Выведение лекарственных средств почками
- •3.2.8. Диурез и диуретики
- •5.9. Мочекаменная болезнь
- •5.9.1. Ураты
- •5.9.2. Оксалаты
- •5.9.3. Фосфаты
- •5.9.4. Цистиновые камни
- •3.2.10. Острая почечная недостаточность
- •5.11. Хроническая почечная недостаточность (хпн)
- •5.12. Дифференциальная диагностика различных видов почечной недостаточности
- •5.13. Лечение острой почечной недостаточности
- •5.13.1. Консервативное лечение хронической почечной недостаточности
- •5.13.2. Активные методы лечения хпн
- •5.14. Трансплантация почки
- •6.1. Кровообращение в ткани печени
- •6.1.1. Анатомия сосудов и макроциркуляция в печени
- •6.1.2. Регуляция кровообращения в печени
- •6.1.2.1. Внутренняя регуляция
- •6.1.2.2. Внешняя регуляция
- •6.1.3. Влияние анестезии на кровоток в печени
- •6.2. Метаболические функции печени
- •6.2.1. Обмен белков
- •6.2.2. Обмен углеводов
- •6.2.3. Обмен липидов
- •6.3. Желчеобразование и желчеотделение
- •6.3.1. Состав и функция желчи. Желчные кислоты
- •6.3.2. Функциональная анатомия желчевыводящих путей
- •6.3.3. Желчеобразование
- •6.3.4. Желчный пузырь и его моторика.
- •Влияние анестезии
- •На нарушение моторики у больных
- •В критическом состоянии
- •6.4. Роль печени в гем0п0эзе
- •6.4.1. Роль печени в эритропоэзе
- •6.4.2. Роль печени в обмене порфиринов
- •6.5. Гуморальная функция печени
- •6.6. Печень и естественная иммунная реактивность
- •6.7. Клинические и биохимические показатели функции печени
- •6.7.1. Клинические симптомы нарушения функции печени
- •6.7.2. Биохимические показатели нарушения функции печени
- •3.3 Вопросы для индивидуального устного опроса:
- •3.4 Задачи для самоконтроля:
- •IV. Материалы для аудиторной самостоятельной работы
- •4.1. Перечень|перечисление| учебных практических|практичных| заданий|задачи|, которые|какие| необходимо выполнить|исполнить| на практическом|практичном| занятии:
- •4.2. Профессиональные алгоритмы:
- •V. Рекомендуемая литература:
6.2.3. Обмен липидов
Липиды — это соединения, отличительными особенностями которых являются наличие в их молекуле остатков жирных кислот и слабая растворимость в воде. Жирные кислоты содержат длинную неразветвленную цепь углеродных атомов (обычно 16, 18 или 20) и различное число двойных связей (от 0 до 4), а на одном из концов углеродного скелета — карбоксильную группу. Соответствующая формула наиболее распространенной насыщенной жирной кислоты — пальмитиновой — составляет 16:0; ненасыщенной кислоты с одной двойной связью — олеиновой — 18 : 1; полиненасыщенных жирных кислот 18 : 2 (линолевая), 18 : 3 (ли-ноленовая), 20 : 4 (арахидоновая). При этом организм человека способен синтезировать насыщенные и мононенасыщенные жирные кислоты. Полиненасыщенные жирные кислоты являются незаменимыми: они должны поступать с пищей. Значение полиненасыщенных жирных кислот обусловлено их ролью в организме. Во-первых, они являются предшественниками простагландинов, выполняющих различные регуляторные функции. Во-вторых, они поддерживают жидкое состояние липидов клеточных мембран. В-третьих, полиненасыщенные жирные кислоты предотвращают отложение холестерина и других липидов в стенках кровеносных сосудов.
Молекулы жирной кислоты содержат большое количество звеньев ((СН2)„), этим объясняется то, что жирные кислоты являются наиболее эффективным энергетическим субстратом организма. Энергия, запасаемая в ходе биологических окислительных процессов, в основном связана с переносом электронов от атомов водорода по дыхательной цепи и фосфорилиро-ванием АДФ до АТФ. Поскольку жирные кислоты построены преимущественно из углерода и водорода, их окисление сопровождается большим выходом энергии, чем, например, углеводов: в состав последних входят и атомы кислорода. Так, при окислении 1 г жиров образуется 9 ккал (37,67 кДж) энергии, 1 г углеводов или белков — по 4 ккал (16,74 кДж). Более половины основной энергетической потребности многих тканей удовлетворяется за счет жиров, особенно в период голодания.
Жирные кислоты редко встречаются в свободном виде. Обычно они входят в состав различных соединений — ацилгли-церидов, фосфоглицеридов, стероидов, жирорастворимых витаминов A, D, Е и К. Среди них особое место занимают три-ацилглицериды. В молекуле глицерина содержатся три гидроксильные группы, которые могут быть этерифицированы жирными кислотами с образованием соответственно моно-, ди- или триацилгли-церидов. Триацилглицериды обычно называют жирами. Их содержание в составе липидов, поступающих с пищей, у человека достигает более 90 %.
Процесс метаболизма липидов пищи в просвете и стенке пищеварительного канала состоит из нескольких основных этапов: 1. Секреция поджелудочной железой гидролитических ферментов, содержащих липазы и буферные системы, разрывающие в жирах сложноэфирные связи. 2. Поступление в просвет ПК в составе желчи желчных кислот, эмульгирующих жиры и продукты их распада. 3. Гидролиз липидов под влиянием секрета поджелудочной железы и желчи до моноглицеридов и свободных жирных кислот. Моноглицериды располагаются между молекулами солей желчных кислот, образуя смешанные мицеллы. 4. Захват слизистой кишок мицелл с последующим превращением в стенке кишок. При этом жирные кислоты и моноглицериды вступают друг с
другом
в энергозависимые реакции реэтерификации с образованием триацилглицеридов, характерных именно для данного организма. 5. Транспорт липидов к печени как по системе воротной вены, так и по системе печеночной артерии.
По системе воротной вены в печень поступает лишь незначительная часть липидов. К ним относятся соли желчных кислот и жирные кислоты с короткой цепью. Последние переносятся к печени в виде комплексов с альбумином плазмы. Достигая печени, они подвергаются катаболизму в ходе реакций окисления и не играют большой роли в обмене веществ, за исключением детей, в питании которых преобладают жиры молока. Соли желчных кислот, наоборот, захватываются печенью для дальнейшего использования. Они поступают в общий пул из нескольких граммов желчных кислот во внутриклеточном пространстве, в желчных протоках и в концен-
трированном виде — в желчном пузыре. Таким образом, совершается энтеросистем-ная рециркуляция желчных кислот. При этом лишь незначительная часть желчных кислот экскретируется с калом.
Основная часть липидов транспортируется к печени по системе печеночной артерии. Ресинтезированный триацилглице-рид и холестерин поступают из кишок в лимфатические сосуды, затем через грудной лимфатический проток попадают в кровь. Липиды к печени переносятся преимущественно в виде хиломикронов, хотя пул транспортных форм липидов разнообразен. После приема жирной пищи в крови содержится большое количество хиломикронов, вследствие чего плазма мутнеет и делается похожей на молоко. Это вызывает появление в крови так называемого просветляющего фактора. В его состав входит липаза липопротеидов, расщепляющая триглицериды хиломикронов и липопротеидов. Расщепляющий фактор образуется под влиянием гепарина, содержащегося в печени, легких, мышцах и других органах. На этом основаны рекомендации добавлять небольшие дозы гепарина в растворы жировых эмульсий при проведении парентерального питания.
Еще одним источником липидов, поступающих в печень, являются свободные жирные кислоты, освобождаемые из жировой ткани и поступающие к печени с кровью в виде комплексов с альбумином. Хотя в самой печени запасы жиров незначительны (они составляют менее 1 % общей массы органа), она занимает ключевую позицию в процессах мобилизации, переработки и биосинтеза жиров.
Окисление жирных кислот в печени осуществляется в митохондриях. Процессы связаны с заключительными реакциями катаболизма в системе переноса электронов и цикла лимонной кислоты. При этом окисление жирных кислот состоит из трех основных этапов (рис. 6.3). 1. Активация жирных кислот путем энергозависимой реакции образования тиоэфиров ацил-КоА. 2. р-Окисление — замкнутый цикл реакций последовательного отщепления атомов водорода от алкильной цепи и двухуглеродных остатков в виде молекул ацетил-КоА. 3. Окисление в цикле лимонной кислоты образующихся молекул ацетил-КоА до СО2 и дополнительного количества водорода, используемого затем при окислительном фосфорилировании.
Печень играет также ключевую роль в процессах липогенеза — в синтезе жирных кислот в организме. За исключением полиненасыщенных, все другие жирные кислоты, необходимые либо как структурные липиды для построения мембран, либо для создания тканевых депо, синтезируется в организме человека. Любое вещество, конечным продуктом обмена которого является ацетил-КоА, может быть использовано в липогенезе. Но наиболее значимым предшественником являются углеводы (см. «Обмен углеводов»). Во всех случаях, когда потребление углеводов превышает энергетические потребности организма, их избыток превращается в жиры.
Печень также принимает активное участие в обмене холестерина в организме человека. В отличие от триацилглицеридов, играющих роль энергетического резерва, холестерин является компонентом клеточных мембран, предшественником солей желчных кислот, стероидных гормонов, витамина D, а при патологии — узловым патогенетическим звеном развития атеросклероза. Часть холестерина поступает в организм с пищей. Небольшое количество

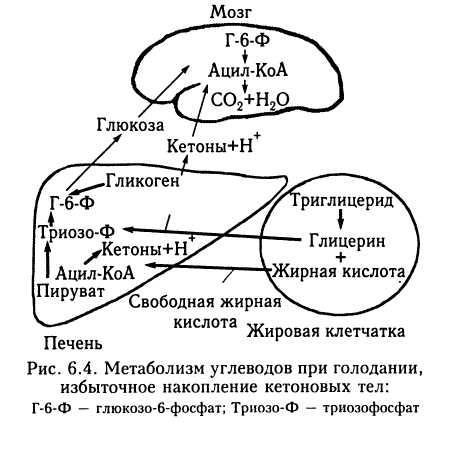
Печень является местом синтеза кетоновых тел (ацетоуксусная кислота, р-оксимас-ляная кислота и ацетон). В норме их содержание в плазме не превышает 10 мг/л, но значительно возрастает при декомпенсации сахарного диабета. При этом происходят противоположные описанным при характеристике обмена углеводов процессы превращения триглицеридов жировой клетчатки (рис. 6.4). В условиях голодания, когда экзогенная глюкоза отсутствует, эндогенные триглицериды жировой клетчатки претерпевают обратное превращение путем липолиза в свободные жирные кислоты и глицерин. Эти соединения транспортируются в печень, где глицерин включается в реакции глюконеогенеза. Синтезируемая при этом глюкоза может поступать в кровоток в то время, когда концентрация глюкозы в плазме имела бы тенденцию к снижению, если бы процесс глюконеогенеза не функционировал. Кроме того, свободные жирные кислоты, поступающие из жировой ткани, могут использоваться большинством органов и тканей (за исключением головного мозга) как источник энергии. При превращении свободных жирных кислот в печени образуется ацетил-КоА. Путем ферментативного превращения двух молей ацетил-КоА в печени образуется ацетоуксусная кислота, которая в дальнейшем может
быть восстановлена до р-оксимасляной кислоты или декарбо-ксилирована с образованием ацетона.
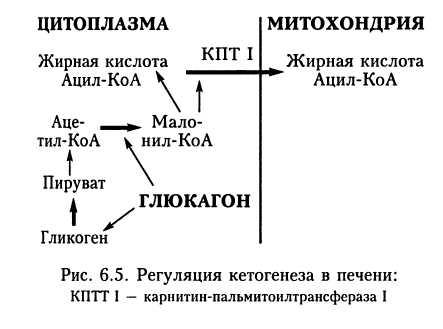
но и накоплением контринсулярных гормонов стресса чаще всего вследствие развития сопутствующего заболевания (прежде всего, воспалительных процессов, тром-боэмболических осложнений, инфаркта миокарда). Одним из таких контринсулярных гормонов является глюкагон (рис. 6.5). Кетоновые тела образуются в митохондриях печени. При этом количество соединений жирных кислот, поступающих в митохондрии печени, зависит от активности фермента карнитин-пальмитоилтрансфе-разы, локализованного на внешней стороне мембраны митохондрии. Обычно активность этого фермента снижена за счет повышенной концентрации в цитоплазме соединения малонил-КоА, являющегося первым промежуточным продуктом синтеза жирных кислот, уровень которого регулируется циркулирующим в крови глюкаго-ном. При накоплении последнего происходит нарушение образования малонил-КоА как вследствие блокирования гликолиза, так и из-за снижения активности малонил-КоА карбоксилазы. В результате увеличивается активность фермента карнитин-пальмитоилтрансферазы. Следствием этих процесов является поступление в митохондрии большого количества жирных кислот с последующим усилением активности кетогенеза. При этом в основном образуются ацетоуксусная кислота и р-гид-роксибутират.
Печень также принимает активное участие в биосинтезе фосфолипидов и липо-протеидов.
В норме печень содержит небольшие запасы жиров. В отдельных случаях возможно патологическое отложение жиров в органе. Это может быть обусловлено или нарушением их метаболизма при нормальном поступлении жиров в печень, или избыточным поступлением жиров на фоне нормальных процессов метаболизма в печеночной клетке. Типичными, причинами жировой инфильтрации печени являются: 1. Воздействие на печень токсикантов, в частности этанола, хлороформа, четырех-хлористого углерода. 2. Инфекционное поражение печени. 3. Поражение печени злокачественным процессом. 4. Избыточное поступление жиров в печень из тканевых депо при голодании, сахарном диабете. 5. Избыточное поступление углеводов в организм при парентеральном питании. 6. Пища, содержащая недостаточное количество белка.
6.2.4. Билирубин и его циркуляция
80 % всей массы билирубина образуется в результате разрушения эритроцитов в системе мононуклеарных фагоцитов, преимущественно селезенки. Высвобождаемый гемоглобин расщепляется до глобина, поступающего в общий фонд белков, и гема, превращающегося в билирубин после потери железа, которое затем используется повторно. К числу других источников билирубина относятся: распад незрелых эритроцитов в тканях костного мозга, а также близких к гемоглобину по составу и свойствам миоглобина и цитохромов.
Образовавшийся в результате распада эритроцитов билирубин называют свободным неконъюгированным билирубином (это билирубин, которому еще не придана водорастворимость в результате конъюгации с глюкуронатом в печени). Он связывается с альбумином плазмы. Вследствие этого билирубин не может проникать ни через почечные клубочки в мочу, ни через биомембраны мозга. Но при низком содержании альбумина в плазме, вытеснении из билирубина связи с альбумином (в том числе и под действием лекарственных соединений), а также при нарушении (незрелости — у новорожденных) механизмов конъюгации в печени в плазме увеличивается фракция свободного неконъюгированного билирубина, который растворим в липидах, проникает через гематоэнцефа-лический барьер и вызывает токсическое повреждение ткани мозга.
В печени происходит перенос билирубина от альбумина плазмы через свобод-нопроницаемую мембрану сосудистых синусов в гепатоциты. Этот процесс осуществляется с помощью транспортных белков. Перенос билирубина происходит быстро вследствие наличия в цитозоле связывающих белков, а также благодаря его быстрому последующему метаболизму в гепа-тоците в реакции глюкуронидизации и выделению в желчь.
В гепатоците происходит активный транспорт поступившего билирубина в гладкий эндоплазматический ретикулум и конъюгация его с глюкуроновой кислотой в ходе процесса, катализируемого уридин-дифосфат-глюкуронилтрансферазой. При печеночно-клеточной желтухе активность этого фермента поддерживается на достаточном уровне, а при холестазе — увеличивается. Однако у новорожденных активность фермента снижена. Дефицит функции конъюгирующих ферментов является основой таких семейных негемолитических гипербилирубинемий, как синдромы Жильбера и Криглера —Найяра. Билирубин-моноглюкуронид поступает к обращенной в сторону желчных канальцев поверхности гепатоцита, где после присоединения второго остатка глюкуро-ната образуется диглюкуронид билирубина, который активно секретируется в желчные канальцы. Последующий транспорт зависит от нормального оттока желчи, а также от состояния транспортных белков. Экскреция билирубина в канальцы происходит с помощью семейства АТФ-зави-симых мультиспецифичных для органических анионов транспортных белков. Желчные кислоты переносятся в желчь также с помощью другого транспортного белка. Наличие разных механизмов транспорта билирубина и желчных кислот обуславливает клиническую картину синдрома Дубина —Джонсона, при котором нарушается экскреция конъюгированного билирубина, но сохраняется нормальная экскреция желчных кислот.
При поражениях печени и повышении давления в желчевыводящих путях наиболее высока вероятность нарушения именно процессов секреции билирубина в желчные протоки, требующих затраты энергии. Поэтому повышение концентрации конъюгированного билирубина в плазме является наиболее ранним проявлением нарушения его экскреции. При печеночной желтухе, как правило, в плазме повышено содержание обеих фракций билирубина, но преобладает конъюгированный, который растворим в воде, менее прочно, чем свободный, связывается с белками и может экскретироваться с мочой.
Конъюгированный билирубин поступает в кишки с желчью. Диглюкуронид билирубина водорастворим (полярная молекула), поэтому в тонкой кишке не всасывается. В толстой кишке конъюгированный билирубин подвергается гидролизу р-глюкуронидазами бактерий до соединений, обозначаемых собирательным термином стеркобилиноген (или уробилиноген кала). При бактериальном холангите часть диглюкуронида билирубина гидролизуется уже в желчных путях с последующей преципитацией билирубина. Этот процесс может играть важную роль в образовании билирубиновых желчных камней.
Небольшая часть стеркобилиногена всасывается, попадает в систему портального кровообращения и преимущественно вновь экскретируется с желчью; очень небольшая его фракция экскретируется с мочой в виде уробилиногена, который, в свою очередь, может быть окислен до уробилина. Уробилин (оген) в отличие от билирубина часто обнаруживается в моче здоровых лиц, особенно в тех случаях, когда экскретируется концентрированная моча. У здорового человека экскреция уробилиногена с мочой настолько изменчива, что клинически значимо только обнаружение очень высокой концентрации уробилиногена в моче во время острых приступов гемолиза.
Неабсорбированный стеркобилиноген окисляется до стеркобилина — пигмента, придающего калу коричневую окраску. Поэтому малоокрашенные фекалии рассматриваются как признак закупорки желчных протоков. Билирубин, уробилин и стер-кобилин (желчные пигменты) — окрашены. Уробилиноген и стеркобилиноген — бесцветны.
Конъюгированный и неконъюгирован-ный билирубин иногда обозначают соответственно терминами «прямой» и «непрямой билирубин».
6.2.5. Влияние анестезии на метаболические функции печени
Стресс, оперативное вмешательство сопровождаются повышением концентрации гормонов стресса (катехоламины, глюка-гон, кортизол) и одновременным снижением анаболических гормонов (инсулин, тестостерон). В результате катаболизм доминирует над анаболизмом. Это проявляется увеличением интенсивности распада белков, образования мочевины, снижением синтеза белков, повышением концентрации глюкозы. Последнее обусловлено активацией гликогенолиза и глюконеоге-неза. Энергетическую ценность образующейся в результате глюконеогенеза глю
■ козы иллюстрируют следующие реакции:
2 Лактат + 6 АТФ ► Глюкоза;
Глюкоза ► 2 Лактат + 2 АТФ.
Метаболизм жиров под влиянием оперативного вмешательства изменяется в меньшей степени. Степень этих отклонений зависит от эффективности анестезии: при использовании регионарных методов анестезии, предотвращающих поступление ноцицептивной информации в централь-
■ ную нервную систему, она меньше.
[ Непосредственному влиянию средств для
■ наркоза на метаболизм в печени посвяще-
ны лишь единичные исследования. Так,
оказалось, что фторотан нарушает потреб-
ление кислорода в цикле синтеза мочеви-
- ны, глюконеогенез, усвоение лактата, содер- i жащегося в плазме. При использовании
- этого анестетика может повыситься концен-
■ трация молочной кислоты в крови. В экс- > периментальных исследованиях на куль-
- турах клеток также выявлено, что фторо-
■ тан и энфлуран могут угнетать синтез бел-
- ков в печеночной клетке.
