
- •Міністерство охорони здоров’я України
- •Контрольні завдання
- •Сучасна номенклатура неорганічних сполук і їх взаємні перетворення. Стехіометричні розрахунки
- •Приклади розв'язування задач
- •Контрольні питання
- •Будова атомів та періодичний закон д.І. Менделєєва
- •Приклади розв'язування задач
- •Контрольні питання
- •Хімічний зв'язок і будова молекул. Конденсований стан речовини
- •Приклади розв'язування задач
- •Контрольні питання
- •Основні закономірності протікання хімічних реакцій. Елементи хімічної термодинаміки і термохімії
- •Приклади розв'язування задач
- •Стандартні ентальпії утворення δн0298, ентропії s0298 і енергії Гіббса δg0298 деяких речовин при 298 к (25°с).
- •Контрольні питання
- •Хімічна кінетика і рівновага
- •Приклади розв’язування задач
- •Контрольні питання
- •Розчини. Коцентрація розчинів
- •Приклади розв’язування задач
- •Контрольні питання
- •Властивості розчинів
- •Контрольні питання
- •Окислювально-відновні реакції. Електрохімічні процеси
- •Слід пам’ятати, що:
- •Правила підбору коефіцієнтів у окислювально-відновних реакціях.
- •Приклади розв’язування задач
- •Контрольні питання
- •Гідроліз солей. Відновний показник (рН)
- •Приклади розв'язування задач
- •Контрольні питання
- •Додаток № 1
- •Константи дисоціації деяких слабких електролітів у водних розчинах при 25°с.
- •Додаток № 2
- •Стандарті електродні потенціали деяких металів у водних розчинах.
- •Література
- •69035, Г. Запорожье, пр. Маяковского, 26
Приклади розв'язування задач
Приклад 1. Пояснити утворення хімічного зв'язку в молекулі О2 на основі методу ВЗ та МО ЛКАО, охарактеризувати магнітні властивості молекули.
Розв'язування: а) МВЗ. У цьому випадку від кожного атома кисню в утворенні зв'язку беруть участь 2s22p4-валентні електрони. Графічно можна зобразити:

б) МО ЛКАО. У даному випадку слід пам'ятати, що МО (молекулярні орбіталі) у порядку зростання енергії розташовані так (наприклад, для молекул Li2→N2, а також ізоелектронних до N2 — CO, CN- та ін.):
Тоді як для молекул O2→Ne2 порядок розташування:
![]()
Графічне зображення за МО ЛКАО:
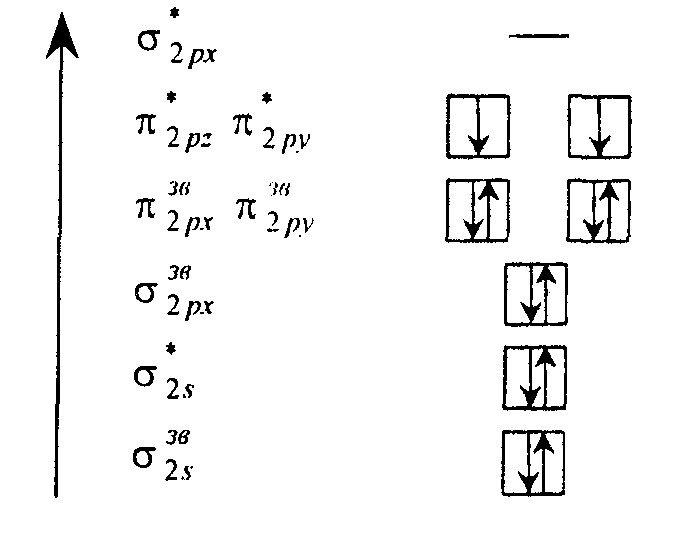
У
молекул кисню 12 електронів. Обчислимо
порядок (кратність)
зв'язку:
![]() ,
де
nзв
– кількість електронів на зв'язуючих
орбіталях і π*
— на розпушуючих.
,
де
nзв
– кількість електронів на зв'язуючих
орбіталях і π*
— на розпушуючих.
Наявність двох неспарених електронів на π 2pz і π 2py обумовлює парамагнітні властивості молекули кисню (ця речовина втягується зовнішнім магнітним полем, тоді як діамагнітні, що містять спарені електрони, виштовхуються ним). Парамагнітна сприйнятливість має позитивний знак, а діамагнітна — негативний.
Феромагнітні речовини мають високу магнітну сприйнятливість (Fe, Co, Ni).
Таким чином, метод валентних зв'язків не дає можливості пояснити магнітні властивості молекули О2 (оскільки утворюється дві електронні пари неспарених електронів немає). Крім того, МО ЛКАО може пояснити також утворення різних молекулярних іонів, наприклад, Н2+, О2+, О2-, О22-, їх стабільність і можливість існування, тоді як використання МВЗ не дає можливості пояснити ці властивості.
Приклад 2. За МВЗ пояснити утворення донорно-акцепторного зв'язку в іонах NH4+ та ВН4-.
Розв'язування: Від атома азоту в утворенні зв'язку беруть участь 2s22p3 електрони, від атома водню — 1s1. Отже, у випадку утворення молекули NН3 це графічно можна зобразити так:

В іоні водню (Н+) є вільна атомна орбіталь (1s1), а в молекулі NH3 — пара електронів (2s1), що дас можливість утворити донорно-акцепторний зв'язок: NН3 + Н+ → NH4+, де атом азоту — донор, іон водню (NH4+) —- акцептор.
Аналогічно утворюється донорно-акцепторний зв'язок в іоні ВН4-: ВН3 + Н- → ВН4-, де Н- — донор, а ВН3 — акцептор. Графічно це можна зобразити так:

Атом бору має вакантну р-орбіталь, а гідрід-іон (Н+) — неподілену пару електронів.
Приклад 3. Пояснити утворення гібридизованих sp3-орбіталей у молекулі СН4.
Розв'язування: у збудженому стані атом вуглецю С має таку електронну конфігурацію валентних електронів:

У даному випадку з чотирьох АО (s1p3) утворюються чотири гібридизовані sp3-орбіталі, з ними перекриваються 1s1-орбіталі чотирьох атомів водню. Утворюється тетраедрична молекула СН4:
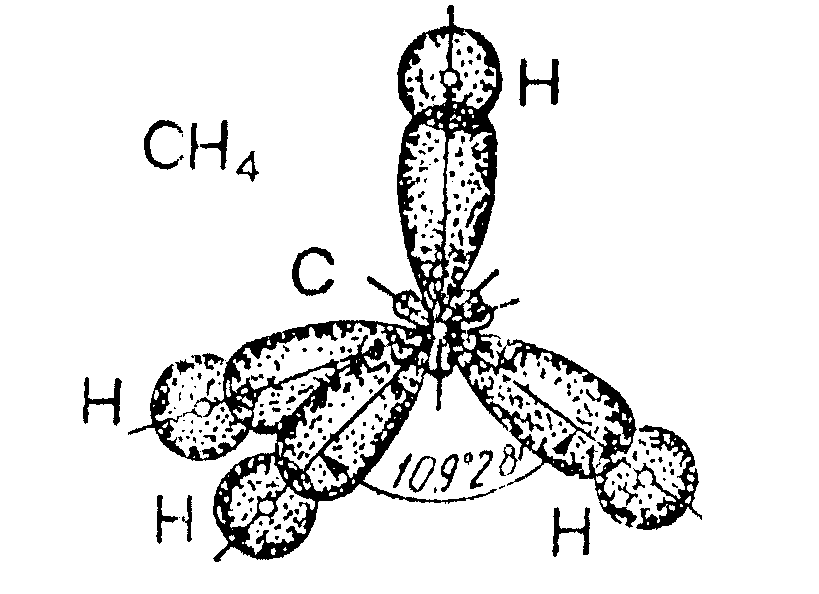
Приклад 4. Пояснити утворення МО у молекулі Н2 з АО (у вигляді діаграми енергетичного стану електронів у двоатомних гомоядсрних частинках).

Приклад 5. Записати електронну конфігурацію молекули CO.
Розв'язування:
Електронна конфігурація атомів вуглецю
і кисню - С 1s22s22p2,
О
1s22s22p4,
всього
14 електронів. Тоді СО[КК(![]() )2(
)2(![]() )2=(
)2=(![]() )2=(
)2=(![]() )2(
)2(![]() )2].
)2].
Кратність зв'язку дорівнює ½(nзв - n*) = ½(8 - 2) = 3.
КК
— це 1s2
атома
C
i
1s2
атома О, тобто (![]() )2(
)2(![]() )2.
)2.
Аналогічну будову мають N2, CN-.
Приклад 6. Чи існує молекула Ne2?
Розв'язування: Електронна формула Ne — 1s22s22p6.
У молекулі Ne2 — 16 електронів (другий енергетичний рівень), які розселюються на 8 МО (див. приклад 1). Тоді кратність зв’язку буде дорівнювати: ½(nзв – n*) = ½(8 - 8) = 0. Якщо кратність зв'язку дорівнює нулю, молекула існувати не може. Справді, благородні гази утворені одноатомними молекулами.
