
- •1.Эквивалент. Эквивалентная масса. Эквивалентный объём. Закон эквивалентов.
- •2.Примеры расчёта эквивалента элемента, оксида, основания, соли, кислоты, окислителя, восстановителя.
- •4.Энергия Гиббса. Направленность самопроизвольных химических реакций.
- •12.Способы выражения состава растворов.
- •13.Осмос. Закон Вант-Гоффа. Роль осмоса в биологических явлениях.
- •14.Давление пара растворителя над раствором. Закон Рауля.
- •15.Кипение и замерзание растворов неэлектролитов.
- •Вопрос 16.
- •Вопрос 17.
- •34. Виды межмолекулярного взаимодействия.
- •35. Водородная связь, ее биологическая роль.
- •36. Комплексные соединения. Теория Вернера. Роль в живом организме.
- •37. Диссоциация комплексных соединений. Константа нестойкости комплексных ионов.
- •38. Химическая связь в комплексных соединениях (примеры).
- •39. Окислительно-восстановительные реакции. Виды окислительно-восстановительных реакций.
- •40. Важнейшие окислители и восстановители. Окислительно-восстановительная двойственность.
- •41. Стандартные электродные потенциалы. Направление протекания окислительно-восстановительных реакций.
- •II. Химия неорганических соединений, биологическая роль, применение в ветеринарии.
- •2. Способы получения галогенов. Применение.
- •3. Водородные соединения галогенов. Свойства, применение.
- •4. Хлорная вода. Получение, свойства, применение.
- •5. Хлорная известь. Получение, свойства, применение.
- •6. Кислородсодержащие кислоты галогенов. Изменение их силы и окислительной способности. Соли кислородсодержащих кислот. Применение.
- •7. Общая характеристика подгруппы кислорода.
- •8. Вода. Физические и химические свойства. Вода как растворитель. Биологическая роль воды.
- •9. Сероводород, получение и свойства. Сероводородная кислота. 1-я и 2-я константы диссоциации. Роль в окислительно-восстановительных процессах. Соли сероводородной кислоты.
34. Виды межмолекулярного взаимодействия.
1) ориентационные(полярные молекулы вследствие электростатического взаимодействия разноименных концов диполей ориентируются с пространстве так, что отрицательные концы диполей одних молекул повернуты к положительным концам диполей других молекул )
2) индукционные(наблюдаются также и у веществ с полярными молекулами, но при этом оно обычно значительно слабее ориентационного. Полярная молекула может увеличивать полярность соседней молекулы. Иными словами, под влиянием диполя одной молекулы может увеличиваться диполь другой молекулы, а неполярная молекула может стать полярной)
3) дисперсионные(эти силы взаимодействуют между любыми атомами и молекулами независимо от их строения. Они вызываются мгновенными дипольными моментами, согласованно возникающими в большой группе атомов)
35. Водородная связь, ее биологическая роль.

36. Комплексные соединения. Теория Вернера. Роль в живом организме.



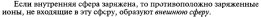
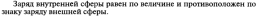

37. Диссоциация комплексных соединений. Константа нестойкости комплексных ионов.


38. Химическая связь в комплексных соединениях (примеры).
В кристаллических комплексных соединениях с заряженными комплексами связь между комплексом и внешнесферными ионами ионная, связи между остальными частицами внешней сферы –межмолекулярные(в том числе и водородные). В большинстве комплексных частиц между центральным атомом и лигандами связиковалентные. Все они или их часть образованы по донорно-акцепторному механизму (как следствие – с изменением формальных зарядов). В наименее прочных комплексах (например, в аквакомплексах щелочных и щелочноземельных элементов, а также аммония) лиганды удерживаются электростатическим притяжением. Связь в комплексных частицах часто называют донорно-акцепторной или координационной связью.
39. Окислительно-восстановительные реакции. Виды окислительно-восстановительных реакций.

Виды окислительно-восстановительных реакций:
1) Межмолекулярные— реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных веществ, например:
Н2S + Cl2 → S + 2HCl
2) Внутримолекулярные— реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах одного и того же вещества, например:
2H2O → 2H2 + O2
3) Диспропорционирование (самоокисление-самовосстановление) — реакции, в которых один и тот же элемент выступает и как окислитель, и как восстановитель, например:
Cl2 + H2O → HClO + HCl
4) Репропорционирование — реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления, например:
NH4NO3 → N2O + 2H2O
40. Важнейшие окислители и восстановители. Окислительно-восстановительная двойственность.
|
Восстановители |
Окислители |
|
Металлы |
Галогены |
|
Водород |
Перманганат калия(KMnO4) |
|
Уголь |
Манганат калия (K2MnO4) |
|
Окись углерода (II) (CO) |
Оксид марганца (IV) (MnO2) |
|
Сероводород (H2S) |
Дихромат калия (K2Cr2O7) |
|
Оксид серы (IV) (SO2) |
Хромат калия (K2CrO4) |
|
Сернистая кислота H2SO3и ее соли |
Азотная кислота (HNO3) |
|
Галогеноводородные кислоты и их соли |
Серная кислота (H2SO4) конц. |
|
Катионы металлов в низших степенях окисления: SnCl2, FeCl2, MnSO4, Cr2(SO4)3 |
Оксид меди(II) (CuO) |
|
Азотистая кислота HNO2 |
Оксид свинца(IV) (PbO2) |
|
Аммиак NH3 |
Оксид серебра (Ag2O) |
|
Гидразин NH2NH2 |
Пероксид водорода (H2O2) |
|
Оксид азота(II) (NO) |
Хлорид железа(III) (FeCl3) |
|
Катод при электролизе |
Бертоллетова соль (KClO3) |
|
Металлы |
Анод при электролизе |

