
- •Государственное образовательное учреждение
- •Раздел 1. Введение в биохимию…………………………………..…..…...5
- •Раздел 1. Введение в биохимию.
- •Раздел 2. Белки: структура, свойства, функции.
- •Раздел 3. Ферменты: структура, свойства, регуляция активности.
- •При аллостерическом ингибировании активности ферментов:
- •Раздел 4. Синтез белка.
- •Раздел 5. Цикл трикарбоновых кислот.
- •Раздел 6. Энергетический обмен.
- •Раздел 7. Биохимия гормонов.
- •Раздел 8. Обмен углеводов.
- •Разел 9. Обмен липидов.
- •Раздел 10. Обмен белков.
- •Раздел 11. Биохимия печени.
- •Раздел 12. Биохимия крови.
- •Раздел 13. Биохимия соединительной ткани.
- •Раздел 14. Биохимия мышечного сокращения.
- •Раздел 15. Биохимия ротовой полости.
- •Ответы. Ответы к разделу 1:
- •Ответы к разделу 2:
- •Ответы к разделу 4:
- •Ответы к разделу 5:
- •Ответы к разделу 6:
- •Ответы к разделу 7:
- •Ответы к разделу 8:
- •Ответы к разделу 9:
- •Ответы к разделу 12:
- •12.1 2→1→3
- •Ответы к разделу 13:
- •Ответы к разделу 14:
- •Ответы к разделу 15:
При аллостерическом ингибировании активности ферментов:
уменьшается скорость реакции;
изменяется конформация фермента;
эффектор присоединяется в активном центре фермента;
нарушается комплиментарность активного центра субстрату;
эффектор присоединяется в аллостерическом центре;
изменяется конформация активного центра.
Участок фермента, стереохимически комплементарный субстрату - это:
аллостерический центр;
регуляторный центр;
активный центр;
адсорбционный центр.
Оптическая специфичность – это:
способность фермента действовать на определенные связи в большом количестве субстратов;
способность фермента воздействовать на определенный участок субстрата;
способность фермента катализировать превращение одного изомера субстрата;
способность фермента катализировать реакции одного типа.
Трансферазы -это:
ферменты, катализирующие перенос групп с субстрата на субстрат;
ферменты, катализирующие перенос одноуглеродных фрагментов;
ферменты, катализирующие перенос групп внутри субстратов;
ферменты, катализирующие перенос альдегидных и кетонных группировок.
В состав активного центра входят:
аминокислоты с функциональными группировками;
все аминокислоты;
определенные аминокислоты, расположенные в полипептидной цепи вдали друг от друга и приближенные друг к другу;
несколько аминокислот, расположенных в полипептидной цепи непосредственно друг около друга.
К особенностям ферментативного катализа относятся:
исходная активность при низкой температуре;
высокие кинетические параметры;
специфичность действия;
высокая скорость реакции;
разнообразие реакций при отсутствии специфичности.
Абсолютная специфичность - это:
способность фермента воздействовать на определенную часть молекулы субстрата;
способность фермента катализировать только одну реакцию;
способность фермента катализировать превращение одного субстрата.
Групповая специфичность – это:
способность фермента воздействовать на определенную часть молекулы субстрата;
способность фермента катализировать превращения одного субстрата;
способность фермента действовать на определенные связи в большом числе субстратов;
способность фермента катализировать реакции одного типа.
П
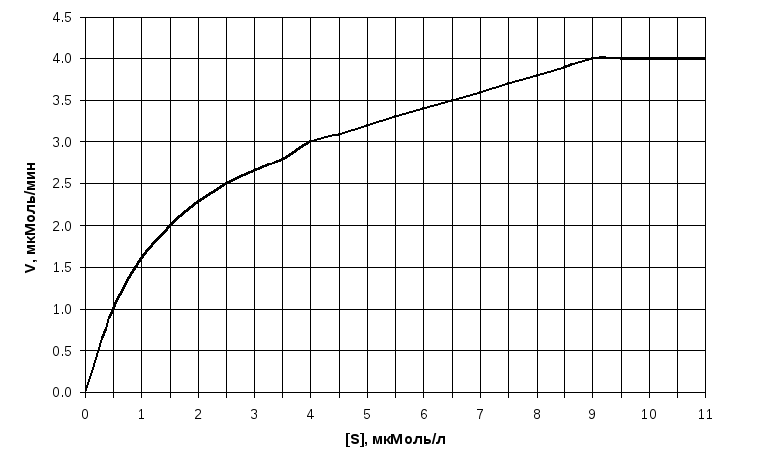 о
графику зависимости скорости реакции
от концентрации субстрата определите
Км этого фермента:
о
графику зависимости скорости реакции
от концентрации субстрата определите
Км этого фермента:
0,5
1
1,5
2,5
3
На рисунке изображен график зависимости скорости реакции от концентрации субстрата.
О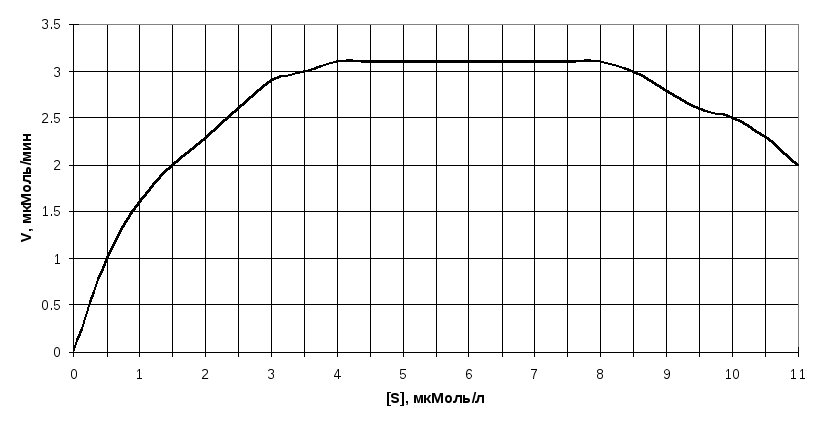 пределите
тип ингибирования:
пределите
тип ингибирования:
Конкурентное.
Неконкурентное.
Бесконкурентное.
Субстратное.
3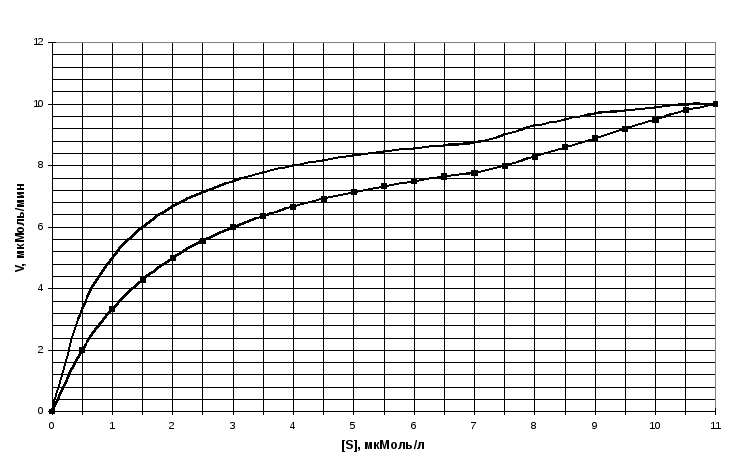

 .112.
На рисунке изображены графики
зависимости скорости реакции от
концентрации субстрата. А – без действия
ингибитора; Б – с добавлением ингибитора.
.112.
На рисунке изображены графики
зависимости скорости реакции от
концентрации субстрата. А – без действия
ингибитора; Б – с добавлением ингибитора.
Определите тип ингибирования:
Конкурентное.
Неконкурентное.
Бесконкурентное.
Субстратное.
3 .113.
На рисунке изображены графики
зависимости скорости реакции от
концентрации субстрата. А – без действия
ингибитора; Б – с добавлением ингибитора.
.113.
На рисунке изображены графики
зависимости скорости реакции от
концентрации субстрата. А – без действия
ингибитора; Б – с добавлением ингибитора.
Определите тип ингибирования:
Конкурентное.
Неконкурентное.
Бесконкурентное.
Субстратное.
