
- •Ионная полимеризация
- •Катионная полимеризация
- •Анионная полимеризация.
- •Собственно анионная полимеризация
- •Анионно-координационная полимеризация.
- •Полимеризация с вероятным образованием карбенов
- •Миграционная полимеризация
- •Полициклоприсоединение
- •Стро.Ение мономеров и их способность к полимеризации
- •Практические способы проведения полимеризации
Ионная полимеризация
Ионная полимеризация, как и радикальная, является разновидностью цепной полимеризации; поэтому, механизмы ионной полимеризации, как и радикальной, включают стадии инициирования, роста и обрыва цепей. В рамках этой общей схемы реакции ионной полимеризации имеют много специфических особенностей, отличающих их от радикальных процессов. Эти особенности можно свести к следующему:
1. Для инициирования процессов ионной полимеризации используют не инициаторы, а катализаторы. Разница между ними в том, что фрагменты инициатора входят в состав полимера (в виде концевых групп, см. выше), а катализатор, естественно, не входит в состав продукта реакции.
2. Энергия активации процессов ионной полимеризации во многих случаях заметно ниже, чем радикальных процессах, что позволяет проводить эти процессы при обычных и даже минусовых температурах.
3. В то время, как реакции радикальной полимеризации проводят в разных системах – в блоке, растворе, эмульсии, суспензии – ионную полимеризацию, как правило, проводят в растворах. Ионные процессы, в отличие от радикальных, весьма чувствительны к природе растворителя – при изменении природы растворителя, например, его полярности, может измениться характер активных центров (допустим, происходить переход от ионных пар к свободным ионам). Вследствие этого значительно изменяются параметры процесса. Поэтому кинетические характеристики процессов ионной полимеризации более разнообразны и сложны, чем для радикальных процессов.
4. Обрыв цепи при реакциях ионной полимеризации, в отличие от радикальных, не может происходить при встрече двух «живых» цепей, т.к. эти цепи одноименно заряжены. Обрыв цепей здесь происходит при взаимодействии «живых» цепей с какими-либо другими частицами – либо присутствующими в реакционной смеси (катализатор, растворитель), либо специально добавленными. В целом ряде случаев обрыв цепи затруднен, а отдельных случаях просто не происходит, и после исчерпания мономера полученный полимер состоит из «живых» цепей. Если к такому полимеру добавить новую порцию мономера, полимеризация возобновляется, а если добавить другой мономер, образуется блок-сополимер; этот вариант весьма полезен.
5. Процессы ионной полимеризации в гораздо большей степени, чем радикальные, способствуют получению стереорегулярных полимеров; отдельные процессы позволяют получить полностью стереорегулярные полимеры; как уже упоминалось (стр. 6), такие полимеры обладают наиболее ценными свойствами.
6. Круг мономеров при реакциях ионной полимеризации несколько шире, чем при радикальной – по ионным механизмам полимеризуются не только винильные мономеры и диены, но и некоторые циклические мономеры.
В зависимости от характера активных центров ионная полимеризация подразделяется на катионную и анионную. В некоторых случаях при инициировании возникают ион-радикалы; однако, дальнейший рост цепи, как правило, протекает по ионным механизмам, поэтому эти процессы рассматриваются как ионные.
Катионная полимеризация
В этих процессах активный центр – катион. Чаще всего это карбокатион (катион карбения); такие центры возникают при полимеризации винильных мономеров. В некоторых случаях (при полимеризации циклических мономеров) возникают также ониевые (оксониевые, сульфониевые) катионы.
По катионным механизмам полимеризуются: А. Винильные мономеры, содержащие при связи С=С электронодонорные заместители - изобутилен, алкилвиниловые эфиры. Причина понятна: донорные заместители стабилизируют катионы и облегчают их образование. Стирол также легко полимеризуется по катионному механизму, как и по анионному и радикальному – бензольное ядро стабилизирует и катионы и анионы и радикалы; вообще, стирол можно считать наиболее универсальным из широко применяемых мономеров. Б. Циклические мономеры, содержащие гетероатомы с неподеленными электронными парами (циклические простые эфиры, сульфиды и др.)
Есть несколько вариантов инициирования ионной полимеризации, которые можно разделить на чисто катионное и катион-радикальное. Чисто катионное инициирование в настоящее время является преобладающим вариантом.
Процессы с чисто катионным инициированием. Катализаторами этих процессов являются электронодефицитные частицы – кислоты Льюиса; они «отбирают» пару электронов у мономера, превращая его в катион. Кислоты Льюиса могут быть протонными (конц. H2SO4, НС1О4), но значительно чаще используются апротонные кислоты Льюиса (BF3, AlCl3, TiCl4 и др.). При использовании апротонных кислот Льюиса необходимо присутствие сокатализатора, обычно в малых количествах, часто следовых. В качестве сокатализаторов могут использоваться вода, протонные кислоты (НС1 и др.), иногда галогенпроизводные. Наиболее вероятная гипотеза, объясняющая роль сокатализаторов – образование активного комплексного соединения из молекул катализатора и сокатализатора:
BF3 + HOH → H+[BF3OH]‾
TiCl4 + HCl → H+[TiCl5]‾
AlCl3 + R– Cl → R+[AlCl4] ‾
Именно это комплексное соединение инициирует катионную полимеризацию
Полимеризация винильных мономеров под действием апротонных кислот Льюиса.
А. Инициирование процесса – взаимодействие каталитического комплекса с молекулой мономера:
К атионная
часть комплекса (в данном случае –
протон) присоединяется к молекуле
мономера (это – первая стадия обычного
электрофильного присоединения к связи
С=С). Молекула мономера превращается в
карбокатион; донорный заместитель Х
стабилизирует его. Этот катион и
противоион (в данном случае [BF3OH]ˉ)
в большинстве случаев образуют ионную
пару, а не
находятся в виде свободных ионов, т.к.
чаще всего полимеризацию проводят в
малополярных
растворителях (пентан, метиленхлорид),
не способствующих полной диссоциации.
атионная
часть комплекса (в данном случае –
протон) присоединяется к молекуле
мономера (это – первая стадия обычного
электрофильного присоединения к связи
С=С). Молекула мономера превращается в
карбокатион; донорный заместитель Х
стабилизирует его. Этот катион и
противоион (в данном случае [BF3OH]ˉ)
в большинстве случаев образуют ионную
пару, а не
находятся в виде свободных ионов, т.к.
чаще всего полимеризацию проводят в
малополярных
растворителях (пентан, метиленхлорид),
не способствующих полной диссоциации.
Энергия активации инициирования здесь значительно меньше, чем для процессов радикальной полимеризации и имеет величину не выше 60 кДж/моль. Единовременная концентрация активных центров здесь выше, чем при радикальных процессах и имеет величину порядка 10-3.
Б. Рост цепи аналогичен росту цепи при радикальной полимеризации: последовательно протекают реакции присоединения активного центра к молекулам мономера:
Р астущая
цепь («живой» полимер) – ионная пара,
содержащая полимерный катион (при
достаточной величине – макрокатион),
в котором положительный заряд находится
на конце цепи. При каждой элементарной
реакции роста цепи молекула мономера
как бы внедряется между катионом и
противоионом. Мономерные звенья
соединяются друг с другом практически
всегда по схеме «голова к хвосту», т.к.
при такой схеме образуются намного
более устойчивые карбокатионы (более
замещенные и к тому же связанные с
электронодонорными заместителями).
астущая
цепь («живой» полимер) – ионная пара,
содержащая полимерный катион (при
достаточной величине – макрокатион),
в котором положительный заряд находится
на конце цепи. При каждой элементарной
реакции роста цепи молекула мономера
как бы внедряется между катионом и
противоионом. Мономерные звенья
соединяются друг с другом практически
всегда по схеме «голова к хвосту», т.к.
при такой схеме образуются намного
более устойчивые карбокатионы (более
замещенные и к тому же связанные с
электронодонорными заместителями).
В. Обрыв цепи. Как уже упоминалось, превращение «живой» цепи в «мертвый» полимер происходит совсем по иным схемам, нежели при радикальной полимеризации. Один из путей - взаимодействие макрокатиона со своим противоионом. В наибольшей степени
понятию обрыва кинетической цепи соответствует взаимодействие с передачей макрокатиону фрагмента сокатализатора; здесь исчезают активные центры:

 Однако взаимодействие может идти и
другим путем – с передачей протона от
макрокатиона к противоиону:
Однако взаимодействие может идти и
другим путем – с передачей протона от
макрокатиона к противоиону:
Здесь регенерируется каталитический комплекс, который может инициировать рост новой полимерной цепи. Это взаимодействие обратимо, поэтому после окончания полимеризации часть цепей может оказаться живой. В отличие от радикальной полимеризации энергия активации реакций обрыва цепи выше энергии активации роста цепи.
Обрыв молекулярных цепей довольно часто идет по схеме передачи цепи.
Реакции передачи цепи при катионной полимеризации винильных мономеров. Аналогично радикальной полимеризации, здесь происходят реакции передачи цепи на мономер, на посторонние молекулы и на полимер.
 А.
Передача
цепи на мономер. Этот
вид передачи встречается чаще, чем при
радикальной полимеризации. Наиболее
типичная схема передачи – передача
протона от макрокатиона к молекуле
мономера:
А.
Передача
цепи на мономер. Этот
вид передачи встречается чаще, чем при
радикальной полимеризации. Наиболее
типичная схема передачи – передача
протона от макрокатиона к молекуле
мономера:
 Б.
Передача
цепи на посторонние молекулы. Передача
на растворитель для катионной полимеризации
не особенно характерна – в большинстве
случаев используются растворители,
устойчивые к электрофильной атаке
макрокатиона. Однако вполне возможна
передача на специально введенные
соединения; в качестве таких передатчиков
могут использоваться нуклеофилы
– соединения,
содержащие атомы с неподеленными
электронными парами: вода, спирты, амины,
карбоновые кислоты. Передача идет по
схеме:
Б.
Передача
цепи на посторонние молекулы. Передача
на растворитель для катионной полимеризации
не особенно характерна – в большинстве
случаев используются растворители,
устойчивые к электрофильной атаке
макрокатиона. Однако вполне возможна
передача на специально введенные
соединения; в качестве таких передатчиков
могут использоваться нуклеофилы
– соединения,
содержащие атомы с неподеленными
электронными парами: вода, спирты, амины,
карбоновые кислоты. Передача идет по
схеме:
Передатчики такого типа могут использоваться для перевода «живых» цепей в «мертвый» полимер, если при полимеризации обрыв не происходит, и после окончания процесса сохраняются «живые» цепи.
В. Передача цепи на полимер. Здесь возможны два варианта: 1. Взаимодействие «живой» цепи с «мертвым» полимером; 2. Внутримолекулярная передача цепи.
Взаимодействие «живой» цепи с «мертвым» полимером. Этот вариант аналогичен передаче цепи на полимер при радикальной полимеризации; разница в том, что от «мертвой» цепи к «живой» переходит атом водорода не с одним электроном («атомарный водород»), а с двумя электронами (условно называемый гидрид-ионом):
В результате, как и при радикальной
полимеризации, образуетсяразветвление;
боковая цепь обычно полимерная.
Естественно, вероятность такой передачи
растет с увеличением глубины процесса.
результате, как и при радикальной
полимеризации, образуетсяразветвление;
боковая цепь обычно полимерная.
Естественно, вероятность такой передачи
растет с увеличением глубины процесса.
Внутримолекулярная передача цепи. При катионной полимеризации возможен еще один тип передачи цепи, мало характерный для радикальных процессов: это внутримолекулярная передача «гидрид-иона» от третьего с конца звена «живой» цепи к концевому катиону (от С5 к С1):
Т акая
передача приводит к превращениюменее
замещенного карбокатиона
(структура 23) в более
устойчивый полностью замещенный
карбокатион
(структура 24); это – перегруппировка с
«гидридным сдвигом», достаточно хорошо
известная в «классической» органической
химии. Передача идет именно от третьего
с конца звена потому, что в этом случае
она протекает через стерически выгодное
6-членное переходное состояние. После
передачи рост кинетической (и молекулярной)
цепи продолжается, а два бывших концевых
звена (включающие атомы С1
– С4)
образуют двухзвенное
ответвление. Разумеется,
такая внутримолекулярная передача цепи
идет при полимеризации монозамещенных
производных этилена, но не 1,1-дизамещенных,
т.к. из 1,1-дизамещенных этилена сразу
образуются максимально замещенные
концевые карбокатионы, и перегруппировка
уже невыгодна.
акая
передача приводит к превращениюменее
замещенного карбокатиона
(структура 23) в более
устойчивый полностью замещенный
карбокатион
(структура 24); это – перегруппировка с
«гидридным сдвигом», достаточно хорошо
известная в «классической» органической
химии. Передача идет именно от третьего
с конца звена потому, что в этом случае
она протекает через стерически выгодное
6-членное переходное состояние. После
передачи рост кинетической (и молекулярной)
цепи продолжается, а два бывших концевых
звена (включающие атомы С1
– С4)
образуют двухзвенное
ответвление. Разумеется,
такая внутримолекулярная передача цепи
идет при полимеризации монозамещенных
производных этилена, но не 1,1-дизамещенных,
т.к. из 1,1-дизамещенных этилена сразу
образуются максимально замещенные
концевые карбокатионы, и перегруппировка
уже невыгодна.
Катионная полимеризация циклических мономеров.
По катионному механизму способны полимеризоваться некоторые гетероциклические мономеры, прежде всего, циклические простые эфиры, такие, например, как тетрагидрофуран. Полимеризация таких мономеров, как и винильных, также чаще всего катализируется неорганическими кислотами Льюиса (с сокатализаторами). При взаимодействии каталитического комплекса с циклическим мономером происходит инициирование – присоединение протона к гетероатому мономера с образованием ониевого катиона:
Р ост
цепичаще
всего происходит при взаимодействии
ониевого катиона с очередной молекулой
мономера:
ост
цепичаще
всего происходит при взаимодействии
ониевого катиона с очередной молекулой
мономера:

Взаимодействие идет по схеме бимолекулярного нуклеофильного замещения (SN2), в котором роль нуклеофильного реагента выполняет молекула мономера, а субстрата – ониевый катион (напомним: оксониевый фрагмент – «хорошая» уходящая группа).
 Обрыв
цепи может
происходить при взаимодействии ониевого
макрокатиона с противоионом:
Обрыв
цепи может
происходить при взаимодействии ониевого
макрокатиона с противоионом:
Реакции катионной полимеризации циклических мономеров, помимо обычных реакций передачи цепи, могут сопровождаться весьма своеобразным вариантом передачи цепи на «мертвый» полимер – передачей цепи с разрывом (используется сокращение ПЦР, которое не следует путать с тем же обозначением для полимеразной цепной реакции синтеза ДНК). Эту передачу можно представить следующей схемой:
(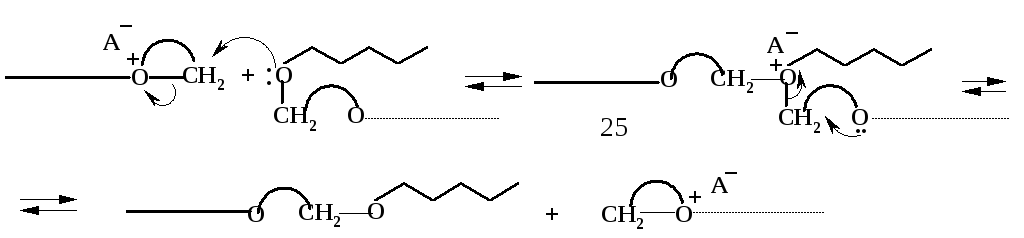 прямая
линия символизирует полимерную «живую»
цепь, ломаная и пунктирная – полимерные
фрагменты «мертвой» цепи).
прямая
линия символизирует полимерную «живую»
цепь, ломаная и пунктирная – полимерные
фрагменты «мертвой» цепи).
При взаимодействии «живой» и «мертвой» цепей образуется оксониевая структура (25), содержащая все три полимерных фрагмента; она может распадаться как по реакции, обратной ее получению, так и по двум другим реакциям, одна из которых представлена на схеме; в результате происходит своеобразный обмен полимерными фрагментами.
Влияние различных факторов на ход и результаты катионной полимеризации.
Влияние концентрации мономера и катализатора. Влияние этих факторов легко определяется при рассмотрении элементарной кинетики катионной полимеризации (т.е. без учета реакций передачи цепи). При этом скорости стадий полимеризации равны:
![]() Инициирование:
Инициирование:
где [Cat] – концентрация катализатора; [M] – концентрация мономера
(Здесь, в отличие от радикальной полимеризации, концентрация мономера входит в уравнение скорости инициирования, т.к. взаимодействие каталитического комплекса с мономером происходит на скоростьопределяющей стадии).
![]() Рост
цепи:
Рост
цепи:
Где [K+] – концентрация катионов (совершенно аналогично радикальной полимеризации)
![]() Обрыв
цепи
Обрыв
цепи
(концентрация катионов – в первой степени, т.к. в обрыве участвует одна «живая» цепь).
![]() Если
выполняется условие квазистационарности,
т.е. [K+]
= const,
то vи
=vo:
Если
выполняется условие квазистационарности,
т.е. [K+]
= const,
то vи
=vo:
Тогда скорость полимеризация, равная скорости роста цепи, выражается как:
![]() Следовательно,
скорость
катионной полимеризации пропорциональна
концентрации катализатора и квадрату
концентрации мономера.
Следовательно,
скорость
катионной полимеризации пропорциональна
концентрации катализатора и квадрату
концентрации мономера.
Средняя степень полимеризации (молекулярная масса полимера) выражается как:
Т![]() .е.молекулярная
масса полимера пропорциональна
концентрации мономера и не зависит от
концентрации катализатора.
.е.молекулярная
масса полимера пропорциональна
концентрации мономера и не зависит от
концентрации катализатора.
Если сравнивать кинетические характеристики радикальной и катионной полимеризации, то можно отметить, что сами по себе константы скоростей роста цепи при катионной полимеризации ниже, чем при радикальной, однако соотношение kp/ko при катионной полимеризации заметно выше (вплоть до нескольких порядков), чем при радикальной. Затрудненность обрыва цепей при катионной полимеризации позволяет получать полимеры с большой молекулярной массой при большей концентрации активных центров, чем при радикальных процессах.
Несмотря на значительную зависимость молекулярной массы и особенно скорости катионной полимеризации от концентрации мономера, скорости процессов здесь высоки и при относительно небольших концентрациях мономера; обычно полимеризацию проводят в растворах.
Влияние температуры. Обычно катионную полимеризацию проводят при низких температурах, в ряде случаев – отрицательных. Скорости процессов при этом сохраняется достаточно высокой; молекулярная масса при повышении температуры во многих случаях снижается, т.к. в этих случаях Еакт. обрыва цепи выше Еакт. роста цепи (в противоположность радикальной полимеризации).
В некоторых случаях понижение температуры до значений, находящихся вблизи температуры кристаллизации полимера, приводит к увеличению скорости полимеризации. Вероятно, это связано с упорядочением молекул мономера вблизи температуры кристаллизации; такая ориентация увеличивает долю эффективных столкновений в ходе роста цепи.
Влияние растворителя. Как известно, растворители оказывают весьма сильное влияние на протеканиеионных процессов; катионная полимеризация – не исключение. В частности, при изменении полярности растворителя, меняется характер активного центра: в малополярных растворителях возникаюттесные (контактные) ионные пары [~CH2–CH(X)]+Aˉ; при увеличении полярности растворителя ионные пары становятсярыхлыми (сольватно разделенными) [~CH2–CH(X)]+║Aˉ, в которых ионы более активны: наконец, при дальнейшем увеличении полярности ионные пары могут частично распадаться с образованием еще более активныхсвободных ионов. Поэтому с ростом полярности растворителя растет скорость роста цепи, что приводит к увеличению как скорости процесса, так и молекулярной массы. Например, при полимеризации стирола под действием ТiCl4–HClпри переходе от бензола (ε=2,3) к нитробензолу (ε=36) скорость полимеризации увеличивается на 2 порядка, а средняя степень полимеризации – в 5 раз. Еще сильнее выражен эффект полярности растворителя при полимеризации того же стирола под действием НС1О4: при замене СС14 (ε=2) на дихлорэтан (ε=9,7)kрувеличивается на 5 порядков.
Процессы с катион-радикальным инициированием. В ранее рассмотренных процессах катионные активные центры возникали при двухэлектронном переносе – например, перемещении двух электронов π-связи мономера к каталитическому комплексу. Однако, возможен другой вариант – одноэлектронный перенос – передача одного электрона от мономера к катализатору; при этом молекула мономера превращается в катион-радикал. В качестве катализаторов таких процессов используются одноэлектронные акцепторы; простой пример – инициирование в присутствии солей Fe3+:
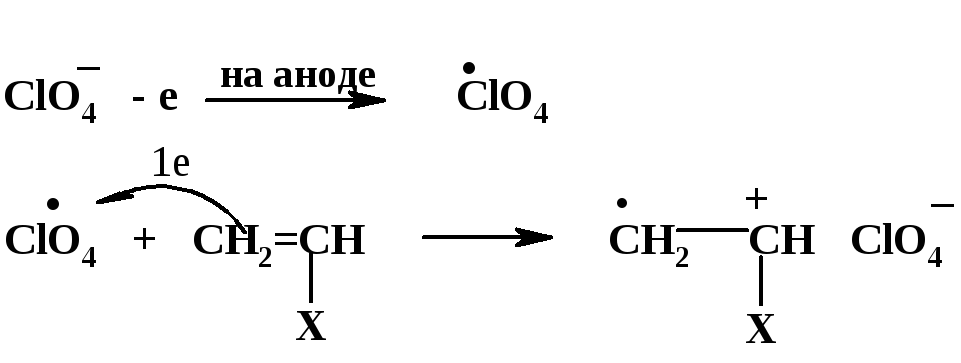
 Возможно
и электрохимическое ион-радикальное
инициирование: при электролизе перхлоратов
или борфторидов в присутствии мономера
происходят следующие реакции:
Возможно
и электрохимическое ион-радикальное
инициирование: при электролизе перхлоратов
или борфторидов в присутствии мономера
происходят следующие реакции:
В качестве одноэлектронного акцептора здесь выступает перхлорат-радикал, возникающий при одноэлектронном анодном окислении перхлорат-аниона; отбирая один электрон от мономера, этот радикал превращается в более устойчивый перхлорат-анион.
Если винильный мономер содержит донорный заместитель Х, то в образовавшемся из него катион-радикале (26) катионный центр, естественно, находится при более замещенном атоме углерода, рядом со стабилизирующей группой Х.
Рост цепи, следующий за инициированием, в принципе может идти и по катионному и по радикальному типу. При низких температурах (при которых обычно и ведут полимеризацию) доминирует рост по катионному типу:
В начале
два катион-радикала рекомбинируют с
образованием дикатиона (27) а затем
происходит рост цепи по катионному типус двух сторон
этого
димерного дикатиона.
начале
два катион-радикала рекомбинируют с
образованием дикатиона (27) а затем
происходит рост цепи по катионному типус двух сторон
этого
димерного дикатиона.
Катион-радикальное инициирование используется мало; более характерно анион-радикальное инициирование, которое будет рассмотрено ниже.
