
- •Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Ульяновский государственный технический университет
- •Введение
- •Лабораторная работа № 1. Термическое окисление кремния
- •Лабораторная работа № 2. Диффузия
- •Лабораторная работа №3 ионная имплантация
- •Лабораторная работа №4. Катодное распыление
- •Приложение Основные параметры химических элементов
Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Ульяновский государственный технический университет
ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ТЕХНОЛОГИИ
ЭЛЕКТРОННЫХ СРЕДСТВ
Сборник лабораторных работ по дисциплине
«Физико-химические основы технологии электронных средств»
Составитель В. И. Смирнов
Ульяновск 2006
УДК 621.38(076)
Физико-химические основы технологии электронных средств … /. Сост. В. И. Смирнов. – Ульяновск: УлГТУ, 2006. – 22 с.
Сборник лабораторных работ выполнен в соответствии с учебными программами дисциплины «Физико-химические основы технологии электронных средств».
В сборнике представлены лабораторные работы, цель которых – изучение основных физико-химических процессов при формировании структур полупроводниковых интегральных микросхем, а именно, диффузии, ионной имплантации, термического окисления, катодного распыления. Работы имеют расчетный характер, в каждой из них даны список литературы и контрольные вопросы для самопроверки.
Ил. 7. Табл. 2. Библиогр.: 7 назв.
Рецензент профессор кафедры АиАиРЭО
Ульяновского высшего авиационного
училища гражданской авиации, к.т.н. А. В. Ефимов
Одобрен секцией методических пособий научно-методического совета университета
© УлГТУ, 2006
СОДЕРЖАНИЕ
Введение …………………………………………………………………….…….. 4
Лабораторная работа №1. Термическое окисление кремния ………….………. 5
Лабораторная работа №2. Диффузия ……………………………………….…… 9
Лабораторная работа №3. Ионная имплантация ………………………………. 13
Лабораторная работа №4. Катодное распыление ……………………………… 18
Приложение ………………………………………………………………………. 22
Введение
Сборник лабораторных работ по дисциплине «Физико-химические основы технологии электронных средств» для студентов, обучающихся по направлению 21020165, включает в себя описания четырех работ, цель которых – изучение физико-химических процессов при формировании структур полупроводниковых интегральных микросхем. Все работы носят расчетный характер и предполагают наличие у студентов навыков работы с компьютером, в частности, с программным пакетом MathCad.
Перед выполнением работы студент обязан сдать допуск по работе и получить у преподавателя исходные данные для расчета. Отчет по работе, кроме названия, цели работы и основных расчетных соотношений, включает в себя также результаты расчета, оформленные в виде таблиц и графиков, и выводов по работе. Каждая из работ имеет список литературы и контрольные вопросы для самопроверки.
Лабораторная работа № 1. Термическое окисление кремния
Цель работы
1. Изучение механизма окисления кремния.
2. Изучение модели Дила-Гроува.
3. Изучение влияния технологических факторов на скорость окисления.
4. Расчет скорости окисления кремния при различных температурах процесса.
Введение
Оксидные пленки на поверхности кремния предназначены в основном для пассивации поверхности полупроводниковых пластин, формирования маскирующих покрытий при фотолитографии и формирования подзатворного слоя диэлектрика в МДП-структурах. Одним из основных способов получения пленок SiO2 является термическое окисление в сухом кислороде или смеси кислорода и паров воды. Соответствующие химические реакции для сухого и влажного окисления имеют вид:
![]()
![]()
Реакция окисления происходит на границе раздела Si SiO2, то есть атомы и молекулы окислителя диффундируют через растущий слой оксида кповерхности кремния, где и происходит реакция. Температура процесса находится в диапазоне 8001300С. Чем выше температура, тем выше скорость роста пленки SiO2. Однако проводить процесс окисления пластин Si при высоких температурах, когда в них уже сформированы элементы микросхемы, нежелательно, поскольку дополнительный нагрев приводит кпроцессу диффузии примесей, уже внедренных в пластину.
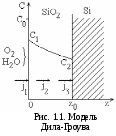 Кинетика
процесса описывается моделью Дила-Гроува.
Согласно этой модели, механизм окисления
можно представить в виде нескольких
стадий: адсорбции и растворения молекул
окислителя в приповерхностном слое
кремниевой пластины, диффузии их через
растущий оксидный слой к границе раздела
Кинетика
процесса описывается моделью Дила-Гроува.
Согласно этой модели, механизм окисления
можно представить в виде нескольких
стадий: адсорбции и растворения молекул
окислителя в приповерхностном слое
кремниевой пластины, диффузии их через
растущий оксидный слой к границе раздела![]() ,
химической реакции молекул окислителя
с атомами кремния. Каждой из этих стадий
можно поставить в соответствие плотность
потока (рис. 1.1), которая по определению
равна количеству молекул окислителя,
пересекающих единицу поверхности за
единицу времени. Плотность токаj1
определяется разностью концентраций
молекул окислителя в газовой фазе C0
и приповерхностном слое пластины C1:
,
химической реакции молекул окислителя
с атомами кремния. Каждой из этих стадий
можно поставить в соответствие плотность
потока (рис. 1.1), которая по определению
равна количеству молекул окислителя,
пересекающих единицу поверхности за
единицу времени. Плотность токаj1
определяется разностью концентраций
молекул окислителя в газовой фазе C0
и приповерхностном слое пластины C1:
![]() ,
,
где h – коэффициент пропорциональности, называемый константой скорости растворения молекул окислителя в слое SiO2.
Плотность потока молекул окислителя через растущий слой оксида кремния j2 определяется законом Фика:
![]() ,
,
где D – коэффициент диффузии молекул окислителя в SiO2; z0 – толщина слоя SiO; С2 – концентрация молекул на границе раздела SiO2 – Si.
Плотность
потока j3,
описывающая скорость химической реакции,
пропорциональна концентрации молекул
окислителя C2
у границы раздела
![]() :
:
![]() ,
,
где k – константа скорости химической реакции.
В установившемся режиме все эти плотности потока равны:
![]() .
.
Исключив из этих равенств С1, получим:
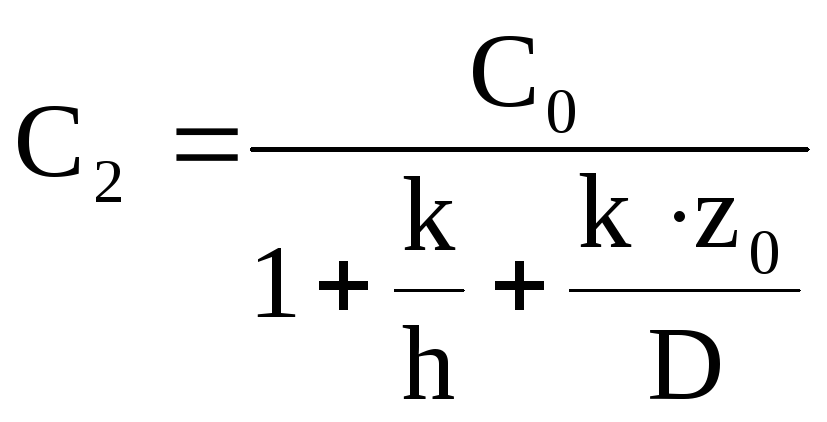 .
.
Для
того, чтобы за время dt
окислить объем
![]() ,
требуется
,
требуется![]() молекул. С другой стороны, это число
равно
молекул. С другой стороны, это число
равно![]() молекул, гдеNi
– концентрация атомов кремния в слое
SiO2
(равная
молекул, гдеNi
– концентрация атомов кремния в слое
SiO2
(равная
![]() ).
Отсюда:
).
Отсюда:
![]()
или
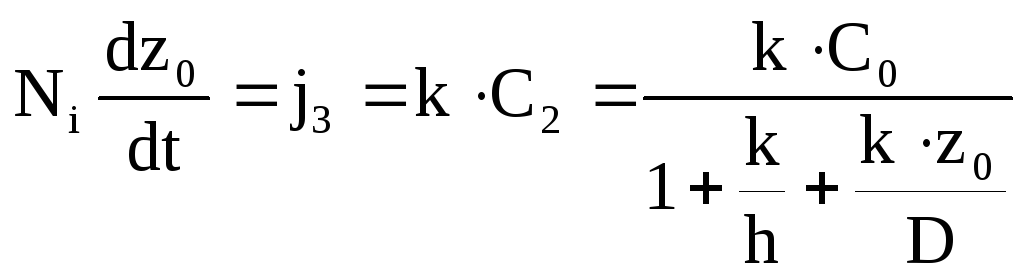 .
.
Следует
учесть, что при влажном окислении в
соответствии с химической реакцией на
образование одного моля SiO2
требуется два моля H2O,
поэтому величину Ni
необходимо взять равной
![]() .
.
Разделяя
переменные и интегрируя с учетом того,
что в момент
![]() на поверхности кремния уже существовал
самородный слой оксида толщинойzi,
получим:
на поверхности кремния уже существовал
самородный слой оксида толщинойzi,
получим:
![]() .
.
Упростим полученное выражение, введя новые обозначения:
![]()
![]()
![]()
С учетом этого получим:
![]() .
.
Решая это квадратное уравнение, найдем зависимость толщины растущего слоя SiO2 от времени:
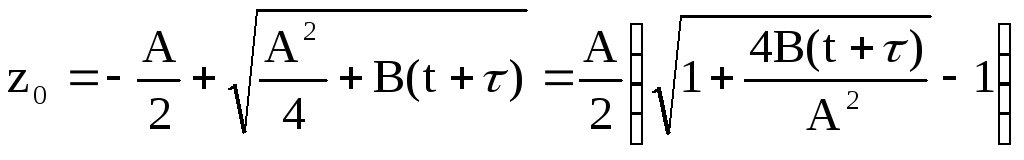 .
.
При
малых временах окисления, когда
выполняется условие
![]() ,
получим:
,
получим:
![]() .
.
При
большом времени окисления, когда
выполняется условие
![]() :
:
![]() .
.
Таким образом, на начальном этапе роста оксидной пленки ее толщина увеличивается со временем линейно, при большом времени окисления – зависимость корневая. Это качественно верно описывает кинетику роста оксидной пленки.
Теоретически было доказано, что параметры A и B экспоненциально зависят от температуры:
![]()
![]() ,
,
где С1, С2, E1, E2 – эмпирические коэффициенты, равные для сухого окисления:
![]()
![]()
![]() ;
;![]() ;
;
для влажного окисления:
![]()
![]()
![]() ;
;![]() .
.
Толщину
самородного слоя zi
при сухом окислении в расчетах можно
принять равной нулю, при влажном окислении
![]() .
.
Кроме температуры и окислительной среды на скорость роста слоя SiO2 влияет давление газа-окислителя. Повышение давления увеличивает концентрацию молекул окислителя, растворенных в приповерхностном слое, тем самым увеличивается градиент концентрации молекул в слое SiO2, а значит, и скорость диффузии. Окисление при повышенном давлении водяного пара (ускоренное гидротермальное окисление) позволяет получать оксидные пленки толщиной 23мкм. Недостатком метода является необходимость использования герметичных и высокопрочных реакторов вместо технологичных проточных систем.
Наиболее часто используется толщина оксидной пленки, составляющая десятые доли микрометра, а верхний практический предел по толщине для обычного термического окисления составляет 1-2 мкм. Значительное положительное влияние оказывает добавление в окислительную среду хлорсодержащих компонентов. Это привело к улучшению стабильности порогового напряжения МДП-транзисторов, увеличению напряжения пробоя и повышению скорости окисления. Главная роль хлора в пленках SiO2 (обычно с концентрацией хлора 1016 – 1020 см-3) заключается в превращении проникших в оксид примесных ионов, таких как Na и K, в электрически неактивные. Кроме того, внедрение хлора может создавать механические напряжения в решетке SiO2, вследствие чего облегчается диффузия молекул окислителя через оксидную пленку.
На скорость роста слоя SiO2 оказывает влияние кристаллографическая ориентация кремниевой пластины. Окисление на пластине с ориентацией (111) происходит быстрее, чем с ориентацией (100). Влияние ориентации особенно заметно при относительно низких температурах. Так, например, при Т = 700С отличие в скорости окисления составляет 40%, а при Т = 1200С всего 2%. Зависимость скорости окисления от кристаллографической ориентации объясняется тем, что различным кристаллографическим направлениям пластины соответствует разное количество связей Si – Si.
Большое влияние на скорость роста слоя SiO2 оказывает концентрация легирующей примеси в исходной пластине кремния. Это влияние обусловлено явлением сегрегации примеси на границе раздела SiO2 – Si. Для одних примесных атомов растворимость в Si выше, чем в SiO2, поэтому притермическом окислении растущий оксид оттесняет примесные атомы вглубь пластины кремния. В результате оксидный слой обедняется данными примесными атомами. Так, в частности, ведут себя атомы фосфора, мышьяка, сурьмы. А такие атомы, как бор, напротив, лучше растворяются в SiO2, чем в Si, поэтому при окислении слой SiO2 получается обогащенным атомами бора. Наличие примесных атомов в слое SiO2 создает в нем механические напряжения и как бы «разрыхляет» его, что способствует увеличению скорости диффузии молекул окислителя через растущий слой оксида. Атомы фосфора, мышьяка и сурьмы оказывают влияние только на скорость химической реакции. Поэтому их влияние существенно только на ранней стадии процесса, когда толщина слоя невелика и общая скорость окисления определяется скоростью химической реакции. Атомы бора, напротив, оказывают влияние и при относительно толстых слоях SiO2.
Задание
1. Получить у преподавателя исходные данные для расчета: окислительная среда, температуры процесса.
2. Рассчитать и построить графики зависимостей толщины оксидной пленки от времени окисления при различных температурах.
Контрольные вопросы
1. Механизм термического окисления (модель Дила-Гроува).
2. Влияние на скорость роста SiO2 температуры и давления газа-окислителя.
3. Влияние на скорость роста и качество пленок хлоросодержащих компонентов.
4. Влияние на скорость роста SiO2 концентрации примеси в кремнии и кристаллографической ориентации подложки.
Литература
1. Курносов А. И., Юдин В. В. Технология производства полупроводниковых приборов и интегральных микросхем. – М.: Высш. шк., 1986. – С. 112-120.
2. Пичугин И. Г., Таиров Ю. М. Технология полупроводниковых приборов. – М.: Высш. шк., 1984. – С. 236-269.
3. Броудай И., Мерей Дж. Физические основы микротехнологии. – М.: Мир, 1985. – С. 358-365.
4. Смирнов В. И. Физико-химические основы технологии электронных средств. Учебное пособие. – Ульяновск: УлГТУ, 2005. – С. 24- 29
