- •Физика атома, атомного ядра и элементарных частиц
- •Водородоподобный атом
- •Теория Бора
- •Второе соотношение, связывающее радиус орбиты электрона и его скорость дает правило квантова-
- •Водородоподобный атом
- •Таким образом, для водородоподобных ато- мов теория, основанная на постулатах Бо- ра, дает
- •Теория Бора - это приближенная полуклас- сическая теория, промежуточный этап в истории создания
- •Схематическое изо- бражение уровней энергии и переходов между ними в атоме водорода
- •Интернет-экзамен
- •Интернет-экзамен
- •Интернет-экзамен

Физика атома, атомного ядра и элементарных частиц
3. (0). Модель водородоподобного атома по теории Бора.

Водородоподобный атом
 Водородоподобным называется атом,
Водородоподобным называется атом,  имеющий один электрон в электронной оболочке. Это атом обычного (легкого) водорода, атом тяжелого водорода (дейтерия), сверхтяжелого водорода
имеющий один электрон в электронной оболочке. Это атом обычного (легкого) водорода, атом тяжелого водорода (дейтерия), сверхтяжелого водорода  (трития), однократно ионизированный
(трития), однократно ионизированный  атом гелия, двухкратно ионизированный атом лития и т.д.
атом гелия, двухкратно ионизированный атом лития и т.д. 

Теория Бора
Рассмотрим водородоподобный атом, т.е. систему из ядра с зарядом +Ze и одного электрона. При Z=1 это водород, при Z=2 – однократно ионизи- рованный атом гелия, при Z=3 – двукратно иони- зированный атом лития и т.д.).
Предположим, что электрон движется вокруг ядра по круговой орбите радиуса r со скоростью v. Приравнивая кулоновскую силу и центробежную  силу, находим:
силу, находим:
m v2 |
Ze2 |
|
e |
4 0r2 |
(3.1) |
r |

Второе соотношение, связывающее радиус орбиты электрона и его скорость дает правило квантова-
ния: |
mevr nh |
|
|
(3.2) |
Решая совместно уравнения (3.1) и (3.2), находим
радиус орбиты электрона: |
|
||
r |
n2 |
4 0h2 |
(3.3) |
n |
|
m Ze2 |
|
|
|
e |
|
Суммируя кинетическую и потенциальную энергию электрона, находим его полную энергию:
E = T +U = |
m v2 |
- |
Ze2 |
= - |
1 |
Z 2m e4 |
||
e |
|
|
|
|
e |
|||
n |
2 |
|
4 0r |
|
n |
2 |
2 |
2 |
|
|
|
|
8hε |
0 |
|||

Водородоподобный атом
Итак, радиус n-ой стационарной орбиты и энергия электро- на на этой орбите в водородоподобном атоме равны:
rn n |
2 4 0h2 |
En = - |
1 Z 2m e4 |
|||||
meZe |
2 |
n |
2 |
8hε |
e |
|||
|
|
|||||||
|
|
0 |
||||||
|
|
|
|
2 |
2 |
|||
Например, для водорода r1 = 0.53 Å, E1 = - 13.6 эВ.
Постоянная Ридберга |
|
m e4 |
|
109740 |
1 |
|
|
R =см e |
|
|
|||
|
|
3 |
2 |
|
|
|
|
|
8chε |
0 |
|
|
R |
С учетом конечной массы ядра M |
|
R |
|
|||
|
|
|
|
1 m / M |
||
|
|
|
|
|
|
e |
постоянная Ридберга точно совпадает с эксперименталь- ным значением 109677,6 см-1 

Таким образом, для водородоподобных ато- мов теория, основанная на постулатах Бо- ра, дает результаты, с высокой точностью совпадающие с экспериментом. Более то- го, эта теория объясняет даже такой тонкий эффект, как изотопический сдвиг спект- ральных линий в спектре водородоподоб- ных атомов.
Однако попытки объяснить строение и свой-  ства более сложных атомов (например, атома гелия с двумя электронами) приво- дят к неудаче.
ства более сложных атомов (например, атома гелия с двумя электронами) приво- дят к неудаче. 

Теория Бора - это приближенная полуклас- сическая теория, промежуточный этап в истории создания квантовой физики.
Однако благодаря своей простоте эта тео- рия до сих пор используется в тех случа- ях, когда надо наглядно объяснить какое- либо явление или эффект и получить  оценку характерных параметров задачи по порядку величины.
оценку характерных параметров задачи по порядку величины. 
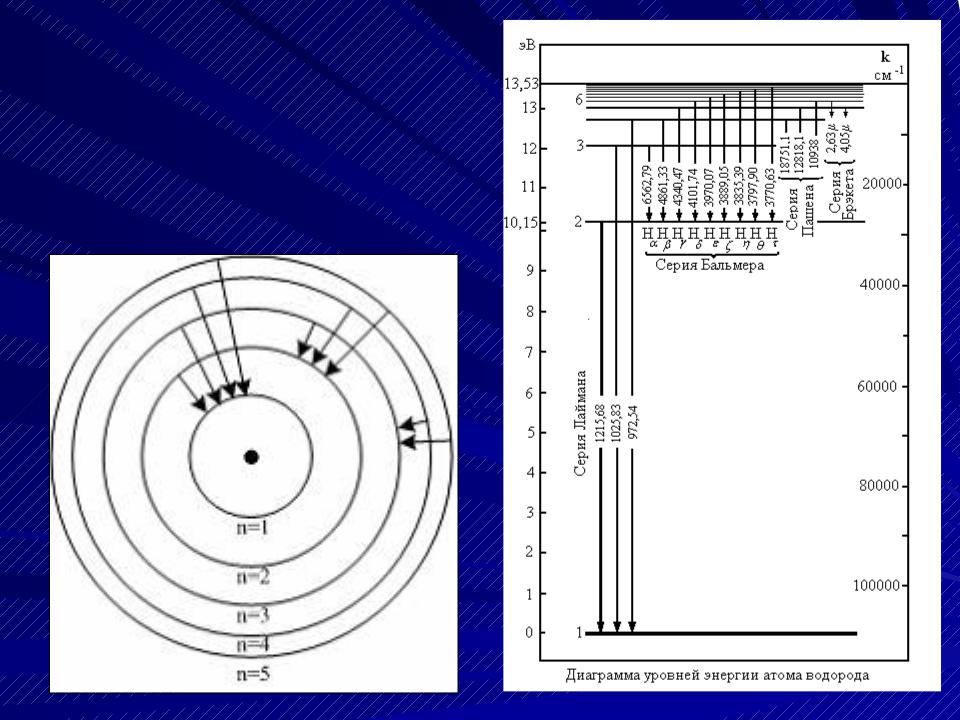
Схематическое изо- бражение уровней энергии и переходов между ними в атоме водорода

Интернет-экзамен
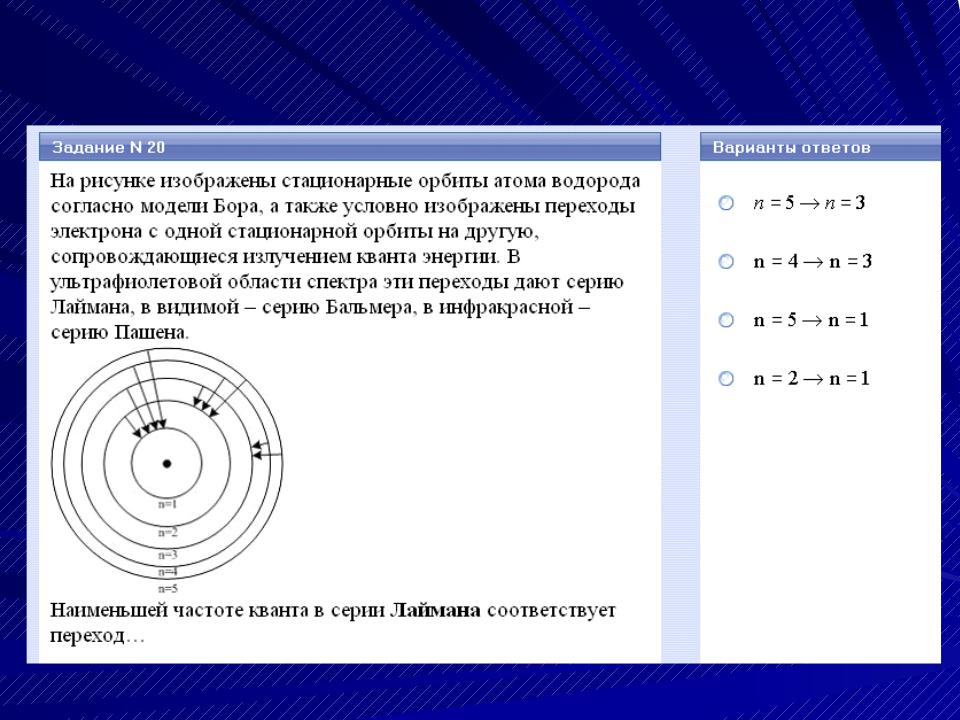
На рисунке изображены стационарные орбиты атома водорода согласно мо- дели Бора, а также условно изображе- ны переходы электрона с одной стаци- онарной орбиты на другую, сопровож- дающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана (Ly- man T.), в видимой – серию Бальмера Balmer J.), в инфракрасной – серию Па-
шена (Paschen F.). Наибольшей частоте кванта в серии Лаймана соответству-
ет переход… |
|
ВАРИАНТЫ ОТВЕТОВ: 1) n=2 n=1 |
2) n=5 n=3 |
3) n=3 n=2 |
4) n=5 n=1 |
 РЕШЕНИЕ: Серия Лаймана: переход на уровень n=1. чем больше изменение энергии, тем больше частота
РЕШЕНИЕ: Серия Лаймана: переход на уровень n=1. чем больше изменение энергии, тем больше частота  излученного кванта. ОТВЕТ: 4.
излученного кванта. ОТВЕТ: 4.