
- •Физика атома, атомного ядра и элементарных частиц
- •Рассмотрим более сложные примеры.
- •Итак, двум p-электронам отвечает де- сять возможных состояний атома. Од- нако все они
- •Действительно, при данных L и S воз- можные значения магнитных кван- товых чисел
- •Составим таблицу возможных значений ML для двух эквивалентных p-электронов
- •Оставшиеся значения ML можно разбить на две группы:
- •Аналогичные рассуждения можно про- вести для любого количества электро- нов, причем векторная модель
- •Правило Хунда
- •Правило Хунда является следствием взаимного отталкивания электронов. Действительно, энер- гия атома (с учетом
- •В качестве примера рассмотрим атом, который имеет два валентных p – электрона. Это

Физика атома, атомного ядра и элементарных частиц
ядра и элементарных частиц
19 (2). Квантовые состояния многоэлектронных атомов.
Правило Хунда.

Рассмотрим более сложные примеры.
Пусть один из электронов перешел в сос- тояние l1 = 1, а второй может оказаться в состояниях l2 = 0, 1, 2. Запишем воз- можные значения L в виде таблицы:

Рассмотрим случай l2 = 1 (оба электрона в состоянии p). Тогда L=0, 1, 2.
Если S = 0, то J = L, и возможны состояния:
при |
L 0 |
1S0 |
, |
при |
L 1 |
1P |
, |
|
|
1 |
|
при |
L 2 |
1D . |
|
|
|
2 |
|

Если S = 1, то количество термов будет больше, т.к. тогда J = L+1, L, L-1.
Если L=0, то |
J 1 |
3S . |
|
|
Если L = 1, то возможно |
1 |
|
||
|
|
|||
J 0,1, 2 |
|
3 P , |
3 P , |
3 P |
|
|
0 |
1 |
2 |
Если L = 2, то возможно |
|
|
||
J 1, 2, 3 |
|
3 D , |
3 D , |
3 D |
|
|
1 |
2 |
3 |

 Итак, двум p-электронам отвечает де- сять возможных состояний атома. Од- нако все они могут осуществиться толь- ко в том случае, если не нарушен прин-
Итак, двум p-электронам отвечает де- сять возможных состояний атома. Од- нако все они могут осуществиться толь- ко в том случае, если не нарушен прин-
цип Паули. Если n1 и n2 (главные кван- товые числа) различны, то могут осу- ществиться все десять возможных сос-
тояний. Если же n1 = n2, то некоторые из найденных термов оказываются за-
найденных термов оказываются за-  прещенными принципом Паули.
прещенными принципом Паули.

Действительно, при данных L и S воз- можные значения магнитных кван- товых чисел ML и MS определяются условиями:
M L L, L 1, L 2, ... , L
MS S, S 1, S 2, ... , S
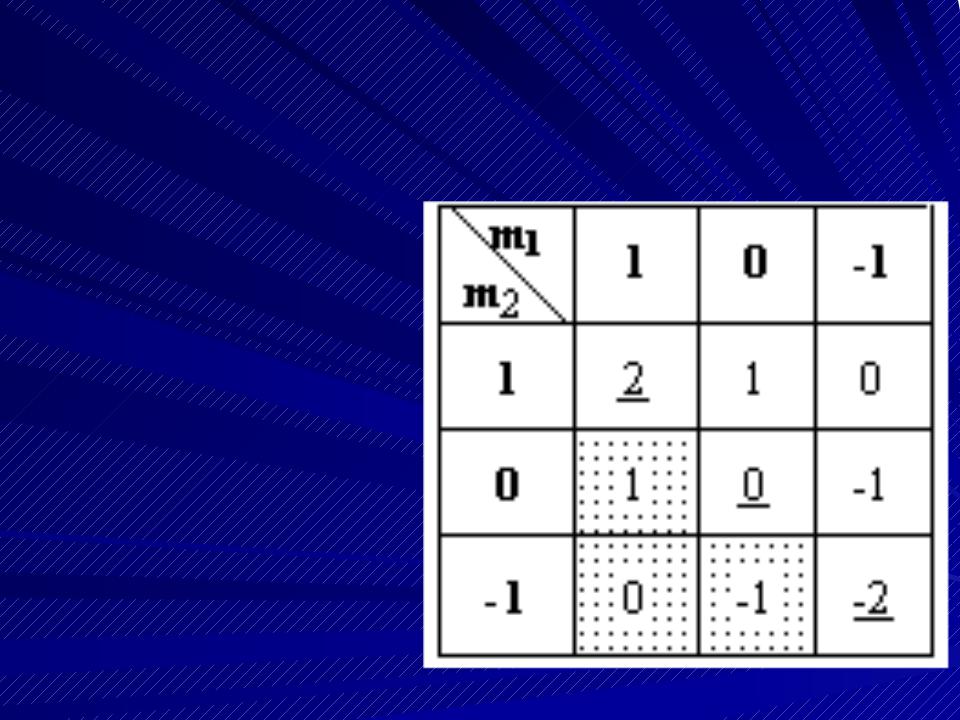
Составим таблицу возможных значений ML для двух эквивалентных p-электронов
(n1 = n2).
Т.к. электроны экви- валентны, то заштри- хованные клетки не дают ничего нового,
и их следует исклю- чить из рассмотре- ния (неважно, m1=1,
m2=0 или m1=0, m2=1, если электроны не- различимы).

Оставшиеся значения ML можно разбить на две группы:
M L 2, 1, 0, 1, 2 L 2
M L 0 L 0
Эти значения осуществляются, если m1=m2, это возможно, если ms1 ≠ ms2, т.е. если  S=0. Поэтому в системе синглетных сос-
S=0. Поэтому в системе синглетных сос-  тояний (S = 0, = 1) остаются состояния
тояний (S = 0, = 1) остаются состояния
1S0 и 1D2 (исключено состояние 1P1).

Если ms1 = ms2, т.е. если S=1, то невозможны состояния с m1=m2, поэтому значения ML на главной диагонали (под- черкнуты) следует отбросить. Тогда остается только один ряд значений ML:
M L 1, 0, 1 L 1
Поэтому в системе триплетных состояний оста- |
||
ются состояния 3 P0 , |
3 P1 , |
3 P2. |
Итак, в случае двух эквивалентных p-электронов возможно существование только пяти состоя-
ний (вместо десяти для электронов с n1 n2).

Аналогичные рассуждения можно про- вести для любого количества электро- нов, причем векторная модель очень точно предсказывает особенности спектров сложных атомов.
После того, как найдены возможные тер- мы атомов, возникает вопрос, какой из этих термов основной. На этот вопрос  дает ответ правило, эмпирически уста- новленное в 1926г Фридрихом Хундом (Hund F.)
дает ответ правило, эмпирически уста- новленное в 1926г Фридрихом Хундом (Hund F.) 
