
- •Тема 1. Второй закон термодинамики.
- •94. Определите изменение энтропии для реакции
- •Решение.
- •Решение.
- •121. Рассчитайте давления, при которых графит и алмаз находятся в равновесии для интервала температур 298—4000 к. При расчете используйте следующие данные для равновесия с (графит) с (алмаз):
- •Решение.
- •Решение.
- •Многовариантные задачи
- •Решение.
- •Тема 2. Характеристические функции
- •Решение:
- •Решение.
- •Решение.
- •Решение.
Многовариантные задачи
1-30. Определить изменение энтропии при протекании реакции при давлении 1,013∙105 н/м2 и 25°С, а также теплоту реакции обратимого процесса и сделать вывод о возможности протекания самопроизвольного процесса.
|
Но мер задачи |
Реакции |
|
кдж/ моль |
|
|
|
1 |
РЬ (т) + 2AgCl (т) =PbCI2 aq +2Ag(т) |
0,490 |
-105,5 |
||
|
2 |
Hg2Cl2 + 2КВг = Hg2Br2 + 2KCl |
0,128 |
-29,54 |
||
|
3 |
Pb + Hg2CI2 (т) =РЬСl + 2Hg |
0,394 |
-128,98 |
||
|
4 |
Cd+2AgCl (т) = CdCl + 2Ag |
0,625 |
-136,4 |
||
|
5 |
TI (т) + AgCl (т) = ТlСl (т) + Ag |
0,558 |
-78,17 |
||
|
6 |
2Ag+Hg2Cl2(т)=2AgCl+2Hg
|
0,046 |
+ 11,25 |
||
|
7 |
Hg2CI2(t) + 2KOH aq =Hg20 (т) +2KC1 (т) + H20 |
0,1542 |
+ 13,73 |
||
|
8 |
CuAc2 aq + Pb = PbAc2 aq + Cu
|
0,4764 |
+69,09 |
||
|
9 |
Zn + CuS04 aq = Cu + ZnS04 aq |
1,100 |
-207,1 |
||
|
10 |
Ag
(т) + |
0,688 |
-64,2 |
||
|
11 |
Ag+
|
0,994 |
-99,16 |
||
|
12 |
2Hg + Вг2 (ж) = Hg2Br2 |
0,925 |
-206,77 |
||
|
13 |
2Hg + Сl2 (г) = Hg2Cl2 |
1,092 |
-264,85 |
||
|
14 |
Pb
(т)
+
|
0,662 |
-175,1 |
||
|
15 |
PbO2(t) + Pb (t) + 2H2S04 aq = 2PbS04 (t) + 2H20 |
1,581 |
-608,68 |
||
|
16 |
Cd (t) + CI2 (r) = CdCl2 (т) |
1,763 |
-389,0 |
||
|
17 |
Cd (т) + Вг2 (ж) = CdBr2 (t) |
1,468 |
-314,5 |
||
|
18 |
Cu (t) + Cl2 (r) =CuCl (т) |
1,023 |
-205,9 |
||
|
19 |
Cu
(t)
+
|
0,025 |
-695,3 |
||
|
20 |
Cu (t) +1/2 Br2 (ж) = CuBr (т) |
0,544 |
-105,1 |
||
|
21 |
Cu(t) +1/2 Cl2 (r) =CuCI(t)
|
0,839 |
-134,7 |
||
|
22 |
Mg (т) + Cl2 (r) = MgCI2 (т)
|
3,723 |
-134,7 |
||
|
23 |
Ni (t) + Cl2 (r) =NiCl2 (t) |
1,610 |
—315,9 |
||
|
24 |
Zn (т) + Сl2 (г) =ZnCl2(т) |
2,123 |
—415,9 |
||
|
25 |
Fe (т) + С12 (г)=FeCl2(т) |
1,800 |
—342,7 |
|
|
|
26 |
Ва(т) +С12 (г)=BaCl2 (т) |
4,259 |
—859,8 |
||
|
27 |
Са(т) +Сl2(г)=CaCl2(т) |
4,226 |
—785,8 |
||
|
28 |
Со (т) + Сl2 (г)=CoCl2(т) |
1,637 |
-325,4 |
||
|
29 |
Аl (т) + 3/2 Сl2(г)=AlCl3(т) |
3,022 |
-697,4 |
||
|
30 |
Sn (т) + Сl2 (г) =SnCl2(т) |
1,496 |
-349,6 |
||

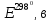
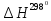
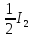 (т) =Agl
(т)
(т) =Agl
(т) (ж)=AgBr
(ж)=AgBr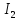 (т)
= Pbl2
(t)
(т)
= Pbl2
(t) (т)
=Cul (т)
(т)
=Cul (т)