
- •Лабораторная работа №1
- •1. Окси-, оксокислоты
- •1.1.Гидроксикарбоновые кислоты Опыт1. Свойства молочной кислоты
- •Опыт 2. Свойства винной кислоты.
- •Опыт 3. Получение цитрата кальция
- •2.1. Кетокислоты. Ацетоуксусный эфир Опыт 4. Получение пировиноградной кислоты окислением молочной кислоты
- •Опыт 5. Свойства ацетоуксусного эфира
- •1.3. Ароматические оксикислоты Опыт 6. Взаимодействие бензойной, коричной и салициловой кислот с бромной водой
- •Опыт 7. Отношение бензойной и коричной кислот к перманганату калия
- •Опыт 8. Реакции бензойной и салициловой кислот с хлоридом железа (III)
- •Опыт 9. Взаимодействие эфиров салициловой кислоты с хлоридом железа (III)
- •Опыт 10. Образование фталевого ангидрида
- •2.2. Аминокислоты Опыт 12. Свойства аминокислот
- •2.3. Мочевина Опыт 13. Свойства мочевины
- •Ароматические амины Опыт14. Растворимость анилина и его солей в воде. Основные свойства анилина
- •Опыт 15. Взаимодействие анилина с бромной водой
- •Опыт 16. Ацилирование анилина
- •Опыт 17. Окисление анилина
- •2.5. Диазо- и азосоединения Опыт 18. Реакция диазотирования анилина (получение соли диазония)
- •Опыт 19. Разложение соли диазония (реакция с выделением азота)
- •Опыт 20. Реакции солей диазония без выделения азота (реакции азосочетания)
- •Опыт 21. Крашение шерсти и шелка кислотными азокрасителями
- •Опыт 22. Крашение хлопчатобумажной ткани (ледяное крашение)
- •Лабораторная работа №3
- •3. Углеводы
- •3.1. Моносахариды Опыт 23. Качественная реакция на углеводы с α -нафтолом (реакция Молиша)
- •Опыт 24. Реакции моносахаридов по карбонильной группе
- •Опыт 25. Реакции на гидроксильные группы в моносахаридах
- •Опыт 26. Цветные реакции на моносахариды
- •3.2. Дисахариды Опыт 27. Реакции на гидроксильные группы дисахаридов
- •Опыт 28. Реакции дисахаридов по карбонильной группе. Сравнение свойств восстанавливающих и невосстанавливающих дисахаридов
- •Опыт 29. Гидролиз (инверсия) сахарозы
- •Опыт 30. Реакция сахарозы с сульфатами кобальта и никеля
- •3.3. Высшие полисахариды Опыт 31. Отношение полисахаридов к реактиву Фелинга
- •Опыт 32. Взаимодействие крахмала и гликогена с иодом
- •Опыт 33. Гидролиз крахмала
- •Опыт 34. Кислотный гидролиз клетчатки
- •Лабораторная работа №4
- •Гетероциклические соединения Опыт 35. Получение фурфурола и его свойства
- •Опыт 36. Получение «белого» индиго и кубовое крашение
- •Опыт 37. Пиридин и его свойства
- •Опыт 38. Мочевая кислота
Опыт 21. Крашение шерсти и шелка кислотными азокрасителями
Реактивы и оборудование:метиловый оранжевый, 2М раствор серной кислоты; химические стаканы на 100 мл, кусочки белой шерстяной или шелковой ткани.
В состав кислотных азокрасителей входят кислые солеобразующие группы (—СООН; —ОSO3H; — ОН). Шерсть и шелк — природные белковые полимеры, имеющие в своем составе амидные (основные) группы, которые могут связываться с кислотными группировками молекул красителя. Обычно красители получают в виде натриевых солей, поэтому для высвобождения кислотных групп и для более эффективного крашения добавляют кислоту (Н2SО4,).
Растворяют 0,1 г метилового оранжевого в 50 мл воды.
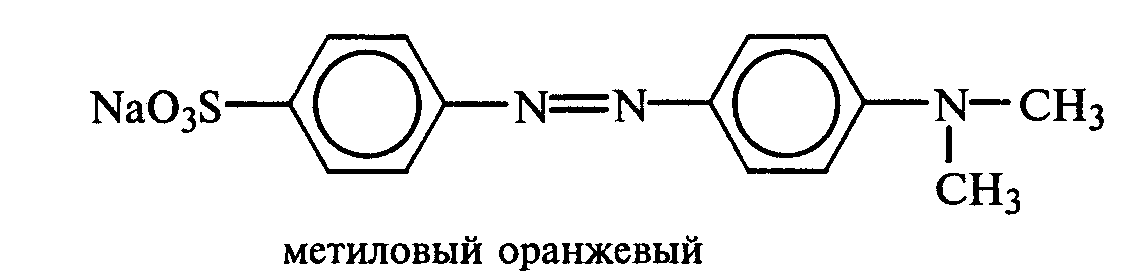
Раствор разливают в два стакана. В один из них добавляют 5 мл 2М раствора серной кислоты. В оба стакана опускают по кусочку белой шерстяной или шелковой ткани. Растворы кипятят 5мин. Затем ткани вынимают, промывают водой и высушивают на воздухе. Окраска ткани, полученная в присутствии серной кислоты, значительно интенсивнее, чем та, что образовалась без добавления кислоты.
Опыт 22. Крашение хлопчатобумажной ткани (ледяное крашение)
Реактивы и оборудование:β-нафтол, 1М раствор гидроксида натрия, 2М раствор ацетата натрия, раствор n-нитрофенилдиазонийхлорида; кусочки белой хлопчатобумажной ткани, химические стаканы на 50 мл.
В отличие от шерсти и шелка, хлопчатобумажная ткань, состоящая из целлюлозы, не содержит групп, обладающих сродством к кислотным и основным красителям. Взаимодействие красителя и ткани происходит за счет сорбции, поэтому ледяное крашение применяют в тех случаях, когда краситель нерастворим или плохо растворим в воде.
Полоску белой хлопчатобумажной ткани пропитывают 2%-ным раствором β -нафтола в 1М растворе гидроксида натрия. Ткань отжимают и сушат над плиткой или газовой горелкой. Высушенную ткань помещают в стаканчики приливают к ней раствор n-нитрофенилдиазонийхлорида и добавляют 2М раствор ацетата натрия. Ткань окрашивается в красный цвет:

Азосочетание с фенолами (нафтолами) проводят в слабощелочной среде, так как нафтолятанион является более сильной электронодонорной группой по сравнению с гидроксильной. За счет этого в щелочной среде в α -положении у нафтолята натрия образуется избыточная электронная плотность, которая является объектом атаки для электрофильной частицы.
Лабораторная работа №3
3. Углеводы
Углеводы —важнейшие природные органические соединения, в состав которых входят карбонильная и не менее двух гидроксильных групп. По составу и строению углеводы делят на несколько групп. Простые углеводы, или моносахариды, — это вещества, не способные гидролизоваться (например, глюкоза, фруктоза и т.д.). Углеводы, состоящие из двух и более остатков моносахаридов, называются олигосахаридами. В эту группу углеводов входят дисахариды (сахароза, лактоза и др.). Полисахариды, или полиозы, состоят из большого числа остатков моносахаридов, определенным образом связанных между собой (крахмал, клетчатка, гликоген и др.).
