
- •Лабораторная работа №1
- •1. Окси-, оксокислоты
- •1.1.Гидроксикарбоновые кислоты Опыт1. Свойства молочной кислоты
- •Опыт 2. Свойства винной кислоты.
- •Опыт 3. Получение цитрата кальция
- •2.1. Кетокислоты. Ацетоуксусный эфир Опыт 4. Получение пировиноградной кислоты окислением молочной кислоты
- •Опыт 5. Свойства ацетоуксусного эфира
- •1.3. Ароматические оксикислоты Опыт 6. Взаимодействие бензойной, коричной и салициловой кислот с бромной водой
- •Опыт 7. Отношение бензойной и коричной кислот к перманганату калия
- •Опыт 8. Реакции бензойной и салициловой кислот с хлоридом железа (III)
- •Опыт 9. Взаимодействие эфиров салициловой кислоты с хлоридом железа (III)
- •Опыт 10. Образование фталевого ангидрида
- •2.2. Аминокислоты Опыт 12. Свойства аминокислот
- •2.3. Мочевина Опыт 13. Свойства мочевины
- •Ароматические амины Опыт14. Растворимость анилина и его солей в воде. Основные свойства анилина
- •Опыт 15. Взаимодействие анилина с бромной водой
- •Опыт 16. Ацилирование анилина
- •Опыт 17. Окисление анилина
- •2.5. Диазо- и азосоединения Опыт 18. Реакция диазотирования анилина (получение соли диазония)
- •Опыт 19. Разложение соли диазония (реакция с выделением азота)
- •Опыт 20. Реакции солей диазония без выделения азота (реакции азосочетания)
- •Опыт 21. Крашение шерсти и шелка кислотными азокрасителями
- •Опыт 22. Крашение хлопчатобумажной ткани (ледяное крашение)
- •Лабораторная работа №3
- •3. Углеводы
- •3.1. Моносахариды Опыт 23. Качественная реакция на углеводы с α -нафтолом (реакция Молиша)
- •Опыт 24. Реакции моносахаридов по карбонильной группе
- •Опыт 25. Реакции на гидроксильные группы в моносахаридах
- •Опыт 26. Цветные реакции на моносахариды
- •3.2. Дисахариды Опыт 27. Реакции на гидроксильные группы дисахаридов
- •Опыт 28. Реакции дисахаридов по карбонильной группе. Сравнение свойств восстанавливающих и невосстанавливающих дисахаридов
- •Опыт 29. Гидролиз (инверсия) сахарозы
- •Опыт 30. Реакция сахарозы с сульфатами кобальта и никеля
- •3.3. Высшие полисахариды Опыт 31. Отношение полисахаридов к реактиву Фелинга
- •Опыт 32. Взаимодействие крахмала и гликогена с иодом
- •Опыт 33. Гидролиз крахмала
- •Опыт 34. Кислотный гидролиз клетчатки
- •Лабораторная работа №4
- •Гетероциклические соединения Опыт 35. Получение фурфурола и его свойства
- •Опыт 36. Получение «белого» индиго и кубовое крашение
- •Опыт 37. Пиридин и его свойства
- •Опыт 38. Мочевая кислота
2.3. Мочевина Опыт 13. Свойства мочевины
Реактивы и оборудование:мочевина кристаллическая, 20%-ный раствор мочевины, концентрированная азотная кислота, ледяная уксусная кислота, концентрированный раствор гидроксида натрия, насыщенный раствор щавелевой кислоты, насыщенный раствор гидроксида бария, 20%-ный раствор нитрита натрия, 10%-ный раствор гидроксида натрия, 1%-ный раствор сульфата меди, бром, лакмусовая бумага (синяя и красная); лед, пипетки, изогнутые газоотводные трубки, химические стаканы на 100 мл, пробирки.
13.1. Растворимость мочевины в воде и образование ее солей. В пробирку вносят 0,2—0,5 г мочевины и добавляют несколько капель воды до полного ее растворения. По капле раствора наносят на синюю и красную лакмусовую бумагу. Раствор мочевины нейтрален на лакмус. Тем не менее основные свойства мочевины можно обнаружить при взаимодействии ее с кислотами. Полученный концентрированный раствор мочевины делят на две части. К первой части добавляют 2—3 капли концентрированной азотной кислоты, а ко второй — 2—3 капли насыщенного раствора щавелевой кислоты. Через несколько секунд наблюдают выпадение кристаллов солей мочевины:
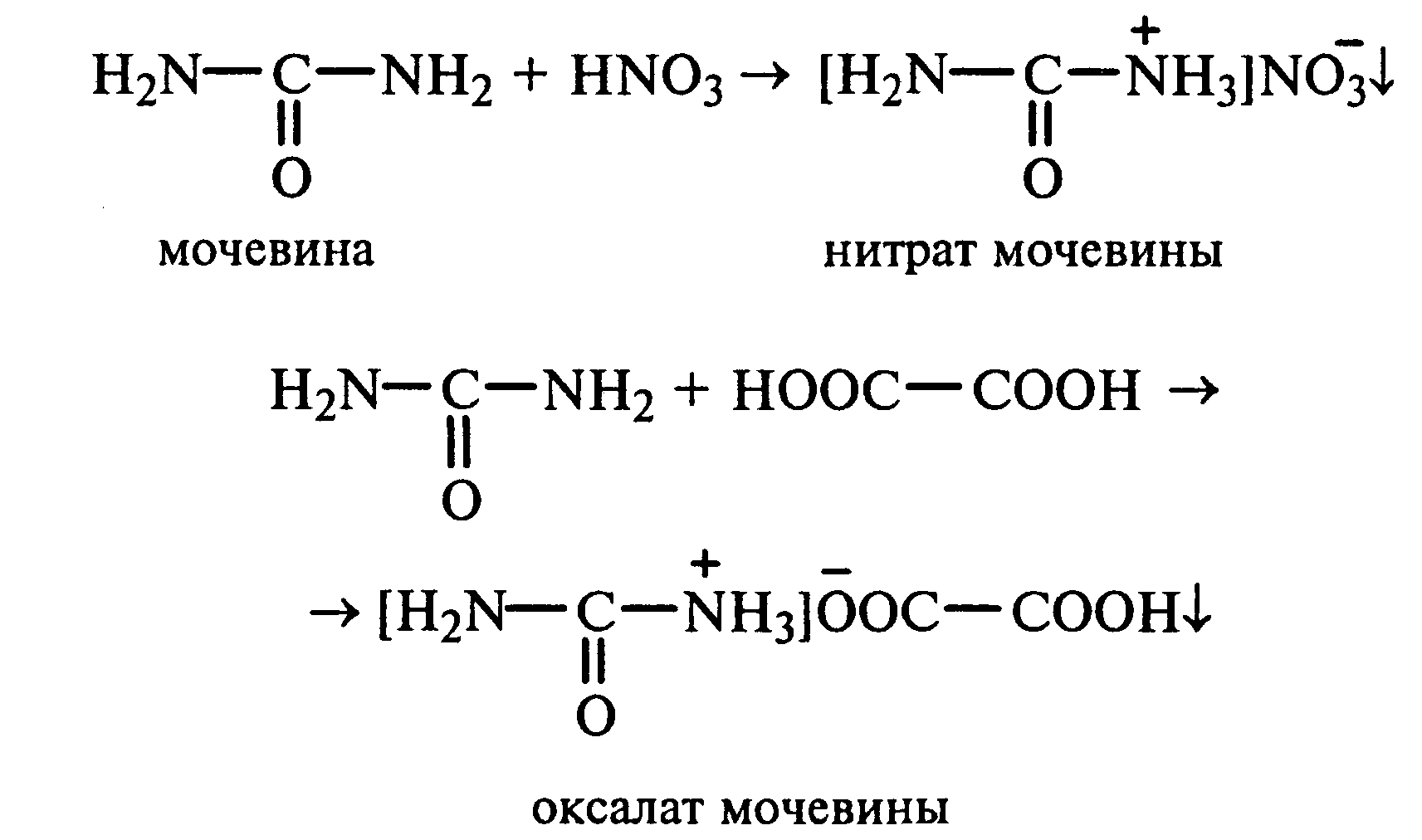
Почему мочевина дает соль только по одной аминогруппе? Способность мочевины образовывать труднорастворимую соль с азотной кислотой используют для обнаружения мочевины в моче. В сутки с мочой из организма человека выделяется около 30 г мочевины.
13.2 Гидролиз мочевины.В пробирку вносят 0,1—0,2 г мочевины и добавляют 1—2 мл баритовой воды (насыщенный раствор гидроксида бария). Раствор кипятят до выпадения в осадок карбоната бария. Влажная красная лакмусовая бумажка, поднесенная к отверстию пробирки во время кипячения раствора, синеет в связи с выделением аммиака:

В живых организмах гидролиз мочевины происходит под действием фермента уреазы (urea — лат.мочевина).
13.3. Реакция мочевины с азотистой кислотой.В пробирку наливают 1 мл 20%-ного раствора мочевины, 1,5 мл 20%-ного раствора нитрита натрия и 2—3 капли ледяной уксусной кислоты. Пробирку закрывают пробкой с изогнутой газоотводной трубкой, конец которой опускают в пробирку с баритовой водой. Пробирку с реакционной смесью встряхивают и наблюдают интенсивное выделение пузырьков газов — азота и оксида углерода (IV). Последний обнаруживают по помутнению баритовой воды.
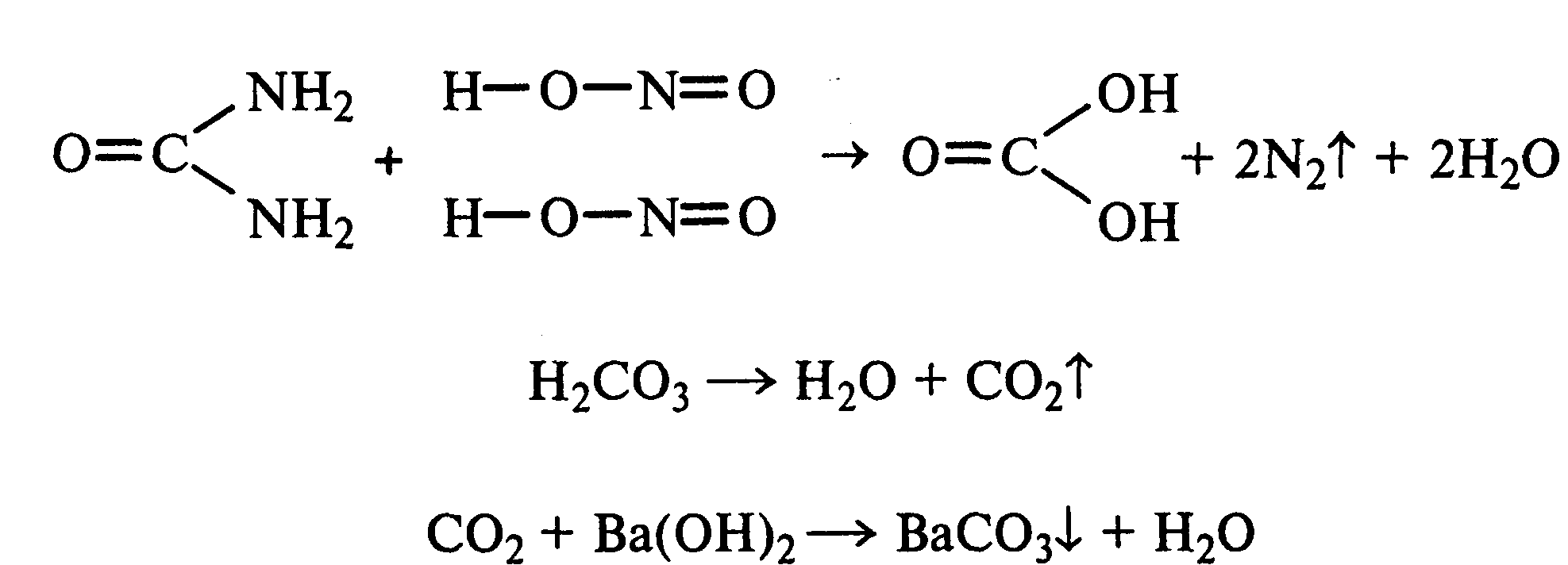
Эта реакция подобна реакции с азотистой кислотой первичных аминов алифатического ряда и аминокислот. Ее также используют для количественного определения мочевины по методу Ван-Сляйка (масса мочевины рассчитывается по объему выделившегося азота).
13.4. Разложение мочевины гипобромитом натрия (тяга).Для приготовления раствора гипобромита натрия в пробирку наливают 1—2 мл концентрированного раствора гидроксида натрия и при охлаждении добавляют 3—4 капли брома. Смесь встряхивают до растворения брома и исчезновения его окраски.
![]()
К 1 мл 20%-ного раствора мочевины добавляют по каплям раствор гипобромита натрия. В пробирке наблюдают бурное выделение азота и оксида углерода (IV):

Эта реакция лежит в основе количественного определения мочевины по методу Бородина (массу мочевины рассчитывают по объему выделившегося азота).
13.5. Образование биурета.В сухую пробирку насыпают 0,2 г мочевины и нагревают ее в пламени горелки. Мочевина сначала плавится, а потом при дальнейшем нагревании разлагается с выделением аммиака, который обнаруживают по посинению влажной красной лакмусовой бумажки, поднесенной к отверстию пробирки, и по запаху. Через некоторое время плав в пробирке затвердевает, несмотря на продолжающееся нагревание:

Пробирку охлаждают, добавляют в нее 2 мл воды и при слабом нагревании растворяют полученный биурет. Когда осадок отстоится, сливают с него раствор биурета и добавляют несколько капель 10%-ного раствора гидроксида натрия и 1—2 капли 1%-ного раствора сульфата меди. Раствор окрашивается в розово-фиолетовый цвет вследствие образования комплексной медной соли биурета.
Схема таутомерных превращений биурета:

Уравнение реакции биурета с гидроксидом меди (II):

комплексная медная соль биурета.
Эта реакция называется биуретовой. Она также является цветной реакцией на пептиды и белки.
