
- •Лабораторная работа №1
- •1. Окси-, оксокислоты
- •1.1.Гидроксикарбоновые кислоты Опыт1. Свойства молочной кислоты
- •Опыт 2. Свойства винной кислоты.
- •Опыт 3. Получение цитрата кальция
- •2.1. Кетокислоты. Ацетоуксусный эфир Опыт 4. Получение пировиноградной кислоты окислением молочной кислоты
- •Опыт 5. Свойства ацетоуксусного эфира
- •1.3. Ароматические оксикислоты Опыт 6. Взаимодействие бензойной, коричной и салициловой кислот с бромной водой
- •Опыт 7. Отношение бензойной и коричной кислот к перманганату калия
- •Опыт 8. Реакции бензойной и салициловой кислот с хлоридом железа (III)
- •Опыт 9. Взаимодействие эфиров салициловой кислоты с хлоридом железа (III)
- •Опыт 10. Образование фталевого ангидрида
- •2.2. Аминокислоты Опыт 12. Свойства аминокислот
- •2.3. Мочевина Опыт 13. Свойства мочевины
- •Ароматические амины Опыт14. Растворимость анилина и его солей в воде. Основные свойства анилина
- •Опыт 15. Взаимодействие анилина с бромной водой
- •Опыт 16. Ацилирование анилина
- •Опыт 17. Окисление анилина
- •2.5. Диазо- и азосоединения Опыт 18. Реакция диазотирования анилина (получение соли диазония)
- •Опыт 19. Разложение соли диазония (реакция с выделением азота)
- •Опыт 20. Реакции солей диазония без выделения азота (реакции азосочетания)
- •Опыт 21. Крашение шерсти и шелка кислотными азокрасителями
- •Опыт 22. Крашение хлопчатобумажной ткани (ледяное крашение)
- •Лабораторная работа №3
- •3. Углеводы
- •3.1. Моносахариды Опыт 23. Качественная реакция на углеводы с α -нафтолом (реакция Молиша)
- •Опыт 24. Реакции моносахаридов по карбонильной группе
- •Опыт 25. Реакции на гидроксильные группы в моносахаридах
- •Опыт 26. Цветные реакции на моносахариды
- •3.2. Дисахариды Опыт 27. Реакции на гидроксильные группы дисахаридов
- •Опыт 28. Реакции дисахаридов по карбонильной группе. Сравнение свойств восстанавливающих и невосстанавливающих дисахаридов
- •Опыт 29. Гидролиз (инверсия) сахарозы
- •Опыт 30. Реакция сахарозы с сульфатами кобальта и никеля
- •3.3. Высшие полисахариды Опыт 31. Отношение полисахаридов к реактиву Фелинга
- •Опыт 32. Взаимодействие крахмала и гликогена с иодом
- •Опыт 33. Гидролиз крахмала
- •Опыт 34. Кислотный гидролиз клетчатки
- •Лабораторная работа №4
- •Гетероциклические соединения Опыт 35. Получение фурфурола и его свойства
- •Опыт 36. Получение «белого» индиго и кубовое крашение
- •Опыт 37. Пиридин и его свойства
- •Опыт 38. Мочевая кислота
1.3. Ароматические оксикислоты Опыт 6. Взаимодействие бензойной, коричной и салициловой кислот с бромной водой
Реактивы и оборудование:насыщенные растворы бензойной, коричной и салициловой кислот, бромная вода (насыщенная); пипетки, пробирки.
В три пробирки наливают по 1—2 мл насыщенных растворов бензойной, коричной и салициловой кислот. В каждую пробирку добавляют по несколько капель насыщенной бромной воды. В пробирке с бензойной кислотой бромная вода не обесцвечивается, так как бензойная кислота бромируется только в присутствии катализатора. Коричная и салициловая кислоты обесцвечивают бромную воду:
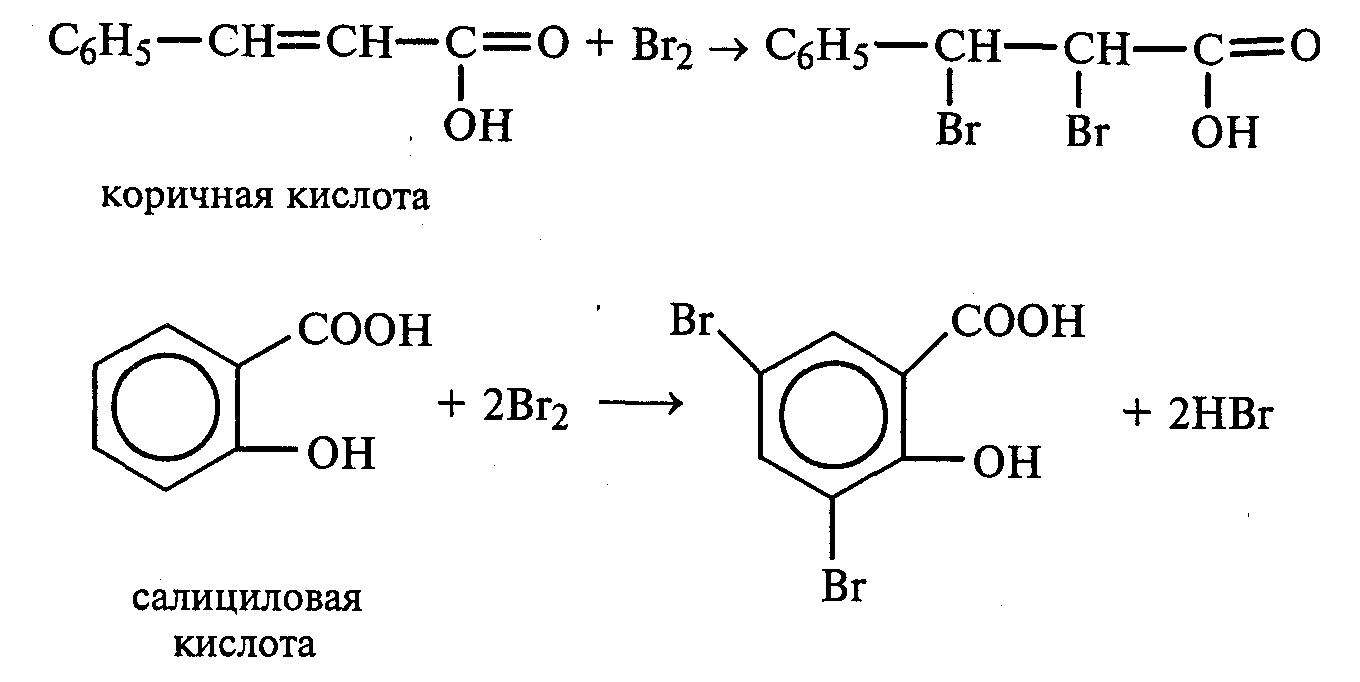
Напишите механизмы данных реакций. Объясните, почему бензойная кислота не взаимодействует с бромом при данных условиях.
Опыт 7. Отношение бензойной и коричной кислот к перманганату калия
Реактивы и оборудование:бензойная кислота, коричная кислота, 10%-ный раствор карбоната натрия, 5%-ный раствор перманганата калия, пробирки.
Небольшие количества (по 0,1 г) бензойной и коричной кислот растворяют в минимальном объеме 10%-ного раствора карбоната натрия. В оба раствора при перемешивании добавляют раствор перманганата калия. Лишь в пробирке с коричной кислотой окраска перманганата калия исчезает, и появляются бурые хлопья оксида марганца (IV). Бензойная кислота устойчива к действию окислителей:

В приведенном уравнении реакции определите степени окисления атомов и расставьте коэффициенты.
Опыт 8. Реакции бензойной и салициловой кислот с хлоридом железа (III)
Реактивы и оборудование:насыщенные растворы бензойной и салициловой кислот, 1%-ный раствор хлорида железа (III); пипетки, пробирки.
В две пробирки наливают по 1 мл насыщенных растворов бензойной и салициловой кислот, добавляют по 1 мл воды, а затем по 1—2 капли 1%-ного раствора хлорида железа (III). Бензойная кислота не взаимодействует с хлоридом железа (III), а в пробирке с салициловой кислотой в результате образования комплексного соединения появляется фиолетовая окраска.
Опыт 9. Взаимодействие эфиров салициловой кислоты с хлоридом железа (III)
Реактивы и оборудование:ацетилсалициловая кислота, фенилсалицилат (салол), этиловый спирт, 1%-ный раствор хлорида железа (III); пробирки.
В одной пробирке растворяют 0,1 г ацетилсалициловой кислоты (аспирина) в 3—4 мл воды. Полученный раствор делят на две части. В другой пробирке к 1,5—2 мл этанола прибавляют несколько кристаллов фенилсалицилата (салола).
В одну из пробирок с раствором ацетилсалициловой кислоты и в пробирку с фенилсалицилатом приливают по 1—2 капли 1%-ного раствора хлорида железа (III). Раствор фенилсалицилата окрашивается в ярко-фиолетовый цвет, а в пробирке с аспирином окраска отсутствует. Однако следует помнить, что при длительном хранении аспирин может гидролизоваться, и в этом случае будет появляться фиолетовая окраска. Реакция с хлоридом железа (III) служит для определения чистоты аспирина.
Вторую пробирку с раствором ацетилсалициловой кислоты кипятят несколько минут на газовой горелке, а затем добавляют 1—2 капли раствора хлорида железа (III). Появляется фиолетовая окраска, которая свидетельствует о том, что при нагревании происходит высвобождение фенольного гидроксила в результате гидролиза:

