
- •Лабораторная работа №1
- •1. Окси-, оксокислоты
- •1.1.Гидроксикарбоновые кислоты Опыт1. Свойства молочной кислоты
- •Опыт 2. Свойства винной кислоты.
- •Опыт 3. Получение цитрата кальция
- •2.1. Кетокислоты. Ацетоуксусный эфир Опыт 4. Получение пировиноградной кислоты окислением молочной кислоты
- •Опыт 5. Свойства ацетоуксусного эфира
- •1.3. Ароматические оксикислоты Опыт 6. Взаимодействие бензойной, коричной и салициловой кислот с бромной водой
- •Опыт 7. Отношение бензойной и коричной кислот к перманганату калия
- •Опыт 8. Реакции бензойной и салициловой кислот с хлоридом железа (III)
- •Опыт 9. Взаимодействие эфиров салициловой кислоты с хлоридом железа (III)
- •Опыт 10. Образование фталевого ангидрида
- •2.2. Аминокислоты Опыт 12. Свойства аминокислот
- •2.3. Мочевина Опыт 13. Свойства мочевины
- •Ароматические амины Опыт14. Растворимость анилина и его солей в воде. Основные свойства анилина
- •Опыт 15. Взаимодействие анилина с бромной водой
- •Опыт 16. Ацилирование анилина
- •Опыт 17. Окисление анилина
- •2.5. Диазо- и азосоединения Опыт 18. Реакция диазотирования анилина (получение соли диазония)
- •Опыт 19. Разложение соли диазония (реакция с выделением азота)
- •Опыт 20. Реакции солей диазония без выделения азота (реакции азосочетания)
- •Опыт 21. Крашение шерсти и шелка кислотными азокрасителями
- •Опыт 22. Крашение хлопчатобумажной ткани (ледяное крашение)
- •Лабораторная работа №3
- •3. Углеводы
- •3.1. Моносахариды Опыт 23. Качественная реакция на углеводы с α -нафтолом (реакция Молиша)
- •Опыт 24. Реакции моносахаридов по карбонильной группе
- •Опыт 25. Реакции на гидроксильные группы в моносахаридах
- •Опыт 26. Цветные реакции на моносахариды
- •3.2. Дисахариды Опыт 27. Реакции на гидроксильные группы дисахаридов
- •Опыт 28. Реакции дисахаридов по карбонильной группе. Сравнение свойств восстанавливающих и невосстанавливающих дисахаридов
- •Опыт 29. Гидролиз (инверсия) сахарозы
- •Опыт 30. Реакция сахарозы с сульфатами кобальта и никеля
- •3.3. Высшие полисахариды Опыт 31. Отношение полисахаридов к реактиву Фелинга
- •Опыт 32. Взаимодействие крахмала и гликогена с иодом
- •Опыт 33. Гидролиз крахмала
- •Опыт 34. Кислотный гидролиз клетчатки
- •Лабораторная работа №4
- •Гетероциклические соединения Опыт 35. Получение фурфурола и его свойства
- •Опыт 36. Получение «белого» индиго и кубовое крашение
- •Опыт 37. Пиридин и его свойства
- •Опыт 38. Мочевая кислота
Опыт 3. Получение цитрата кальция
Реактивы и оборудование:5%-ный раствор лимонной кислоты, 5%-ный раствор хлорида кальция, 10%-ный раствор аммиака, лакмусовая бумага; пробирки.
В пробирку вносят 1 мл раствора лимонной кислоты, который затем нейтрализуют 10%-ным раствором аммиака, приливая его по каплям при перемешивании до нейтральной реакции среды (лакмус). К полученному раствору цитрата аммония добавляют 1 мл 5%-ного раствора хлорида кальция. Раствор осторожно нагревают в пламени горелки до кипения. Выпадает осадок цитрата кальция. При охлаждении раствора осадок растворяется, так как эта соль в горячей воде растворяется хуже, чем в холодной.
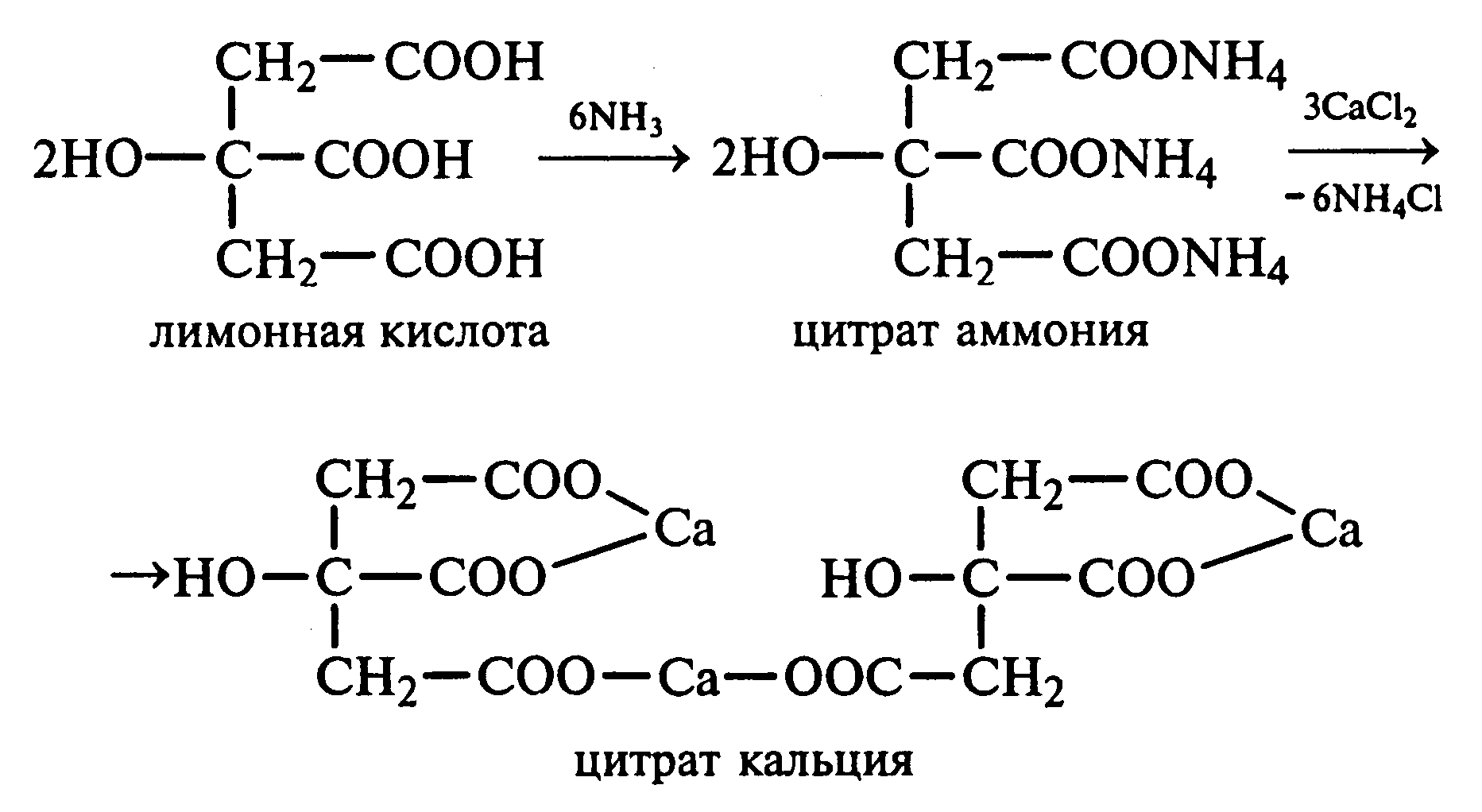
2.1. Кетокислоты. Ацетоуксусный эфир Опыт 4. Получение пировиноградной кислоты окислением молочной кислоты
Реактивы и оборудование:5%-ный раствор молочной кислоты, 1%-ный раствор перманганата калия, 10%-ный раствор карбоната натрия, 2%-ный раствор нитропруссида натрия, 10%-ный раствор гидроксида натрия, универсальная индикаторная бумага; фильтровальная бумага, химические воронки, пробирки.
В пробирку наливают 0,5 мл молочной кислоты, которую нейтрализуют, прибавляя по каплям 10%-ный раствор карбоната натрия (контроль рН среды осуществляют по универсальной индикаторной бумаге). Затем добавляют 2—3 мл 5%-ного раствора перманганата калия. Содержимое пробирки тщательно перемешивают и доводят до кипения на газовой горелке. Фиолетово-розовая окраска перманганата калия исчезает, и выпадает бурый осадок оксида марганца (IV).
![]()

Полученный раствор фильтруют. Для обнаружения пировиноградной кислоты проводят качественную реакцию на кетогруппу. Для этого к фильтрату приливают 1 мл 2%-ного раствора нитропруссида натрия и 1 мл 10%-ного раствора гидроксида натрия. Раствор окрашивается в оранжево-красный цвет. При добавлении нескольких капель концентрированной уксусной кислоты раствор становится вишнево-красным.
Опыт 5. Свойства ацетоуксусного эфира
Реактивы и оборудование:ацетоуксусный эфир, натрий металлический, бромная вода (насыщенная), 2%-ный раствор хлорида железа (III); лед, фильтровальная бумага, скальпели, пинцеты, химические стаканы на 100 мл, пробирки.
5.1. Кето-енольная таутомерия ацетоуксусного эфира.В пробирку вносят 1—2 капли ацетоуксусного эфира и приливают 2 мл дистиллированной воды. Смесь энергично перемешивают и добавляют 1 каплю 2%-ного раствора хлорида железа (III). Постепенно развивается фиолетовое окрашивание, которое свидетельствует о наличии енольной группы в растворе ацетоуксусного эфира. Хлорид железа (III) образует с енольной формой окрашенное комплексное соединение.
При добавлении нескольких капель бромной воды раствор обесцвечивается, так как бром присоединяется по двойной связи, и гидроксильная группа утрачивает енольный характер:
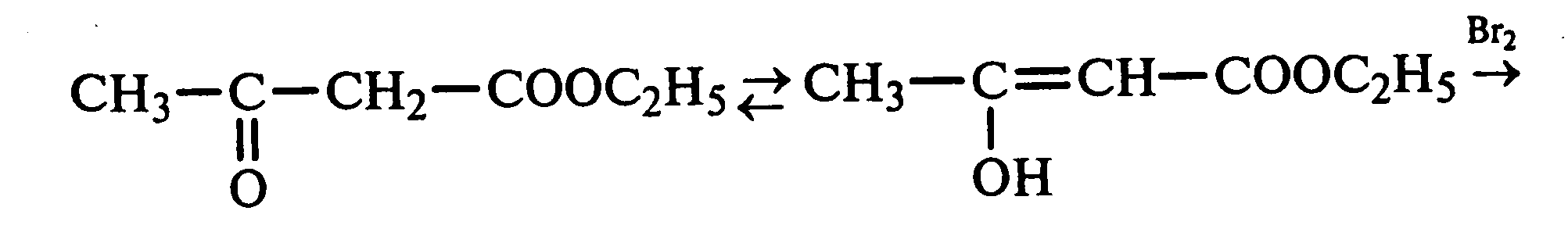

Через некоторое время раствор вновь окрашивается в фиолетовый цвет, так как связывание енольной формы нарушает динамическое равновесие, и часть оставшейся кетонной формы ацетоуксусного эфира переходит в енольную, образующую окрашенный комплекс с ионами Fe3+. В енольную форму может также переходить монобромацетоуксусный эфир. При повторном добавлении бромной воды снова наблюдают обесцвечивание раствора с последующим возобновлением фиолетовой окраски. Этот процесс может продолжаться до полного замещения подвижных атомов водорода на бром, т. е. до получения дибромацетоуксусного эфира, не способного к таутомерным превращениям.

5.2. Взаимодействие ацетоуксусного эфира с металлическим натрием.В пробирку наливают 2 мл свежеперегнанного ацетоуксусного эфира и бросают в него небольшой кусочек(1/4горошины) металлического натрия, очищенного от оксидной пленки и отжатого в фильтровальной бумаге. Идет довольно интенсивная реакция с выделением водорода. После ее окончания пробирку охлаждают в стакане со льдом. Натрийацетоуксусный эфир выпадает в осадок:

