
- •02080165 “Экология”, 11090165 “Водные биоресурсы и аквакультура”, 08040165 “Товароведение и экспертиза товаров”, колледж “Технолог”
- •Часть I
- •Содержание
- •Введение
- •Правила техники безопасности при работе в химической лаборатории
- •Правила техники безопасности при работе с кислотами и щелочами
- •Правила техники безопасности при работе с бромом
- •Правила техники безопасности при работе с металлическими натрием и калием
- •Техника безопасности при работе с легковоспламеняющимися жидкостями
- •Техника безопасности при работе под вакуумом
- •Меры безопасности при утечке газа и тушении локального пожара и горящей одежды
- •Оказание первой медицинской помощи при ожогах и отравлениях химическими веществами
- •1. Качественный элементный анализ органических соединений Лабораторная работа № 1
- •Опыт 1. Обнаружение углерода пробой на обугливание
- •Опыт 2. Обнаружение углерода и водорода окислением вещества оксидом меди (II)
- •Органическом веществе:
- •Опыт 5. Определение галогенов в органических веществах
- •2. Свойства углеводородов алифатического и ароматического ряда Лабораторная работа № 2 Опыт 6. Реакция углеводородов с бромом
- •Опыт 7. Отношение углеводородов к окислению( реакция Вагнера)
- •Опыт 8. Взаимодействие углеводородов с серной кислотой
- •Опыт 9. Получение ацетилена и исследование его свойств
- •3. Гидроксипроизводные углеводородов Лабораторная работа № 3
- •3.1. Алифатические спирты
- •Опыт 10. Образование и свойства этилата натрия
- •Опыт 11. Получение глицерата меди
- •Опыт 12. Реакции окисления этилового спирта
- •Опыт 13. Получение простого диэтилового эфира
- •3.2. Фенолы Осторожно! Фенолы вызывают ожоги кожи Опыт 14. Образование и разложение фенолятов
- •Опыт 15. Взаимодействие фенола с бромной водой
- •Опыт 16. Окисление фенола
- •Опыт 17. Взаимодействие фенолов с хлоридом железа (III)
- •4. Оксопроизводные углеводородов Лабораторная работа №4
- •4.1. Алифатические альдегиды и кетоны
- •Опыт 18 . Получение уксусного альдегида окислением этилового спирта дихроматом калия
- •Опыт 19. Реакции окисления альдегидов
- •Опыт 20. Альдольная и кротоновая конденсация уксусного альдегида и его осмоление
- •Опыт 21. Получение ацетона пиролизом ацетата кальция
- •4.2.Ароматические карбонильные соединения Опыт 22. Окисление бензальдегида (реакция «серебряного зеркала»)
- •Опыт 23. Получение фенилгидразона бензойного альдегида
- •Опыт 24. Получение бензальанилина (основание Шиффа)
- •Опыт 26. Получение высших жирных кислот и их свойства
- •Опыт 27. Взаимодействие бензойной и салициловой кислот с бромной водой
- •Опыт 28. Отношение бензойной кислоты к перманганату калия
- •Опыт 29. Свойства олеиновой кислоты
- •5.2. Двухосновные карбоновые кислоты Опыт 30. Свойства щавелевой кислоты
- •Опыт 31. Получение ангидрида янтарной кислоты
- •Опыт 32. Образование фталевого ангидрида
- •5.3. Сложные эфиры предельных одноосновных кислот Опыт 33. Получение этилацетата
- •Опыт 34. Гидролиз этилацетата
- •5.4. Жиры и масла Опыт 35. Определение непредельности растительного масла реакцией с бромом
- •Опыт 36. Взаимодействие растительного масла с водным раствором перманганата калия (реакция Вагнера)
- •Список рекомендуемой литературы
2. Свойства углеводородов алифатического и ароматического ряда Лабораторная работа № 2 Опыт 6. Реакция углеводородов с бромом
Реактивы и оборудование: жидкие насыщенные углеводороды, жидкие ненасыщенные углеводороды, бензол, толуол, 5%-ный раствор брома в четыреххлористом углероде.
В сухие пробирки наливают по 1 мл исследуемого раствора и добавляют по каплям раствор брома. На край каждой пробирки помещают полоску смоченной водой синей лакмусовой бумажки, и нагревают пробирки на водяной бане (осторожно, возможно воспламенение!).
В каких из пробирок жидкость обесцвечивается? Где изменяется цвет лакмусовой бумаги?

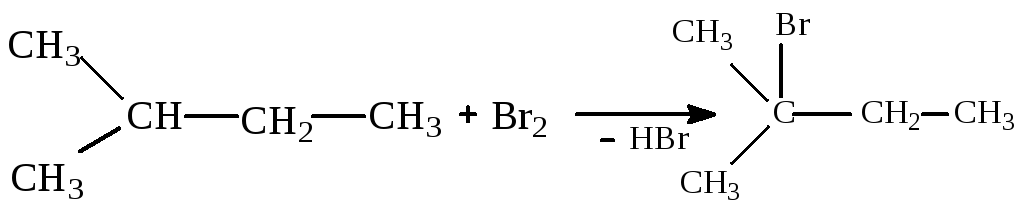
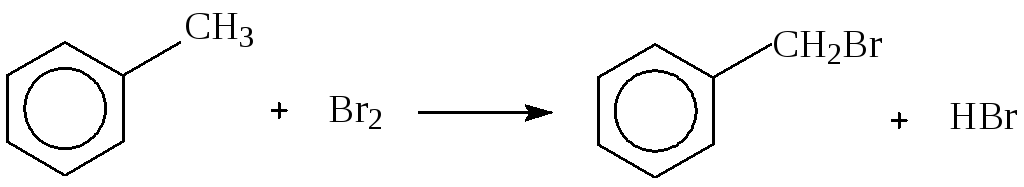
Назовите исходные и конечные продукты реакции. Сделайте вывод о том, в какие типы реакций способны вступать исследуемые углеводороды.
Опыт 7. Отношение углеводородов к окислению( реакция Вагнера)
Реактивы и оборудование: жидкие насыщенные углеводороды, жидкие ненасыщенные углеводороды, бензол, толуол, 1%-ный раствор перманганата калия, 5 %-ный раствор карбоната натрия, 10%-ный раствор серной кислоты; пробирки.
В пробирки наливают по 1 – 2 мл исследуемых углеводородов. В пробирки с алифатическими углеводородами добавляют столько же раствора соды , а в пробирки с ароматическими углеводородами - раствор серной кислоты. Во все пробирки наливают по нескольку капель раствора перманганата калия и энергично встряхивают. Отмечают, в каких пробирках изменилась окраска.
Уравнения реакций окисления:


Объясните проделанные реакции.
Опыт 8. Взаимодействие углеводородов с серной кислотой
Реактивы и оборудование: жидкие насыщенные углеводороды, жидкие ненасыщенные углеводороды, бензол, толуол, серная кислота – концентрированная.
В четыре пробирки наливают по 4 мл концентрированной серной кислоты, а затем по 0,5 мл исследуемых углеводородов. Содержимое пробирок тщательно, но осторожно встряхивают, затем нагревают в бане.
Отметьте различное отношение предельных и непредельных углеводородов к серной кислоте.
Непредельные углеводороды в кислой среде полимеризуются:

Назовите соединения и дайте определение реакции полимеризации.
Сульфирование бензола происходит только олеумом, а толуол сульфируется по уравнению:

Почему сульфирование толуола происходит по о – и п – положениям? Объясните влияние СН3 – группы на бензольное кольцо. Как доказать, что реакция прошла?
Опыт 9. Получение ацетилена и исследование его свойств
Реактивы и оборудование:карбид кальция (кусочки), насыщенная бромная вода, 0,5%-ный раствор перманганата калия, аммиачный раствор окиси серебра, аммиачный раствор закиси меди.
В сухую пробирку помещают кусочек карбида кальция, добавляют 1,5 – 2 мл воды, пробирку сразу же закрывают пробкой с отводной трубкой.
Реакция начинается мгновенно и протекает очень бурно (осторожно!), поэтому пробирки с аммиачным раствором окиси серебра аммиачным раствором закиси меди,с раствором перманганата калия и с бромной водой готовят заранее. Выделяющийся ацетилен пропускают через приготовленные заранее растворы, погружая в них поочередно конец газоотводной трубки.
Протекающие при этом реакции можно выразить уравнениями:

Назовите полученные соединения!
В какие типы реакций способны вступить алкины? В чем их отличие от алкенов?
