
- •02080165 “Экология”, 11090165 “Водные биоресурсы и аквакультура”, 08040165 “Товароведение и экспертиза товаров", колледж “Технолог”.
- •Часть II
- •Содержание
- •Введение
- •Правила техники безопасности при работе в химической лаборатории
- •Правила техники безопасности при работе с кислотами и щелочами
- •Правила техники безопасности при работе с бромом
- •Правила техники безопасности при работе с металлическими натрием и калием
- •Техника безопасности при работе с легковоспламеняющимися жидкостями
- •Техника безопасности при работе под вакуумом
- •Меры безопасности при утечке газа и тушении локального пожара и горящей одежды
- •Оказание первой медицинской помощи при ожогах и отравлениях химическими веществами
- •Лабораторная работа №1
- •1. Окси-, оксокислоты Опыт 1. Свойства оксикислот
- •Опыт 2. Свойства винной кислоты.
- •Опыт 3. Получение пировиноградной кислоты окислением молочной кислоты
- •Опыт 4. Получение пировиноградной кислоты.
- •Опыт 5. Получение фенилгидразона пировиноградной кислоты.
- •Опыт 6. Свойства ацетоуксусного эфира
- •Опыт 7. Взаимодействие бензойной, коричной и салициловой кислот с бромной водой
- •Опыт 8. Отношение бензойной, салициловой и коричной кислот к окислению
- •Опыт 9. Взаимодействие эфиров салициловой кислоты с хлоридом железа (III)
- •Лабораторная работа №2
- •2. Углеводы
- •2.1. Моносахариды Опыт 10. Качественная реакция на углеводы с α –нафтолом (реакция Молиша)
- •Опыт 11. Реакции моносахаридов по карбонильной группе
- •Опыт 12. Образование сахарата меди (II)
- •2.2. Дисахариды Опыт 13. Реакция дисахаридов с гидроксидом меди (II) в щелочной среде
- •Опыт 14. Сравнение свойств восстанавливающих и невосстанавливающих дисахаридов
- •Опыт 15. Гидролиз (инверсия) сахарозы
- •2.3. Высшие полисахариды Опыт 16. Отношение полисахаридов к реактиву Фелинга
- •Опыт 17. Взаимодействие крахмала с йодом
- •Опыт 18. Гидролиз крахмала
- •Опыт 19. Кислотный гидролиз клетчатки
- •Лабораторная работа №3
- •3. Азотсодержащие соединения Опыт 20. Свойства аминов
- •Опыт 21. Свойства аминокислот
- •Опыт 22. Свойства мочевины
- •Опыт 23. Растворимость анилина и его солей в воде. Основные свойства анилина
- •Опыт 24. Взаимодействие анилина с бромной водой
- •Опыт 25. Окисление анилина
- •Лабораторная работа №4
- •Гетероциклические соединения Опыт 26. Получение фурфурола и его свойства
- •Опыт 27. Сравнение свойств пиридина и хинолина
- •Опыт 28. Отношение пиридина и хинолина к окислению.
- •Опыт 29. Мочевая кислота
- •Список рекомендуемой литературы
Опыт 28. Отношение пиридина и хинолина к окислению.
Реактивы и оборудование:водные раствор пиридина, водный раствор хинолина, 2%-ный раствор перманганата калия, раствор соды; пробирки.
В первую пробирку наливают по 0,5 мл раствора пиридина, перманганата калия и раствор соды. Во вторую пробирку – хинолин и перманганат калия. Отметьте, в какой пробирке произошло обесцвечивание раствора. Пробирку, в которой не наблюдалось изменений, нагрейте. Что происходит?
Объясните, какое из соединений – бензол, пиридин или хинолин – проявляет более выраженный ароматический характер и почему.
Опыт 29. Мочевая кислота
Реактивы и оборудование: мочевая кислота, 10%-ный раствор гидроксида натрия, разбавленная соляная кислота, реактив Фелинга; пробирки.
Несколько кристаллов мочевой кислоты растворяют в 1—2 мл воды. Смесь нагревают и отмечают, что даже при нагревании мочевая кислота плохо растворима в воде. После охлаждения пробирки в нее приливают 10%-ный раствор гидроксида натрия до полного растворения мочевой кислоты. Образуется двузамещенная соль урат натрия. Необходимо отметить, что мочевая кислота реагирует только как двухосновная кислота.
Полученный щелочной раствор урата натрия разливают на две пробирки. В первую пробирку по каплям добавляют разбавленную соляную кислоту. Сначала выпадают кристаллы малорастворимой соли — кислого урата натрия, а при дальнейшем подкислении раствора — малорастворимой в воде мочевой кислоты:
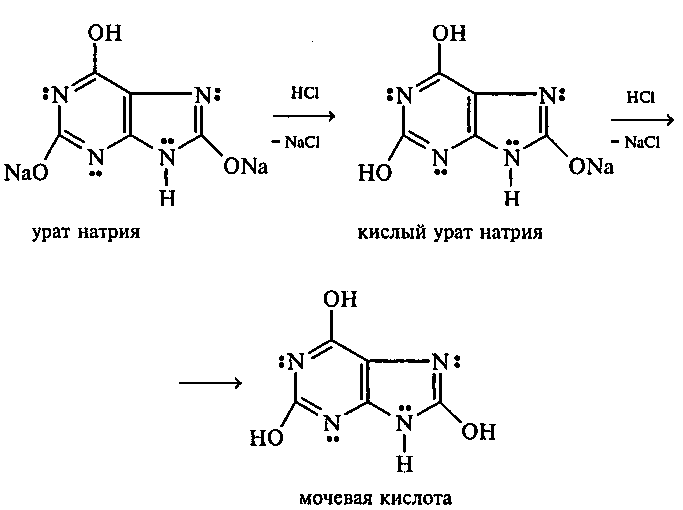
Кристаллы мочевой кислоты имеют форму удлиненных призм.
Во вторую пробирку добавляют равный объем фелинговой жидкости. Смесь нагревают на газовой горелке. Выпадает красный осадок оксида меди (I).
Таким образом, мочевая кислота легко окисляется даже слабыми окислителями:
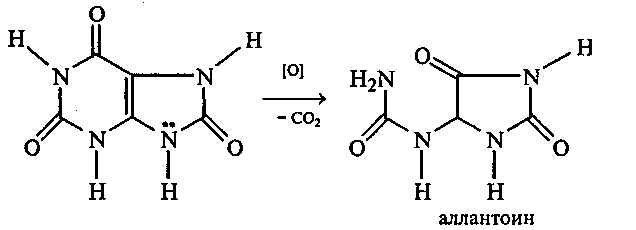
Список рекомендуемой литературы
В.Г. Иванов, О.Н. Гева, Ю.Г. Гаверова. Практикум по органической химии. - М.: Издательский центр «Академия», 2000. – 288 с.
В.В. Некрасов. Руководство к малому практикуму по органической химии. -М.: «Химия», 1975.- 328 с.
Лабораторные работы по органической химии./ Под ред. Гинзбурга О.Ф. и Петрова А.А.- М.: Высшая школа, 1982.- 269 с.
Р. Шрайнер, Р. Фьюзон, Д. Кёртин, Т. Моррилл. Идентификация органических соединений. - М.: Мир, 1983.- 704 с.
Л. Гаттерман-Г. Виланд. Практические работы по органической химии. - М.: ГХИ, 1985.-514 с.
АГТУ заказ Тираж
