
2. ОРГАНИЧЕСКАЯ_ХИМИЯ_В_СХЕМАХ_И_РИСУНКАХ
.pdf
H+
H2C  CH2 + HOH
CH2 + HOH  H3C CH2 OH
H3C CH2 OH
H2C |
|
|
CH2 |
|
H C |
|
CH |
|
|
|
|
|
|||||||
|
|
|
|
|
|||||
|
|
|
|
+ H2 |
2 |
|
|
|
3 |
H2C |
|
CH2 |
|
|
|
|
|
||
|
H C |
|
CH |
3 |
|||||
|
|
|
|||||||
|
|
|
|||||||
|
|
|
|
|
2 |
|
|
|
|
3. Реакции отщепления (или элиминирования, символ Е, от английского elimination-изъятие) - это реакции, при которых от исходной молекулы отщепляются простые или сложные вещества:
t0' кат.
H3C CH3  H2C
H2C  CH2 + H2
CH2 + H2
H C |
|
CH |
|
|
Br |
H2C |
|
CH2 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
||||||
2 |
|
|
|
2 |
+ Zn |
|
|
|
+ ZnBr2 |
|
|
|
|
|
|
|
|
|
|
||
H C |
|
CH |
|
|
Br |
H2C |
|
CH2 |
|
|
|
|
|
|
|
||||||
|
2 |
|
||||||||
2 |
|
|
|
|
|
|
|
|
||
4. Реакции перегруппировки (изомеризации) - это такие превращения, в результате которых происходит перестройка углеродного скелета, функциональной группы или изменение положения функциональной группы:
H3C |
|
CH2 |
CH2 |
CH2 |
CH3 |
t0 , Al2O3 |
H3C |
|
|
CH |
|
CH2 |
CH3 |
|||||||
|
|
|
|
|
||||||||||||||||
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
H3C |
|
C |
|
|||||||
|
|
|
|
|
H C |
|
C |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|||||||||||||||
|
2 |
|
|
|
|
|
|
|
|
H |
|
|||||||||
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
По способу разрыва и образования связей реакции делят на радикальные
иионные.
1.Радикальный или гомолитический разрыв - это такой разрыв, при ко-
тором электронная пара, осуществляющая связь, распадается симметрично, и каждый из уходящих фрагментов исходной молекулы приобретает один неспаренный электрон, т.е. превращается в радикал:
 C.
C. .X
.X 
 C. + .X
C. + .X
Такой тип разрыва характерен для неполярных или малополярных связей.
2. Ионный или гетеролитический разрыв - это такой разрыв, при кото-
ром электронная пара, образующая связь, переходит к одной из уходящих частиц, в результате чего образуются ионы:
41

 C
C  .. X
.. X 
 C+ + : X -
C+ + : X -
C .. X |
C-: + X + |
Такой тип разрыва характерен для полярных связей.
Образовавшаяся в результате гетеролитического разрыва положительная частица называется электрофилом (Elektrophil-любящий электроны) и обозначается символом Е+; отрицательная частица называется нуклеофилом (Nucleophil-любящий ядра) и имеет символ Nu
6.2 Механизм реакций радикального замещения (SR)
Механизм реакции – это описание каждого элементарного акта реакции, с указанием реакционных центров, начальных и конечных продуктов.
Типичным примером реакций SR является галогенирование алканов, протекающее в несколько стадий:
I стадия - инициирование цепи.
Под действием света или при нагревании до 400°С молекулы галогенов (хлора, брома) претерпевают гомолитический разрыв, в результате чего возникают радикалы:
Cl. .Cl |
свет |
2 Cl. |
|
II стадия - развитие цепи.
Образовавшийся радикал Сl инициирует гомолитический разрыв связи С-Н в алкане, вследствие чего возникает радикал алкил, который в свою очередь способствует расщеплению связи в другой молекуле галогена:
CH3 |
.. H + .Cl |
CH3 |
. + HCl |
|
CH |
. + Cl..Cl |
CH CI + .Cl |
||
|
3 |
|
3 |
|
Образовавшийся на последней стадии радикал хлора начинает новую цепь реакций; поэтому те реакции, в которых на одной из стадий образуются частицы, инициирующие последующие новые реакции, называются цепными. В результате цепных реакций, как правило, получается смесь моно- и полизамещенных продуктов. Так, при хлорировании метана образуются:
СН3С1, СН2Сl2 , СНС13, ССl4. III стадия - обрыв цепи.
читается «эс эр»
42

Свободные радикалы могут взаимодействовать друг с другом, в результате чего происходит обрыв цепи:
CH3. + .Cl |
CH3Cl |
CH3. + .CH3 |
CH3-CH3 |
6.3 Механизм реакций электрофильного замещения (SE )*
Типичным примером SE реакций являются галогенирование, нитрование, сульфирование, алкилирование, ацилирование аренов.
На первом этапе происходит электростатическое взаимодействие электрофильной частицы с -электронной системой и образуется -комплекс:
E+
+
+ E
-комплекс
Далее электрофил «вытягивает» из 6- -электронной системы бензольного кольца два электрона, за счет которых формируется связь между электрофилом и одним из атомов углерода бензольного ядра. Атом углерода, с которым образовалась данная связь, переходит в sp3-гибридное состояние. Образовавшийся промежуточный продукт называется -комплексом. Таким образом, при формировании -комплекса ароматическая шестиэлектронная-система разрушается, а оставшиеся четыре электрона по-прежнему делокализованы между пятью sp2-гибридными атомами углерода, что обозначается дугой, охватывающей эти атомы:
E + |
E |
|
|
|
|
+ |
|
атом углерода в |
H |
sp3-гибридном состоя нии |
-комплекс
На третьем этапе связь Сsp3-H разрывается по гетеролитическому механизму и отщепляется ион водорода (протон), а оставшаяся пара электронов возвращается в -систему, благодаря чему вновь формируется шестиэлектронная -система и ароматичность восстанавливается:
. |
E |
E |
|
+ |
.H |
+ |
H |
||
+ |
|
|
||
В качестве примера рассмотрим реакцию нитрования. Электрофильной
* читается «эс е»
43

частицей в данном случае является катион нитрония, образующийся по следующей схеме:
|
|
|
|
|
|
|
|
NO2+ + H3O+ |
_ |
|
||||
|
|
|
|
HONO2 + 2 H2SO4 |
|
+ 2 HSO4 |
||||||||
Далее реакция протекает так: |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
NO+ |
|
|
|
NO2 |
|
|
|
|
|
|
|
|
2 |
. |
|
|
|
NO2 |
|||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
+ |
|
|
|
|
.H |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
NO2 |
|
|
|
+ |
_ H+ |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бензол |
-комплекс |
-комплекс |
нитробензол |
||||||||||
6.4Механизм реакции нуклеофильного замещения (SN)* у sр3-гибридного атома углерода.
Типичным примером таких реакций являются реакции замещения в галогеналканах или спиртах. Как правило, они протекают по двум механизмам: SN1 (замещение нуклеофильное мономолекулярное) и SN2 (замещение нуклеофильное бимолекулярное)**. Термин "мономолекулярный" обозначает, что скорость реакции зависит от концентрации одного реагента, "бимолекулярный" - скорость реакции зависит от концентрации двух реагентов.
Механизм SN1 реализуется в две стадии: а) медленная диссоциация связи Сsp3-Х; б) быстрая атака образовавшегося карбкатиона нуклеофилом. Известно, что карбкатион имеет плоское тригональное строение, поэтому на второй стадии он может быть атакован нуклеофилом с разных сторон плоскости, что при наличии в исходной молекуле хирального центра приводит к образованию рацемической смеси:
|
R'' |
|
|
R'' |
|
50% _ |
R'' |
|
|
R'' |
|
|
|
|
медленно |
|
|
|
|
||||
R' |
|
Hal |
+ |
Nu |
С Nu |
+ |
|
С |
|
||
R''' |
|
-Hal |
С |
R''' |
быстро |
|
R' |
||||
|
|
|
R' |
|
Nu |
|
|||||
|
|
|
|
' |
|
|
|
R ''' |
|
||
|
|
|
|
R |
|
|
R''' |
|
|
|
|
|
|
|
|
|
|
|
50% |
|
|
50% |
|
|
|
|
|
50% |
|
|
|
|
|
|
|
Так как скорость реакции определяется наиболее медленной стадией, в которой участвует только одно вещество, то реакция относится к мономолекулярным.
Механизм SN1 наиболее характерен для третичных галогеналканов и спиртов, т.к. третичный карбкатион наиболее устойчив. Протеканию реакции по данному механизму способствуют также полярные растворители (облегчают
*читается «эс эн»
**SN1- читается «эс эн один», SN2- читается «эс эн два»
44

диссоциацию) и слабые нуклеофилы.
Механизм SN2 включает постепенное «выталкивание» замещаемой группы нуклеофилом, в результате чего нуклеофил оказывается с противоположной стороны по отношению к уходящей группе, что при наличии хирального центра в исходной молекуле приводит к обращению конфигурации (изменению на противоположную):
|
R' |
|
|
' |
|
|
|
|
_ |
|
|
- |
R |
|
|
|
R' |
|
|
|
|
|||||
Nu + |
Ñ Hal |
|
|
- |
|
|
|
|
Nu |
Ñ Hal |
-Hal- Nu |
C |
" |
||||
|
" |
|
|
|
|
|||
|
|
" |
|
''' |
|
|||
|
R |
|
|
|
|
R |
||
|
R''' |
|
R |
|
R |
|
|
R''' |
|
|
|
|
|
|
|
||
переходное состояние
Так как в формировании переходного состояния принимают участие два вещества, то реакция относится к бимолекулярным. Механизм SN2 наиболее характерен для первичных галогеналканов и спиртов, т.к. в переходном состоянии при наличии объемных заместителей могут возникать стерические затруднения. Протеканию реакций по этому механизму также способствуют малополярные растворители и сильные нуклеофилы.
6.5Механизм реакций электрофильного присоединения
(AdE)*
Типичным примером таких реакций являются реакции присоединения к непредельным углеводородам, в частности к алкенам**.
На первом этапе электрофильная частица притягивается электронами - связи, в результате чего образуется -комплекс:
 C C
C C + E+
+ E+ 
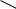 C C
C C
E+
-комплекс
На втором этапе происходит гетеролитический разрыв -связи и за счет освободившейся пары электронов электрофил присоединяется к одному из атомов углерода, образуется карбкатион:
C C |
+ |
С С |
E+ |
E |
|
карбкатион |
||
|
На третьем этапе оставшийся нуклеофил присоединяется к электронодефицитному атому углерода с противоположной стороны по отношению к электрофилу, т.е. происходит транс-присоединение:
*читается «а дэ е»
**При определенных условиях реакции присоединения в алкенах могут протекать и по радикальному механизму (AdR).
45

|
|
+ |
+ Nu |
_ |
|
|
|
|
Nu |
|||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||
С |
|
C |
|
|
C |
|
C |
|
||||
|
|
|||||||||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
E |
|
|
|
|
|
E |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
Например, реакция гидробромирования этилена протекает по схеме:
|
|
+ |
_ |
|
|
|
|
|
|
|
_ |
|
|
Br |
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|||
|
|
H-Br |
|
|
|
_ |
+ Br |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||||||
H2C |
|
CH2 |
|
H2C |
|
CH2 _ Br |
H2C CH2 |
|
H2C CH2 |
||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|||||||||||
|
|
|
|
H + |
|
H |
|
H |
|||||||
|
|
|
|
|
|
|
|
|
|||||||
Br _
-комплекс
6.6 Механизм реакций нуклеофильного присоединения (AdN)*
Типичным примером реакций AdN являются реакции присоединения к карбонильным соединениям. Так как в карбонильную группу входят разные по электроотрицательности элементы, то она полярна, причем на более электроотрицательном атоме кислорода возникает -, а на атоме углерода +. Именно поэтому карбонильный атом углерода способен взаимодействовать с нуклеофильными частицами. Известно, что карбонильная группа является плоской (оба атома, образующие ее, находятся в sp2-гибридном состоянии), значит, атака нуклеофилом равновероятна с обеих сторон плоскости, что при наличии в исходном соединении разных заместителей приводит к образованию рацемической смеси:
_ |
H |
OH |
|
|
OH |
|
|
O |
50% |
Nu |
|
|
|
||
C |
C |
|
+ |
C |
'' |
||
R'' |
'' |
|
|||||
|
+ |
|
|
|
|
|
|
|
|
R |
R' |
Nu |
Nu |
R' |
R |
R ' |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
50% |
|
|
|
|
|
|
Реакции могут катализироваться кислотами (если реагент достаточно сильный нуклеофил) и в этом случае активизируется карбонильное соединение, что показано на примере образования полуацеталей:
* читается «а дэ эн»
46

3 |
|
|
H |
|
|
|
+ |
3 |
|
+ |
|
|
|
|
.. |
||||||||
|
|
3 |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
2 5.. |
|||||||||||||||
H C |
|
|
|
_ |
+ |
|
H C |
|
|
|
H C |
|
|
|
|
|
|
C H OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
C |
|
O |
|
|
|
|
|
|
H |
C |
|
OH |
H |
C |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
H3C |
C |
|
OH |
|
|
|
|
H3C |
OH |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
+ |
|
|
|
-H+ |
|
|
C |
|
|
|
|
|
|
|
|
||||
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
O |
|
C2H5 |
|
|
|
|
H |
O |
|
C2H5 |
|
1-этоксиэтанол |
||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
H |
III |
II |
|
|
|
|
На первом этапе к карбонильному соединению присоединяется протон и формируется карбкатион (I), к которому далее присоединяется молекула спирта с образованием промежуточного соединения (II). Последнее, теряя протон (возврат катализатора), превращается в конечный продукт реакции - полуацеталь (Ш).
Если атакующая частица является слабым нуклеофилом, то для ее активизации используют основный катализ. Например, взаимодействие с циановодородной кислотой:
|
|
|
|
|
|
|
|
_ |
|
|
|
|
_ |
|
|
|
|
|
HCN |
+ OH |
|
|
HOH |
+ CN |
|
|
|||||
|
|
|
|
|
|
||||||||||
|
|
слабый |
|
|
|
|
|
сильный |
|
|
|||||
|
|
|
|
|
|
|
нуклеофил |
|
|||||||
|
нуклеофил |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
_ |
_ |
|
|
|
_ |
|
|
|
H3C |
OH |
||
|
|
|
|
|
|
|
|
||||||||
H C + |
|
|
H3C |
O |
|
HOH_ |
|||||||||
|
CN |
|
|
|
|||||||||||
3 |
C |
|
O |
|
|
|
|
|
C |
|
|
C |
|||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
-OH |
|
||||||
|
|
|
|
H3C |
H3C |
||||||||||
H3C |
|
|
|
|
|
|
|
CN |
|
|
CN |
||||
|
|
|
|
|
|
|
|
|
|||||||
возврат
катализатора
47
7. РЕАКЦИОННАЯ СПОСОБНОСТЬ И СПОСОБЫ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ В СХЕМАХ
48

Алканы (СnH2n+2)
Алканы (предельные углеводороды) - это нециклические углеводороды, в молекулах которых встречаются только одинарные связи. Мало реакционноспособны. Наиболее характерны реакции радикального замещения. . Возможны реакции горения, дегидрирования(начиная с этана), изомеризации (начиная с бутана), крекинг.
Прочие реакции |
|
Реакции замещения |
||
В обычных |
KMnO4 |
|
Cl2, свет |
|
условиях |
|
|||
устойчивы |
|
|
|
CH3-CH2Cl + HCl |
|
|
|
||
|
|
|
хлорэтан |
|
к окислению |
|
|
|
|
|
|
|
|
|
|
O2, t 0 |
|
SR |
Br2, свет |
CO2 + H2O |
|
CH3-CH3 |
|
CH3-CH2Br + HBr |
|
|
этан |
|
бромэтан |
|
Ni, t 0 |
|
|
разб. HO-NO2, t0 |
H2 + CH2=CH2 |
|
|
|
CH3-CH2-NO2 + H2O |
этен |
|
нитроэтан |
|
|
|
|
конц. HO-SO H, t0 |
|
|
3 |
CH3-CH2-SO3H + H2O |
|
|
|
|
|
этансульфокислота |
NB! При наличии в молекуле алкана первичных,
вторичных и третичных атомов углерода реакции радикального замещения преимущественно идут по третичному атому. Причина - наибольшая устойчивость третичного радикала.
Изомеризация |
|
|
|
|
|
|
|
|
||||||
H3C |
|
CH |
|
CH |
|
CH3 |
AlCl3, t |
0 |
|
|
|
|
|
|
|
2 |
2 |
|
H3C |
|
|
CH |
|
CH3 |
|||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
||||||||
|
бутан |
|
|
|
CH |
3 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Крекинг |
|
изобутан |
||||||||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
кат, t0 |
|
|
|
|
|
|
|
|
||
C10H22 |
C5H12 + C5H10 |
|
|
|
||||||||||
декан |
пентан |
пентен |
|
|
|
|||||||||
Специфические свойства некоторых алканов
1) разложение метана
1000 0 C
2CH4  HC
HC  CH + 3H2
CH + 3H2
ацетилен
конверсия метана
t0
СH4 + H2O  CO + 3H2
CO + 3H2
49

2) окисление бутана |
|
|
кат |
СH3-CH2-CH2-CH3 + 5[O] |
2CH3-COOH + H2O |
|
уксусная кислота |
Способы получения алканов
1. Гидрирование непредельных углеводородов:
|
|
|
|
|
H2, Ni |
|
|
H2, Ni |
|||||
|
|
|
|
|
|||||||||
H3C |
|
C |
|
CH |
H3C |
|
CH |
|
CH2 |
H3C |
|
CH2 |
CH3 |
|
|
|
|
|
|||||||||
|
|
|
|
||||||||||
|
|
||||||||||||
пропин |
|
пропен |
пропан |
||||||||||
2. Восстановление иодалканов:
R J + HJ
 R-H + J2
R-H + J2
H3C |
|
CH2 |
CH2J + HJ |
H3C |
|
CH2 |
CH3 + J2 |
|
|||||||
|
|
||||||
1-йодпропан |
|
пропан |
|||||
NB! Обратите внимание, что в примерах 1 и 2 число атомов углерода и порядок их соединения в исходном веществе и продукте не меняется
3. Разложение солей карбоновых кислот:
R-COONa + NaOH |
t 0 |
R-H + Na2CO3 |
|
||
|
|
t 0 |
CH3-CH2-COONa + NaO H |
CH3-CH3 + Na2CO3 |
|
пропионат натрия |
этан |
|
NB! Обратите внимание, что в продукте реакции на один атом углерода меньше, чем в исходном соединении
4. Реакция Вюрца - взаимодействие галогеналканов с металлическим натрием:
R-Hal + 2Na + Hal-R |
R-R + |
2NaHal |
CH3-CH2-Br + 2Na + Br-CH2-CH3 |
CH3-CH2-CH2-CH3 + 2NaBr |
|
бромэтан |
|
бутан |
NB! Обратите внимание, что в продукте реакции по сравнению с исходным веществом число атомов углерода увеличивается.
5. Природные источники: нефть, уголь, природный газ.
50
