
2. ОРГАНИЧЕСКАЯ_ХИМИЯ_В_СХЕМАХ_И_РИСУНКАХ
.pdf
Хиральностью обладают любые предметы, которые являются асимметрическими (несимметричными), например, правая и левая рука (правую перчатку нельзя надеть на левую руку). В химии тоже встречаются асимметричные объекты - молекулы. Например:
|
|
H |
|
|
|
|
|
|
|
|
|
H C |
|
C* |
COOH |
|
|
|
|
||||
3 |
|
|
|
|
2-гидроксипропановая |
|
|
|
|
||
|
|
OH |
|
кислота |
|
Такие молекулы имеют хиральный центр, т.е. такую структурную единицу, которая обусловливает отсутствие в молекуле элементов симметрии (ось симметрии, плоскость симметрии, центр симметрии). Наиболее часто в природе встречаются соединения, в которых хиральными центрами являются один или несколько асимметрических атомов углерода.
Все молекулы, имеющие асимметрические атомы углерода, существуют в виде пространственных изомеров, число которых определяется по формуле N=2n (где N – число стереоизомеров, n – число асимметрических атомов).
Например, вещества, в молекулах которых присутствует один асимметрический атом углерода, встречаются в виде двух пространственных изомеров (N=21=2) , что
видно на примере 2-гидроксипропановой : в этой кислоты
молекуле один асимметрический атом углерода (он обозначен *), поэтому возможны только два стереоизомера:
|
COOH |
|
COOH |
|||
|
* |
|
|
* |
|
|
H |
C |
|
OH |
HO |
C |
H |
|
|
|
||||
|
CH3 |
H3C |
|
|
||
|
|
|
|
|||
|
I |
|
|
|
II |
|
Соединения I и II называются энантиомерами (антиподами, зеркальными изомерами, оптическими изомерами).
Энантиомеры – это пространственные изомеры, молекулы которых являются зеркальным отражением друг друга.
Все энантиомеры, являются хиральными соединениями и обладают оптической активностью.
Оптическая активность – это способность вещества вращать плоскость плоскополяризованного света.
Если раствор вещества вращает плоскость плоскополяризованного света вправо (по часовой стрелке), то вещество называют правовращающим, если влево (против часовой стрелки) - левовращающим. Правое вращение обозначают символом (+) , левое - символом (-). Определяют знак вращения в стандартных условиях с помощью прибора поляриметра. Угол, на который вещество поворачивает плоскополяризованный свет, является величиной постоянной, называется удельным вращением, обозначается символом и служит важнейшей характеристикой при определении подлинности многих
31

лекарственных веществ, молекулы которых хиральны.
Рацемической смесью называется смесь равных количеств энантиомеров.
Рацемическая смесь оптически неактивна.
4.2 Свойства хиральных соединений
Все физические и химические свойства энантиомеров в симметричном окружении идентичны. В несимметричном окружении свойства энантиомеров могут различаться: энантиомеры вращают плоскость поляризованного света в равной степени, но в противоположные направления; с другими хиральными соединениями они реагируют с разными скоростями. На этом основано действие многих биологически активных веществ, например, ферментов.
4.3 Правила работы с проекционными формулами Фишера
Для изображения оптических изомеров обычно используют формулы Фишера.
Формула Фишера - это проекция тетраэдрической модели на плоскость, ориентированной таким образом, чтобы горизонтальная пара связей была обращена к наблюдателю, а вертикальная удалена от него.
a
b c
d
Заместители b и c обращены к наблюдателю, a и d- находятся за плоскостью листа
В общем случае одна тетраэдрическая модель может дать 12 проекционных формул Фишера (в зависимости от ориентации тетраэдра в пространстве). Однако обычно углеродную цепь располагают сверху вниз в соответствии с нумерацией атомов углерода в соединении. Хиральный центр подразумевается на пересечении горизонтальной и вертикальной линий и в формуле не указывается.
3 |
2* |
1 |
|
|
|
|
|
з |
|
|
|
|
|
|
|||
|
|
|
COOH |
|
е |
|
|
COOH |
|||||||||
H3C |
|
|
CH |
|
COOH |
|
|
|
|
||||||||
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
* |
|
|
р |
|
|
|
|
* |
|
|
|
OH |
|
|
H |
|
OH |
HO |
|
|
H |
||||||
|
|
|
|
|
к |
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
а |
|
|
CH3 |
|
||||
|
|
|
|
|
|
|
|
л |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
о |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
энантиомеры |
|
||||||
Для сопоставления различных |
формул |
Фишера |
одного |
и того же |
|||||||||||||
|
|
|
|
|
|
32 |
|
|
|
|
|
|
|
|
|
||

вещества используют следующие правила: -формулы Фишера нельзя:
а) выводить из плоскости чертежа; б) рассматривать “на просвет” с обратной стороны бумаги;
-формулы Фишера можно:
в) вращать в плоскости чертежа на 1800;
|
COOH |
|
|
CH3 |
||||||
H |
|
|
|
OH |
|
HO |
|
|
|
H |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||||
|
CH3 |
|
|
COOH |
||||||
поворот на 1800 
г) делать в них четное число перестановок заместителей;
|
COOH |
первая |
|
|
COOH |
|
вторая |
|
COOH |
|||||||||
H |
|
|
|
OH |
перестановка |
H |
|
|
|
CH3 |
перестановка |
HO |
|
|
|
CH3 |
||
|
|
|
поменяли СН3 и OH |
|
|
|
поменяли Н и OH |
|
|
|
||||||||
|
CH3 |
|
|
OH |
|
H |
||||||||||||
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
антипод
идентичны
д) вращать три заместителя по часовой стрелке.
COOH |
COOH |
COOH |
H  OH
OH  H3C
H3C  H
H  HO
HO CH3
CH3
CH3 |
OH |
H |
Вещество может содержать два и более асимметрических атомов углерода. Такое вещество имеет несколько стереоизомеров. Общее число возможных стереоизомеров определяют по формуле N=2n, где n-число хиральных центров.
Например, для 2,3-дигидроксибутановой кислоты, имеющей 2 хиральных центра, существует 22=4 стереоизомера:
|
|
|
|
|
|
|
|
* |
* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
CH |
3 |
|
CH |
|
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
COOH |
|
|
COOH |
|
|
|
|
|
|
|
COOH |
|
|
|
|
COOH |
|||||||||||||||
H |
|
|
|
OH |
HO |
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
OH |
|
HO |
|
|
|
|
H |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
H |
|
|
|
OH |
HO |
|
|
|
|
H |
|
|
|
|
|
HO |
|
|
|
|
H |
|
H |
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
CH3 |
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
CH3 |
|||||||||||||||
|
|
|
I |
|
|
II |
|
|
|
|
|
|
|
|
III |
|
|
|
|
|
IV |
||||||||||||
I и II; |
III и IV – энантиомеры (зеркальные изомеры, антиподы); |
|
|
|
|
||||||||||||||||||||||||||||
I и III; |
I и IV; |
II и III; II и IV - диастереомеры. |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
Диастереомеры – это пространственные изомеры, не являющиеся |
|||||||||||||||||||||||||||||||||
энантиомерами (В |
таких |
стереоизомерах конфигурации |
атомных |
групп у |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
33 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

одних хиральных центров совпадают, а у других – зеркально противоположны). Для веществ типа Cabd-Cabd существует меньшее число стереоизомеров. Например, 2,3-дигидроксибутандиовая (винная) кислота имеет три
стереоизомера.
|
|
|
|
|
|
|
|
* * |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
HOOC |
|
CH |
|
CH |
|
COOH |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
OH OH |
|
|
|
|
|
|
||||||||
|
COOH |
|
|
|
COOH |
|
|
COOH |
||||||||||||||
H |
|
|
|
|
OH |
HO |
|
|
|
|
|
|
H |
H |
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
HO |
|
|
|
|
H |
H |
|
|
|
|
|
|
OH |
H |
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
COOH |
|
|
|
COOH |
|
|
COOH |
||||||||||||||
|
I |
|
|
|
II |
|
|
III |
||||||||||||||
Формулы I и II изображают энантиомеры. Если к формуле III построить зеркальный изомер, то при внимательном рассмотрении окажется, что это идентичные формулы, т.к. превращаются друг в друга при повороте на 1800.
Формула III изображает оптически неактивное вещество, называемое мезоформой.
Формулы I и II изображают оптически активные вещества, так как их молекулы несимметричны; формула III изображает оптически неактивное вещество, так как симметрична (имеет плоскость симметрии).
COOH
плоскость H  OH
OH
симметрии H  OH
OH
COOH III
Мезо-формами называются оптически неактивные вещества с четным числом асимметрических атомов углерода, имеющие плоскость симметрии.
5. СТЕРЕОХИМИЧЕСКАЯ НОМЕНКЛАТУРА
Согласно правилам ИЮПАК названия органических веществ, отражающие их пространственное строение, строятся с помощью приставок: D-,L-;R-,S-; мезо-; эритро-, трео-; цис-, транс-; E-, Z- и др. Эти приставки добавляются к систематическим названиям .
5.1 D-, L-система обозначений
В настоящее время эта система в основном применяется в номенклатуре аминокислот, гидроксикислот и углеводов.
Чтобы отнести вещество к D-,L-стереохимическим рядам, конфигурацию (пространственное строение) его молекулы сравнивают с конфигурацией
34

стандарта – глицеринового альдегида:
|
|
|
|
|
* |
|
|
O |
|
|
|||
|
|
|
|
|
CH |
|
|
CH |
|
C |
|
|
|
|
|
|
|
|
2 |
|
H |
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH OH |
|
|
||||||
|
|
|
|
|
|
|
|
||||||
|
|
|
O |
|
|
|
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
C H |
|
|
|
|
|
|
|
C H |
||||
H |
|
|
|
OH |
D(+) глицериновый |
HO |
|
H |
|||||
|
|
|
|
||||||||||
|
CH2OH |
|
CH2OH L(-) глицериновый |
||||||||||
|
альдегид |
|
|||||||||||
|
|
|
|
|
|
|
альдегид |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Если конфигурация молекулы совпадает с конфигурацией D-глицеринового альдегида, – это вещество D-ряда, и, соответственно, L-ряда, если конфигурация совпадает с конфигурацией L-глицеринового альдегида.
Например:
H3C |
|
|
|
|
CH |
|
COOH |
2-аминопропановая кислота (аланин) |
|||||||||
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
||||
Формула Фишера одного из изомеров: |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
COOH |
совпадает с конфигурацией |
|
C |
H |
|||||||||||
|
|
D - глицеринового альдегида |
|
||||||||||||||
H |
|
|
|
|
|
|
NH2 |
H |
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
CH3 |
|
|
|
CH2OH |
|||||||||||
D(-)аланин |
D(+) глицериновый альдегид |
|
Если формула Фишера записана нестандартно, ее следует преобразовать по вышеизложенным правилам в соответствии с нумерацией атомов углерода в углеродной цепи (см. стр. 32). Если при этом группы ОНили NH2- окажутся справа, то вещество имеет D-конфигурацию, если слева – L-конфигурацию. Например, формула Фишера одного из изомеров 2,3-дигидроксипропановой кислоты записана в виде I. Привести ее к стандартной форме записи можно путем поворота в плоскости листа на 180 (формула II). Сравнение с формулой эталона показывает, что вещество имеет L-конфигурацию.
|
|
|
|
|
* |
|
|
|
|
|
|
|
2,3 - дигидроксипропановая кислота |
|
|
||||||
|
|
|
|
|
HO |
|
CH2 |
|
CH |
|
|
COOH |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|||
|
3 CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||
|
поворот на |
1COOH |
совпадает с конфигурацией |
|
C |
H |
|||||||||||||||
|
2 |
|
|
|
1800 |
|
|
|
|
|
|
|
|
|
|
L-глицеринового альдегида |
|
|
|||
H |
|
|
OH |
|
HO |
|
2 |
|
|
|
H |
HO |
|
|
H |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
1COOH |
|
|
|
|
|
|
|
3CH OH |
|
|
CH OH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
2 |
|
||
|
|
|
I |
|
|
|
|
|
|
|
|
II |
|
L(-) глицериновый |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
35

5.2 R-,S-система обозначений
Эта система используется для всех оптически активных веществ. Чтобы отнести вещество к R,S-стереохимическим рядам:
1. Определяют старшинство заместителей по правилу последовательности Кана-Ингольда-Прелога.
Согласно этому правилу:
1) старшинство заместителей устанавливают по атомам 1-го слоя (т.е. атомам, непосредственно связанным с асимметрическим атомом углерода). Старшим считается заместитель, содержащий атом с большим порядковым номером в периодической системе элементов;
2) если с хиральным центром связано два или несколько одинаковых атомов, старшинство устанавливается по второму слою (т.е. атомам непосредственно связанным с атомами первого слоя). При этом старшинство зависит от наличия и числа атомов с большим порядковым номером;
3)если по второму слою старшинство определить не удается, используют атомы третьего слоя и т. д.;
4)если в состав заместителя входят атомы, связанные двойной или тройной связью, то их число соответственно удваивается или утраивается.
Согласно приведенным правилам заместители, содержащие атомы углерода, можно расположить в порядке уменьшения старшинства следующим образом:
C O , |
|
C O |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||||||
|
, |
|
CH2OH , |
|
C6H5 , |
|
C |
|
CH , |
|
C |
|
CH3 , |
|
CH=CH2 , |
|
C2H5 , |
|
CH3 |
|||
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
OH |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
2. Формулу Фишера преобразуют по вышеизложенным правилам (см. стр. 32) так, чтобы младший заместитель оказался внизу (что будет соответствовать его наибольшему удалению от наблюдателя в стереохимической формуле).
3. Устанавливают, как падает старшинство заместителей: если по часовой стрелке –это вещество R-ряда, если против часовой стрелки -это вещество S-ряда.
Например: Пример 1.
HOOC CH CH2OH
NH2
2-амино-3-гидроксипропановая кислота (серин)
стереохимическая формула одного из изомеров
36

наблюдатель
|
COOH |
|
|
|
N |
|
H |
1 |
||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||
H2N |
C |
H |
Наиболее удален |
|
H |
|
|
|||||||
|
|
от наблюдателя |
|
O |
|
|
||||||||
|
|
CH2OH |
|
|
|
|||||||||
|
|
|
|
|
|
C |
|
O0 |
2 |
|||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
H |
|
|
||
|
|
|
|
|
|
|
C |
|
|
H |
3 |
|||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
O |
|
H |
||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
H |
|
|
|
|
4 |
|||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
I |
|
II |
|
III |
||||
|
|
|
|
|
слой слой слой |
|||||||||
С асимметрическим атомом углерода связаны заместители: -NH2, -COOH, -CH2OH, -H. В первый слой входят атомы: N, C, C и H, имеющие соответственно порядковые номера: 7, 6, 6 и 1. Следовательно, по первому слою устанавливают, что самой старшей является группа –NH2, а самым младшим – водород. Чтобы сравнить старшинство групп -COOH и -CH2OH, надо сравнить атомы второго слоя: в группе –COOH второй слой содержит три атома кислорода [O, O, O0], в группе -CH2OH два водорода и один кислород. Следовательно, COOHгруппа старше CH2OHгруппы. Между всеми четырьмя заместителями старшинство распределяется так: -NH2; -COOH; -CH2OH; -H.
|
2 |
|
|
2 |
|
||
|
COOH |
|
COOH |
||||
|
|
|
|
|
|
|
|
1 |
C |
H энантиомер этого вещества |
3 |
C |
H |
||
H2N |
|
|
3 |
HOH2C |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
NH2 |
|
|
|
S -2 -амино -3-гидрокси- |
||||
R -2- амино -3 -гидрокси- |
пропановая кислота |
||||||
пропановая кислота |
|
|
|
|
|||
Пример 2.
OH
H2N CH2 CH CH3
1-аминопропанол-2
37

Формула Фишера одного из изомеров:
CH2NH2
H 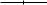 OH
OH
CH3
|
|
|
|
H |
|
H |
4 |
|||||||
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
N |
|
H 2 |
|||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
C |
|
|
|
|
H |
3 |
|||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
O |
|
|
|
H |
1 |
|||
|
|
|
|
|
|
|
||||||||
|
|
|
|
I |
|
II |
|
III |
||||||
слой слой слой
1.Определяют старшинство заместителей. Порядок уменьшения старшинства: -OH> -CH2NH2> -CH3> -H.
2.Преобразуют проекцию Фишера так, чтобы младший заместитель был внизу, а старшинство остальных изменялось плавно:
|
CH2NH2 |
первая |
|
CH2NH2 |
вторая |
|
CH2NH2 |
H |
OH |
перестановка |
H3C |
OH |
перестановка |
HO |
CH3 |
|
|
||||||
|
CH3 |
|
|
H |
|
|
H |
R -1 -аминопропа- нол -2
Примечание:
1)D-, L-система часто используется для обозначения относительной конфигурации, а R-, S-система – для обозначения абсолютной конфигурации.
Термин «относительная конфигурация» согласно правилам ИЮПАК используется для описания положения заместителей у разных атомов молекулы друг относительно друга. Термин «абсолютная конфигурация» используют для описания пространственного положения заместителей вокруг хирального центра.
2)Обозначения (+) и (-) перед названиями веществ не связаны с приставками D-, L-, R- и S- и могут быть определены только с помощью поляриметра.
В номенклатуре диастереомеров используют приставки:
1) мезо- для соединения с двумя одинаковыми асимметрическими атомами типа Cabd-Cabd
38

CH3
H Cl мезо -2,3 -дихлорбутан
H Cl
CH3
2) эритро- и трео- для соединений с двумя разными асимметрическими атомами типа Савd-Caвf или Савd-Cafe. При стандартном написании проекционной формулы Фишера у эритро-изомера одинаковые (или родственные) заместители расположены по одну сторону проекционной формулы, у трео-изомера по разные
|
|
CH3 |
|
CH3 |
|
|
CH3 |
|
|
CH3 |
||||||||
H |
|
|
Cl |
Cl |
|
|
H |
Cl |
|
|
|
H |
H |
|
|
Cl |
||
|
|
|
|
|
|
|
|
|
||||||||||
H |
|
|
|
Br |
Br |
|
|
H |
H |
|
|
Br |
Br |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
CH3 |
|
CH3 |
|
|
CH3 |
|
|
CH3 |
||||||||
эритро- |
эритро- |
|
|
трео- |
|
|
трео- |
|||||||||||
|
|
|
|
|
|
|
||||||||||||
3) цис-, транс- для обозначения конфигурации геометрических изомеров. Приставка цисиспользуется в том случае, когда одинаковые или сходные заместители расположены по одну сторону, а приставку транспо разные стороны общей для стереоизомеров плоскости сравнения (плоскости двойной связи или плоскости цикла).
Например:
|
H |
H |
H3C |
|
|
|
H |
|||||
|
C |
|
C |
|
|
C |
|
C |
||||
|
|
|
|
|||||||||
|
|
|
|
|||||||||
H3C |
CH2 |
CH3 |
|
H |
|
|
|
CH2 |
CH3 |
|||
цис-пентен-2 |
транс-пентен-2 |
|||||||||||
H H |
|
|
H |
CH3 |
||||||||
|
|
|
|
|
|
|
|
|
||||
CH3 CH3 |
|
|
CH3 |
H |
||||||||
цис-1,2-диметилциклопропан транс-1,2-диметилциклопропан
4) Е-, Z- для обозначения конфигурации геометрических изомеров. Может быть применима во всех случаях.
Приставка Z- (от немецкого слова zusammen – вместе) используется в случае, когда два старших заместителя лежат по одну сторону плоскости сравнения.
Приставка Е -(от немецкого слова entgegen – напротив) используется в случае, когда два старших заместителя лежат по разные стороны плоскости сравнения.
Старшинство заместителей определяют по правилу последовательности Кана-Ингольда-Прелога (см. стр. 36) среди каждой пары заместителей связанных с одним и тем же атомом углерода.
39
Например:
старший H3C |
|
COOH старший |
старший H C |
|
|
CH |
3 |
младший |
C |
|
C |
3 |
C |
|
C |
|
|
|
|
|
|
|
||||
младший H |
|
CH3 младший |
младший H |
|
|
|
||
|
|
|
COOH старший |
|||||
Z -2 -метилбутен -2-овая кислота |
E -2 -метилбутен -2-овая кислота |
|
Примечание: кроме понятия конфигурация в стереохимии большое значение имеет понятие конформация.
Конформации (или конформационные изомеры) – это формы, которые приобретает молекула только путем свободного вращения атомов вокруг связей. В отличие от конфигурационных изомеров конформационные изомеры быстро превращаются друг в друга и не поддаются разделению.
Большое значение имеют конформации циклических систем, например циклогексана
конформация ванны (лодки)  конформация кресла
конформация кресла
6. КЛАССИФИКАЦИЯ И МЕХАНИЗМЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
6.1 Классификация реакций
Органические реакции можно классифицировать по: I - направлению реакций;
II - способу разрыва и образования связей.
По направлению различают реакции замещения, присоединения, отщепления, перегруппировки.
1.Реакции замещения (символ S, от английского substitution-замещение)
-это реакции, при которых атом или группа атомов в соединении замещаются на другой атом или группу атомов:
CH4 + Cl2 |
свет |
CH3Cl + |
HCl |
|
C2H5Cl + NaOH (водный)  C2H5OH + NaCl
C2H5OH + NaCl
2. Реакции присоединения (символ Ad, от английского aduition -
присоединение) - это реакции, при которых одна молекула присоединяется к другой:
40
