
- •Тема 1. Атомно-кристаллическое строение металлов
- •Энергия межатомной связи и свойства металлов
- •911 1392 -Fe -Fe -Fe (-Fe).
- •Тема 2. Деформация, разрушение и механические свойства металлов Упругая и пластическая деформация. Пути повышения прочности
- •Наклеп и рекристаллизация
- •Холодная и горячая деформация
- •Механические свойства металлов
- •Тема 3. Основы теории сплавов. Диаграммы состояния
- •Практическое значение диаграмм состояния
- •Тема 4. Диаграмма состояния железо–цементит
- •Критические точки
- •Тема 5. Превращения в сталях при нагреве и охлаждении
- •Тема 6. Основные виды термической обработки сталей
- •Тема 7. Основы легирования сталей
- •Особенности термической обработки легированных сталей
Практическое значение диаграмм состояния
Основоположником учения о связи диаграмм состояния со свойствами сплавов является академик Н.С. Курнаков. В общем виде зависимость свойств от химического состава сплава (типа диаграммы) приведена на рис. 10.
В сплавах, компоненты которых не растворяются друг в друге и не образу-ют химических соединений, свойства изменяются в основном прямолинейно. В сплавах, имеющих структуру твердых растворов, свойства изменяются по криволинейной зависимости, то есть более существенно, чем для сплавов, имеющих структуру смеси кристаллов. При образовании химических соединений на графике отмечается характерный перелом. Это объясняется тем, что химические соединения обладают индивидуальными свойствами, обычно резко отличающимися от свойств образующих их компонентов.

Закономерности, обнаруженные Н. С. Курнаковым, являются основой при разработке составов сплавов с заданными свойствами. Следует отметить, что указанные закономерности справедливы для оценки не только механических, но и физических, а также многих технологических свойств сплавов. Так, например, для системы А–В, диаграмма состояния которой представлена на рис. 11, можно следующим образом прогнозировать свойства сплавов по сравнению с заранее известными свойствами чистых компонентов:
а) твердость, прочность и электросопротивление твердых растворов и выше, чем у чистых металлов (кривые 1 и 2, отрезки аб и вг);
б) электропроводность и температурный коэффициент электросопротив- ления у твердых растворов ниже, чем у чистых металлов (кривые 3 и 4, отрезки аб и вг);
в) литейные свойства лучше у эвтектического сплава (кривые 5 и 6). Известно, что технологические литейные свойства, определяющие способность сплава при затвердевании давать высококачественные слитки или отливки, зависят от жидкотекучести, склонности к образованию трещин внутри и на поверхности слитков, возможности формирования концентрированной усадочной раковины.
Жидкотекучесть – это способность расплава заполнять литейную форму сложной конфигурации. Чем больше температурный интервал кристаллизации, тем ниже жидкотекучесть; одновременно увеличивается склонность образовывать трещины и мелкую пористость, рассеянную по всему объему
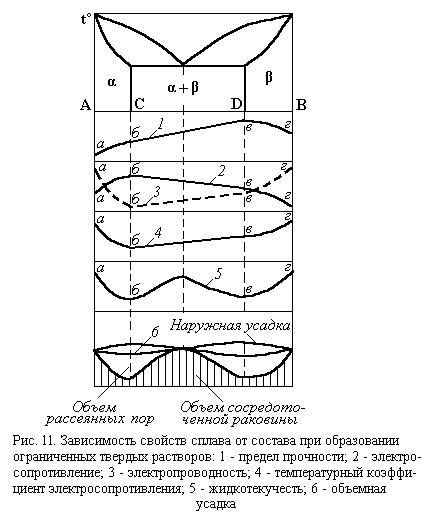
отливки, что нередко выводит литье в брак. Поэтому однофазные сплавы со структурой твердого раствора, особенно сплавы, составы которых находятся близко к предельным точкам С и D, обладают плохими литейными свойствами и непригодны для фасонного литья. Однако эти сплавы имеют высокое сопротивление коррозии и хорошую технологическую пластичность, необходимую для изготовления деталей методами обработки металлов давлением (прокатка, прессование, ковка и др.). Пластичность сильно понижается при появлении в структуре эвтектики.
Таким образом, диаграммы состояния позволяют на научной основе предвидеть поведение сплавов и выбирать материалы в зависимости от их назначения.
Тема 4. Диаграмма состояния железо–цементит
О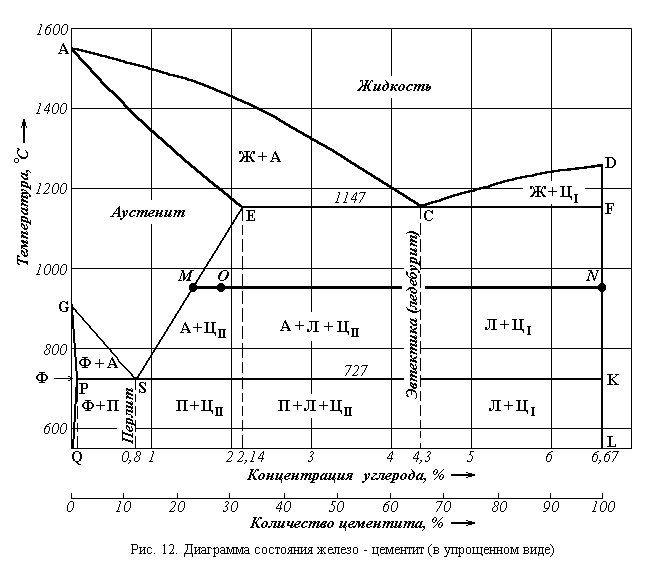 сновой
науки о стали и чугуне является диаграмма
системы сплавов железо–углерод. Железо
с углеродом образуют три химических
соединения: Fe3C,
Fe2C,
FeC. Однако практическое значение имеют
сплавы, содержащие не более 5 % углерода,
поэтому рассматривают лишь первую
часть общей диаграммы: систему
железо–цементит (рис. 12).
сновой
науки о стали и чугуне является диаграмма
системы сплавов железо–углерод. Железо
с углеродом образуют три химических
соединения: Fe3C,
Fe2C,
FeC. Однако практическое значение имеют
сплавы, содержащие не более 5 % углерода,
поэтому рассматривают лишь первую
часть общей диаграммы: систему
железо–цементит (рис. 12).
В зависимости от температуры и концентрации углерода железоуглеродистые сплавы имеют следующие структурные составляющие:
феррит (Ф) – твердый раствор внедрения углерода в -железе, кристаллическая решетка ОЦК. Растворимость углерода в -железе мала (область на диаграмме GPQ). Механические свойства: В = 250 Н/мм2; 0,2 = = 120 Н/мм2; = 50 %; KCU = 2,5 МДж/м2; твердость 80 НВ;
аустенит (А) – твердый раствор внедрения углерода в -железе. Он имеет решетку ГЦК, межатомные поры в которой больше, чем в ОЦК решетке, поэтому растворимость углерода в -железе значительно больше (область на диаграмме GSE) и достигает 2,14 % при 1147 С. Аустенит пластичен ( = = 40…50 %), но прочнее феррита (160…200 НВ);
цементит (Ц) – химическое соединение железа с углеродом – карбид железа
Fe3C, содержит 6,67 % углерода. Цементит твердый ( 800 НВ) и хрупкий;
перлит (П) – двухфазная структура, состоящая из феррита и цементита (эвтектоид), содержит 0,8 % углерода. Перлит может быть пластинчатым или зернистым в зависимости от формы цементита (пластинки или глобулярные частицы). Свойства зернистого перлита: В = 800 Н/мм2; = 15 %; твердость 160 НВ. Пластинчатый перлит имеет твердость до 200 НВ. Чем грубее и крупнее выделения цементита, тем хуже механические свойства перлита;
ледебурит (Л) – эвтектика, образуется во время затвердевания расплава при температуре 1147 С, содержит 4,3 % углерода. Различают высокотемпера-турный ледебурит (смесь аустенита и цементита) и низкотемпературный ледебурит (смесь перлита и цементита). Ледебурит имеет твердость 600 НВ и высокую хрупкость.
Сплавы с содержанием углерода до 2,14 % называют сталями, а от 2,14 до 6,67 % углерода – чугунами. Стали при нагреве можно перевести в одно-фазное состояние, которое обладает высокой пластичностью. Поэтому стали в горячем состоянии хорошо поддаются обработке давлением: прокатке, ковке, штамповке. Чугуны при нагреве не дают однофазной структуры вплоть до плавления. Ледебуритная эвтектика, присутствующая в структуре, затрудняет обработку резанием и давлением. В то же время наличие эвтектики улучшает литейные свойства. Поэтому чугуны относятся к литейным материалам.
С помощью диаграммы железо–цементит можно определить фазовый состав и структуру сталей и чугунов, а также описать превращения, происходящие в любом сплаве при затвердевании.
Пример. Для сплава, содержащего 1,8 % углерода, определить процентное содержание углерода в фазах и количественное соотношение фаз при температуре 850 С.
Решение. Для решения этой задачи найдем на рис. 12 точку О, соответствующую заданному составу и температуре. В структуре сплава в этих условиях будут две однофазные составляющие, то есть две фазы: аустенит и цементит. Для определения состава и количества фаз при рассматриваемой температуре необходимо через данную точку О провести горизонтальную линию, параллельную оси концентрации, до пересечения с ближайшими сплошными линиями диаграммы состояния (линия ES и вертикальная ось). Эта линия называется конодой. Точка пересечения коноды с линией ES, спроектированная на ось концентраций, показывает состав аустенита
(концентрацию углерода в аустените), а точка пересечения с вертикальной осью – состав цементита. Таким образом, в аустените содержится 1,5 % С, в цементите 6,67 % С.
Для определения количественного соотношения фаз воспользуемся правилом отрезков. Конода делится конкретным составом сплава на два отрезка. Для определения количества аустенита нужно взять отношение длины отрезка, противоположного составу данной фазы, к длине всей коноды:
количество аустенита = ON/MN100 % =
= (6,67 – 1,8) / (6,67– 1,5) 100 % = 94 %;
количество цементита = 100 % 94 % = 6 %.
Температуры, при которых происходят фазовые превращения, называются критическими точками. Они обозначаются буквой А с индексами: с – для нагрева, r – для охлаждения. Характеристика основных критических точек железоуглеродистых сплавов в равновесном состоянии приведена в табл. 2.
Таблица 2
