
- •Политехнический институт Кафедра промышленной энергетики
- •Правила выполнения лабораторных работ и оформления отчетов
- •Работа № 1
- •Выполнение работы
- •Расчетные формулы и расчеты
- •6. Контрольные вопросы
- •Работа № 2 определение параметров влажного воздуха
- •Цель работы
- •2. Основные положения
- •3. Схема и описание установки
- •Выполнение работы
- •5. Расчетные формулы и расчеты
- •Контрольные вопросы
- •Работа № 3 исследование процесса истечения воздуха через суживающееся сопло
- •1. Цель работы
- •2. Основные положения
- •3. Схема и описание установки
- •Выполнение работы
- •5. Расчетные формулы и расчеты
- •6. Контрольные вопросы
- •Работа № 4 определение коэффициента теплопроводности теплоизоляционного материала
- •1. Цель работы
- •2. Основные положения
- •3. Схема и описание установки
- •4. Выполнение работы
- •5. Расчетные формулы и расчеты
- •6. Контрольные вопросы
- •Работа № 5 теплоотдача вертикального цилиндра при естественной конвекции
- •1. Цель работы
- •2. Основные положения
- •3. Схема и описание установки
- •4. Выполнение работы
- •5. Расчетные формулы и расчеты
- •6. Контрольные вопросы
- •Работа № 6
- •3. Схема и описание установки
- •4. Выполнение работы
- •5. Расчетные формулы и расчеты
- •6. Контрольные вопросы
- •Температура и методы ее измерения
- •1. Цель работы
- •2. Температура - мера кинетической энергии составляющих тело молекул
- •3. Температурные шкалы
- •4. Методы измерения температуры
- •5. Контрольные вопросы
6. Контрольные вопросы
1. Сформулируйте цель лабораторной работы и поясните, как она достигается?
2. Назовите основные узлы экспериментальной установки и укажите их назначение.
3. Какими методами измеряется температура в данной работе?
4. Как измеряется и регулируется расход воздуха в данной работе?
5.По каким признакам можно судить о стационарном режиме теплообмена с окружающей средой?
6. Как осуществляется выбор контрольной оболочки рассматриваемой термодинамической системы?
7.Дайте формулировку и математическое выражение уравнения первого закона термодинамики, используемого для решения задачи данного опыта.
8. Укажите способы определения величин, входящих в уравнение 1-го закона термодинамики, используемого для решения задачи данного опыта, с полным обоснованием используемых расчетных формул.
9. Какие существуют методы и приборы для измерения температуры, давления и расхода?
10. Как определяется плотность воздуха в условиях лабораторной установки?
11. Какие виды конвекции существуют, в чем их различие?
12. В чем сущность "Теории подобия" и как с ее помощью определяются коэффициенты теплоотдачи?
13. Как составляются критериальные уравнения?
14. Составьте в общем виде критериальные уравнения для вынужденной и свободной (естественной) конвекции.
15. Каков физический смысл критериев подобия, входящих в уравнение для свободной конвекции?
16. Каков физический смысл критериев подобия, входящих в уравнение для вынужденной конвекции?
17. Что такое "определяемый" и "определяющий" критерий?
18. Как выбирается определяющий (характерный) размер и определяющая температура при расчете критериев подобия?
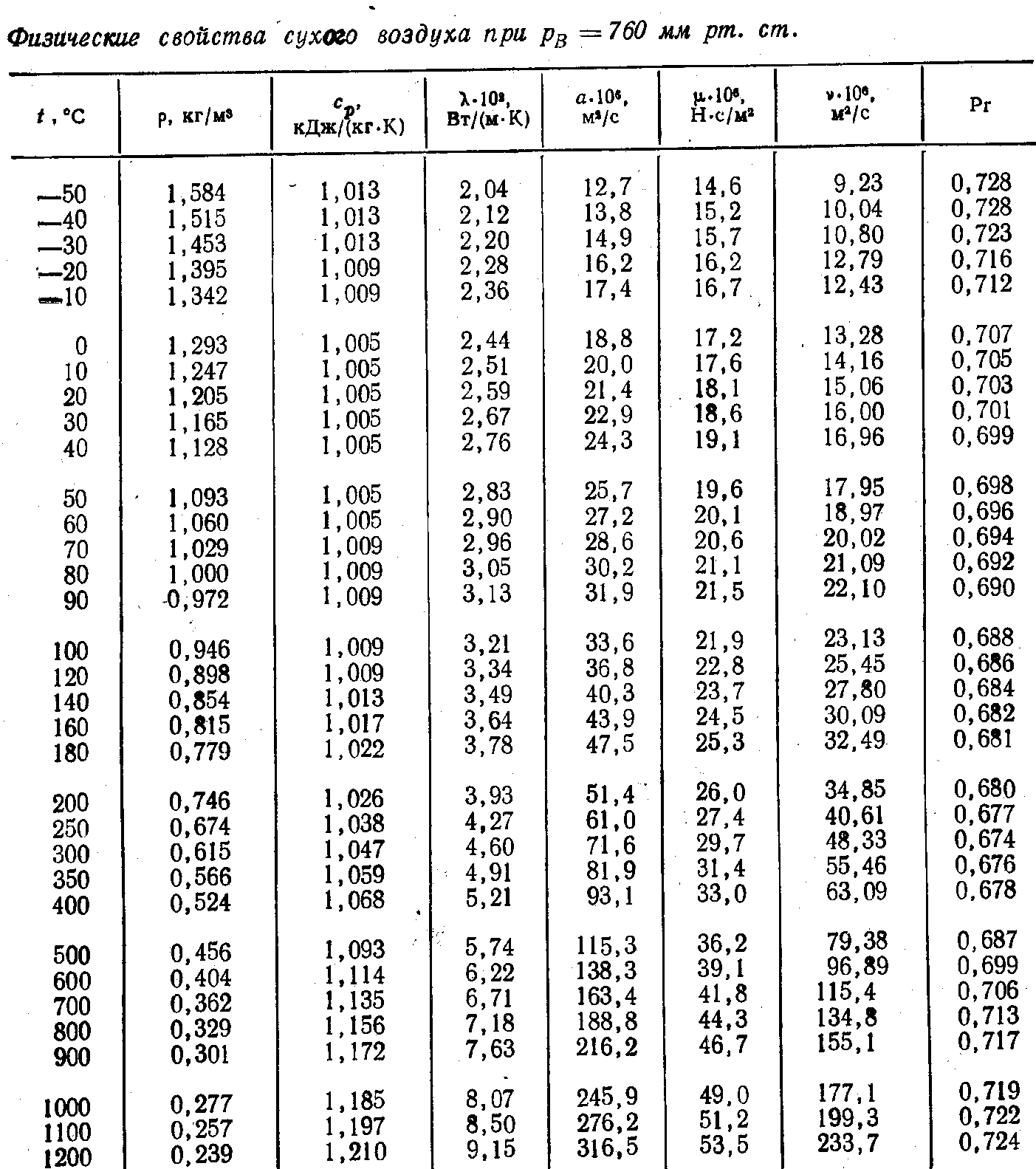
Таблица 3
Лабораторная работа № 7
Температура и методы ее измерения
1. Цель работы
Ознакомление с понятием температуры и методами ее измерения.
2. Температура - мера кинетической энергии составляющих тело молекул
Температура является основным термическим параметром системы. Она является мерой нагретости тела. Температура определяет направление передачи теплоты. Если температура первого тела t1°С, выше, чем температура второго тела t2°С, то при тепловом контакте тел теплота передается от первого тела ко второму. Если передачи теплоты между телами не происходит, то их температуры одинаковы (t1 = t2).
Температура, являясь мерой нагретости тела, представляет собой меру средней кинетической энергии движения составляющих тело атомов и молекул, т.е. температура характеризует среднюю интенсивность движения молекул; и чем больше кинетическая энергия движения молекул, тем выше температура тела.
При повышении температуры не только возрастает кинетическая энергия движения молекул, но меняется и сам характер движения молекул. Это вызывает изменение и самого состояния тела.
Рассмотрим это на примере последовательного изменения агрегатного состояния вещества при увеличении его температуры.
При очень низких температурах все вещества находятся в твердом состоянии. Их молекулы (атомы) располагаются в узлах кристаллической решетки и удерживаются в этих положениях силами молекулярного взаимодействия (притяжения). На рис.1 изображена наиболее простая (кубическая) кристаллическая решетка. Молекулы обозначены точками, а силы молекулярного притяжения - условно в виде пружинок.
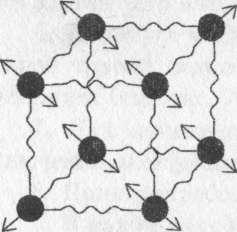
Рис.1. Кристаллическая (кубическая) решетка вещества
Молекулы не являются неподвижными - они колеблются около состояний равновесия. С увеличением температуры вещества возрастают кинетическая энергия и амплитуда колебаний этого колебательного движения. В твердых телах температура является мерой кинетической энергии колебательного движения молекул. С увеличением температуры кинетическая энергия и амплитуда колебательного движения возрастают, и при некоторой температуре они достигают такой величины, что вещество плавится - переходит из твердого состояния в жидкое. Температура этого перехода называется температурой плавления tпл.
В жидкостном состоянии вещества его молекулы по-прежнему образуют кристаллическую структуру и находятся в узлах кристаллической решетки. Но здесь уже рвутся молекулярные связи (пружинки) на границе больших конгломератов (кусков) молекул, которые получают возможность двигаться (скользить) относительно друг друга - жидкость течет.
При увеличении температуры жидкости от tпл и выше еще больше возрастают кинетическая энергия и амплитуда колебательного движения молекул относительно состояния равновесия (узлов) в кристаллической решетке. В жидкостях (как и в твердых телах) температура является мерой кинетической энергии колебательного движения молекул.
С увеличением температуры энергия колебательного движения еще больше возрастает и достигает такой величины, когда кинетическая энергия колебательного движения превышает потенциальную энергию притяжения молекул и кристаллическая решетка разрушается. Пружинки (см. рис. 1) рвутся, и молекулы отправляются в свободный полет. Вещество при этом переходит из состояния жидкости в пар, а температура этого фазового перехода называется температурой кипения tкип.
В парообразном состоянии вещества его молекулы находятся в состоянии беспорядочного теплового движения. Мерой интенсивности этого теплового движения является кинетическая энергия свободного поступательного движения молекул. Между средней кинетической энергией поступательного движения молекулы mV2/2 и температурой пара (газа) выполняется простое соотношение
mV2/2= 3/2 kT, (1)
где Т - абсолютная температура;
m - масса молекулы;
V - средняя скорость поступательного теплового движения молекул;
k - постоянная Больцмана.
Из этого соотношения следует, что при увеличении температуры пара (газа) линейно возрастает и кинетическая энергия поступательного движения молекул.
Таким образом, независимо от вида агрегатного состояния вещества, температура является мерой кинетической энергии движения его молекул. Отсюда становится ясным и то, почему при тепловом контакте теплота передается от нагретого тела к холодному: если два тела с различными средними кинетическими энергиями движения молекул привести в соприкосновение, то тело с большей средней кинетической энергией молекул (с большей температурой) будет отдавать кинетическую энергию движения молекул (теплоту) телу с меньшей средней кинетической энергией молекул (с меньшей температурой) в результате взаимодействия молекул соприкасающихся тел.
