
Modul_No2_ZanjatieNo1_Spirty.Aminy
.pdf
CH2 OH |
|
|
|
H2 SO 4, t |
CH2 OH |
|||
+ |
HO |
|
N O2 |
|
||||
|
|
|
|
|
|
|||
|
|
-H2 O |
|
|
||||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N O2 |
||
Бензиловый спирт n-Нитрофенилметанол
Многоатомные спирты
Многоатомные спирты можно рассматривать как производные углеводородов, в которых несколько атомов водорода замещены на группы ОН.
Двухатомные спирты, называются диолами или гликолями, трехатомные
– триолы или глицерины.
Названия многоатомных спиртов образуются по общим правилам номенклатуры ИЮПАК. Представителями многоатомных спиртов являются:
|
CH2 - OH |
CH2 - OH |
||||
|
|
|
|
|
||
|
CH - OH |
|||||
|
||||||
|
|
|
|
|
|
|
CH2 - OH этандиол-1,2 |
|
|
CH2 - OH пропантриол-1,2,3 |
|||
|
|
|||||
|
Этиленгликоль |
|
|
|
глицерин |
|
Физические свойства спиртов.
Многоатомные спирты – это вязкие жидкости, сладкого вкуса, хорошо растворимые в воде и этаноле, плохо – в других органических растворителях. Этиленгликоль сильный яд.
Химические свойства спиртов.
Для многоатомных спиртов характерны реакции одноатомных спиртов и они могут протекать с участием одной или нескольких групп –ОН.
1. Взаимодействие с активными металлами:
2 |
CH2 |
- OH |
+ 2 Na |
|
2 |
CH2 |
- ONa |
+ H2 |
||
|
CH2 - OH |
|
|
CH2 - ONa |
||||||
|
|
|
|
|
|
|
||||
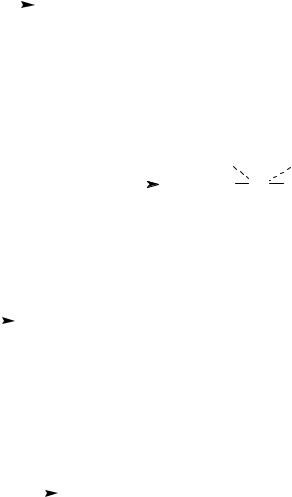
2. Взаимодействие со щелочами. Введение в молекулу дополнительных групп ОН, являющихся электроноакцепторами, усиливает кислотные свойства спиртов, так как происходит делокализация электронной плотности.
CH |
2 |
- OH |
+ 2 NaOH |
|
CH2 |
- ONa |
2HO |
||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|||
CH2 - OH |
|
|
CH2 - ONa |
2 |
|||||
|
|
|
|||||||
3. Взаимодействие с гидроксидами тяжелых металлов
(гидроксидом меди) – качественная реакция на многоатомные спирты.
|
CH |
|
|
OH |
|
|
|
HO |
|
CH |
|
CH |
|
|
OH |
HO |
|
CH |
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
2 |
|
OH + HO-Cu-OH + |
HO |
|
|
2 |
|
|
|
2 |
.. |
.. |
|
|
2 |
||||||||||
|
|
CH |
|
|
|
|
CH |
|
|
|
CH |
|
|
|
O Cu |
O |
|
|
|
CH |
|||||||
|
|
|
|
|
|
- 2H2O |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
CH2 |
|
|
OH |
|
|
|
HO |
|
CH2 |
|
CH2 |
|
|
OH |
|
CH2 |
||||||||||
4. Взаимодействие с галогеноводородами: |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
CH2 |
- OH |
+ 2HBr |
|
|
CH2 - Br |
+ 2H2O |
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
CH2 - OH |
|
|
|
CH2 - Br |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
5. Взаимодействие с кислотами с образованием сложных эфиров:
а) с минеральными кислотами
CH2 |
- OH |
|
|
CH2 - O-NO2 |
+ 3H2O |
|||
|
|
|
+ 3HO - NO2 |
|
|
|
|
|
|
|
|
|
CH - O - NO2 |
||||
|
|
|
|
|||||
CH - OH |
|
|
||||||
|
CH |
2 |
- OH |
|
|
|
CH2 - O - NO2 |
нитроглицери |
|
|
|
||||||
|
|
|
|
|
|
|
||
н
Нитроглицерин – бесцветная маслянистая жидкость. В виде разбавленных спиртовых растворов (1%) применяется при стенокардии, т.к. оказывает сосудорасширяющее действие.
При взаимодействии глицерина с фосфорной кислотой образуется смесь α- и β-глицерофосфатов:

|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|||
CH2OH |
|
CH2 |
|
O |
|
|
|
|
|
CH2OH |
|
O |
|||||||||
|
|
|
P |
|
OH |
|
|||||||||||||||
|
|
||||||||||||||||||||
|
|
|
|
||||||||||||||||||
|
|
H3PO4 |
|
|
|
|
|
+ CH |
|
O |
|
|
|
|
|
OH |
|||||
CHOH |
|
CHOH |
|
OH |
|
|
|
P |
|
||||||||||||
|
|||||||||||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
-H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
CH2OH |
|
|
|
|
|
CH2OH |
|
OH |
|||||||||||
|
|
a - глицерофосфат |
в - глицерофосфат |
||||||||||||||||||
Глицерофосфаты – структурные элементы фосфолипидов, применяются как общеукрепляющее средство
б) с органическими кислотами. При взаимодействии глицерина с высшими карбоновыми кислотами образуются жиры:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
CH2 - OH |
|
|
|
|
|
|
|
|
CH2 |
- O - C - C17H35 |
|
|||||||||||||
|
|
|
|
|
|
+ 3 C17H35COOH |
|
|
|
|
|
|
|
|
|
|
|
O |
+ 3H2O |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CH - OH |
|
|
|
|
|
|
|
|
|
|
|
CH - O - C - C17H35 |
||||||||||||
|
CH2 - OH |
|
|
|
|
|
|
|
|
|
|
|
CH2 - O - C -C17H35 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
6. Реакции дегидратации |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
CH2 |
|
OH |
HO |
|
|
|
CH2 |
H+, t |
|
|
CH2 |
|
|
O |
|
|
CH2 |
|
||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
+ |
|
|
|
|
|
|
|||||||||||||
|
|
CH2 |
|
OH |
HO |
|
|
|
CH2 |
- 2H2O |
|
CH2 |
|
|
O |
|
|
CH2 |
|
|||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
диоксан (циклический диэфир)
1. При нагревании глицерин разлагается с образованием слезоточивого вещества – акролеина:
H C |
|
|
|
|
|
OH |
|
|
|
|
|
CH2 |
|
|
|
CH |
|||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
2 |
|
|
|
|
|
|
|
KHSO4, t |
|
|
|
|
|
|
|
|
|
|
2 |
||||||
CH |
|
|
OH |
|
|
H2O |
|
C |
|
|
|
|
|
|
|
CH |
|||||||||
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
-2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
OH |
|
|
|
C |
|
O |
|||||||
CH |
|
|
OH |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|||||||||
H |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Акролеин
2.Окисление:

При окислении глицерина образуется ряд продуктов. При мягком окислении – глицериновый альдегид (1) и дигидроксиацетон (2):
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
H2C |
|
|
OH |
|||
H |
C |
|
|
OH |
|
|
|
|
|
C |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||
2 |
|
|
|
|
|
OH + 2 O |
|
|
|
|
|
|
H |
+ |
C |
|
|
|
O |
||
2 HC |
|
|
|
|
|
|
|
|
|
HC |
OH |
|
|
|
|||||||
|
|
|
|
-2 |
H |
O |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
H |
C |
|
|
OH |
H2C OH |
|
H2C |
|
|
|
OH |
||||||||||
|
|
|
|
2 |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
При окислении в жестких условиях образуется 1,3-диоксоацетон (3):
|
|
|
|
|
|
|
|
|
OH |
|
|
|
O |
|
|
|
|
|
|
|
HC |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
C |
||
|
|
|
|
|
|
|
|
|
|
|
|||
H2C |
|
OH |
|
|
|
|
|
|
H |
||||
|
|
|
|
OH |
|
|
|
||||||
2 HC |
|
|
OH + 2 CuO |
|
C |
OH |
|
|
C O |
||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
-3 Cu |
|
-3 |
H2O |
|
H |
||
|
|
|
|
|
|
|
|
||||||
H2C |
|
OH |
OH |
|
|||||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
HC |
|
|
|
|||
|
|
|
|
|
|
|
OH |
|
|
|
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
3 |
||
|
|
|
|
|
|
|
|
|
|
|
|
||
.
Биологически значимыми являются пяти- и шестиатомные спирты.
Накопление –ОН групп ведет к появлению сладкого вкуса. Ксилит и сорбит – заменители сахара для больных диабетом
Инозиты – шестиатомные спирты циклогексанового ряда. В связи с наличием ассиметрических атомов углерода у инозита существует несколько стереоизомеров; наиболее важен мезоинозит (миоинозит)
HO
HO
OH
|
OH |
|
OH |
OH |
||
|
|
|||||
|
|
H |
|
|
|
OH |
|
|
|
|
H |
H |
|
|
OH |
|
OH |
|
H |
|
|
OH |
|
|
|
H |
|
|
|
|
|
|
||
|
|
H |
OH мезоинозит |
|||
|
OH |
инозит |
|
|
||
Мезоинозит относится к витаминоподобным соединениям (витамины группы В) и является структурным компонентом сложных липидов. В растениях широко распространена фитиновая кислота, представляющая собой

гексафосфат мезоинозита. Её кальциевая соль, называемая фитином, стимулирует кроветворение, улучшает нервную деятельность при заболеваниях, связанных с недостатком фосфора в организме.
Фенолы
Фенолы – это производные ароматических углеводородов, в которых один или несколько атомов водорода замещены на гидроксильные группы.
1.Классификация фенолов.
Взависимости от числа групп ОН фенолы делятся на: одноатомные и
OH
двухатомные фенолы:
OH |
OH |
|
OH |
|||
|
||||||
|
OH |
|
|
|||
|
|
OH |
|
|
||
|
|
OH |
||||
|
|
|||||
|
|
|
||||
|
|
|
|
|||
Пирокатех |
Резорцин, |
Гидрохинон, |
||||
ин, |
||||||
|
|
|
|
|||
1,2- |
1,3- |
1,4- |
||||
Дигидрокси- |
Дигидрокси- |
|||||
Дигидрокси- |
||||||
|
|
|
|
|||
бензол |
бензол |
бензол |
||||
|
|
|
|
|||
трехзамещенные фенолы: (пирогаллол), симметричный и несимметричный
|
OH |
OH |
|
OH |
|
OH |
|
. |
OH |
OH |
|
OH |
|||
|
|
||
OH |
|
OH |
Номенклатура и изомерия.
Названия фенолов составляют с учетом того, что для родоначальной структуры по правилам ИЮПАК сохранено тривиальное название «фенол». Нумерацию атомов углерода бензольного кольца начинают от атома, непосредственно связанного с группой ОН и продолжают в такой последовательности, чтобы имеющиеся заместители получили наименьшие номера.
Строение фенола, взаимное влияние бензольного кольца и гидроксильной группы.
В молекуле фенола бензольное кольцо и группа ОН взаимно влияют друг на друга. Неподеленная пара электронов атома кислорода группы ОН находится в р, π-сопряжение с бензольным кольцом. Поэтому в феноле группа ОН, помимо отрицательного индуктивного эффекта проявляет положительный мезомерный эффект. Величина +М-эффекта больше, чем –I-эффекта. Поэтому группа ОН является электронодонором (Э.Д) по отношению к бензольному кольцу и повышает полярность связи О – Н и, следовательно происходит увеличение подвижности атома водорода и тем самым усиливаются кислотные свойства.
Кроме того, +М-эффект группы ОН повышает электронную плотность в орто-и пара-положениях бензольного кольца и в положениях 2, 4, 6 возникает частичный отрицательный заряд что облегчает реакции электрофильного замещения.
Кислотный центр

O Hδ+
δ− δ− 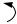
δ− |
–I< +М, ЭД |
Физические свойства.
Фенол – это бесцветное кристаллическоевещество с резким запахом, плохо растворим в воде при обычной температуре, а при температуре выше 660 смешивается с водой в любых соотношениях. На воздухе окисляется и становится розовым. Фенол – токсичное вещество, вызывает ожоги кожи, его 10% водный раствор называется карболовой кислотой и применяется как антисептик.
Химические свойства.
Химические свойства фенолов обусловлены наличием группы ОН и бензольного кольца.
|
|
|
Реакции с участием гидроксильной группы. |
||||||||||
1. |
Диссоциация в водных растворах: |
||||||||||||
|
OH |
O- |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
+ H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
фенолят - ион |
2. Взаимодействие с активными металлами (сходство с |
|||||||||||||
простыми спиртами): |
|
|
|
|
|
||||||||
|
|
OH |
|
|
|
ONa |
|||||||
|
|
|
2 |
|
+ H2 |
||||||||
2 |
|
|
|
+ 2 Na |
|
|
|
||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|||||||||
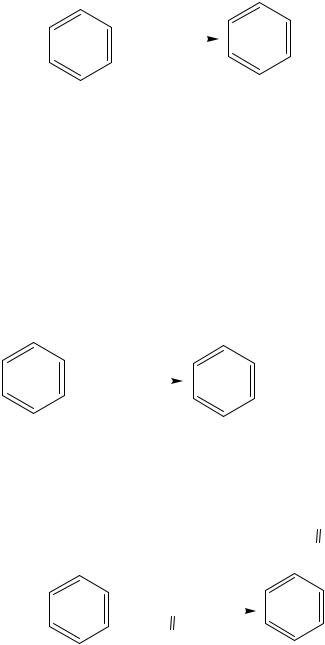
3. Взаимодействие со щелочами (отличие от спиртов):
OH |
|
ONa |
||
|
+ NaOH |
|
|
+ H2O |
|
|
|
||
|
|
|
||
|
||||
Образующиеся феноляты легко разлагаются при действии кислот. Поэтому при действии Н2СО3 (СО2 + Н2О) и др. кислот феноляты легко разлагаются и обратная реакция не возможна.
С6Н5ОNа + СО2 + Н2О → С6Н5ОН + NаНСО3
|
4. Взаимодействие |
|
с галогеналканами с образованием |
||
простых эфиров: |
|
|
|||
|
OH |
O - CH3 |
|||
|
+ H3C-Br |
|
|
|
+ HBr |
|
|
|
|
||
|
|||||
|
|
|
|
|
метилфениловый эфир |
5. Взаимодействие с ангидридами кислот с образованием сложных эфиров:
|
|
|
|
|
|
O |
|
OH |
O - C - CH3 |
||||
|
|
+ H3C- C - Cl |
H+, t |
|
|
+ HCl |
|
|
|
|
|||
|
|
|||||
|
|
O |
|
фенилацетат |
||
6. |
Взаимодействие с солями (хлоридом железа III). Данная реакция |
|||||
является качественной реакцией на фенольный гидроксид Каждый фенол дает свое характерное окрашивание в качественной
реакции с FеС13: |
|
Фенол → Фиолетовое, |
Гидрохинон → Грязно-зеленое, |
Пирокатехин → Зеленое, |
Пирогаллол → Красное. |
Резорцин → Фиолетовое |
|
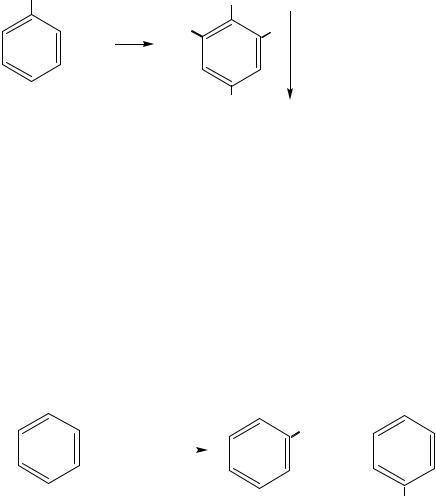
3С6Н5ОН + FеС13 → (С6Н5О)3Fе↓ + 3НС1
Фиолетовое окрашивание
7. Р-ция восстановления с цинковой пылью при нагревании:
+ Zn, t
С6Н5ОН + 3Н2 → С6Н12 + ZnО
1.1. .Р-ции по бензольному кольцу (SЕ )
Как было сказано выше, –ОН группа – ориентант I рода, облегчает реакции по бензольному кольцу, направляя атаку электрофильного реагента преимущественно в орто- и параположения:
1.Галогенирование фенола:
OH |
OH |
Br |
Br |
+ 3Br2 |
|
+ 3HBr
Br 2,4,6-трибромфенол
Происходит обесцвечивание бромной воды и образование белого осадка. Эта реакция используется как качественная реакция на фенол.
2. Нитрование фенола. Под действием 20% раствора азотной кислоты на холожу фенол превращается в смесь орто- и пара- нитрофенол:
|
|
OH |
|
OH |
OH |
||
2 |
|
2 HO-NO2 |
|
|
NO2 |
|
+ 2H2O |
|
|
|
|
||||
|
|
|
|
||||
|
|
+ |
|
||||
|
|||||||
NO2
2-нитрофенол – 40% |
4-нитрофенол – |
10%
Для получения 2,4,6-тринитрофенола (пикриновой кислоты) фенол предварительно растворяют в концентрированной серной кислоте, а зате6м подвергают нитрованию концентрированной азотной кислотой:
OH |
|
OH |
|
|||||
|
+ 3 HO-NO2 |
H2SO4 |
O2N |
|
|
|
NO2 |
|
|
||||||||
|
|
|
||||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
+ 3H O |
||
|
|
|
|
|
|
|
|
2 |
|
|
|
|
пикриновая |
||||
|
|
|
|
|
NO2 |
|||
|
|
|
|
|||||
кислота
3.Сульфирование фенола:
|
OH |
|
OH |
OH |
|||
2 |
|
+ 2 HO-SO3H |
|
|
SO3H |
|
|
|
|
|
|
|
|||
|
|
+ |
|
+ 2H2O |
|||
|
|
|
|||||
SO3H
4. Р-ция конденсации. При взаимодействии с формальдегидом фенол образует полимеры различного строения (линейного, разветвленного, сетчатого) – фенолформальдегидные смолы.
OH |
OH |
OH |
OH |
H |
O H |
|
CH2 |
+ |
CH2 + |
|
|
-H2O |
и т.д. |
Фрагмент
фенолоформальдегидной
смолы
5.Р-ция гидрирования (восстановление):
