
ред.Рыбкиной - Простое вещество (2000)
.pdfМинистерство образования Российской Федерации
Российский химико-технологический университет им. Д.И. Менделеева
Новомосковский институт
ПРОСТОЕ ВЕЩЕСТВО
Методические указания
Под редакцией кандидата химических наук
Т.И. Рыбкиной
Новомосковск 2000
УДК 546
ББК 24.1 П431
Рецензент:
кандидат химических наук, доцент НИ РХТУ им. Д.И. Менделеева Н.Ф. Кизим
Составитель: Э.А. Кириченко
П431 Простое вещество: Методические указания /Под ред. канд. хим. наук Т.И. Рыбкиной; РХТУ им. Д.И. Менделеева, Новомос- ковский ин-т; сост. Э.А. Кириченко. Новомосковск. 2000, 48 с.
Методические указания «Простое вещество» посвящены соедине- ниям, образованным атомами одного элемента. Эти соединения по- лучили название «гомоатомные соединения» или «простые вещест- ва». В данной теме уделено внимание методам получения таких веществ, их очистке, формам существования (аллотропия, поли- морфизм). Особенно большое внимание уделено с нашей точки зрения наиважнейшему вопросу: внутреннему (кристаллохимиче- скому) строению простых веществ и тому, как это строение связано с проявляемыми физическими свойствами гомоатомных соедине- ний. Проявление химических свойств простых веществ в пособии дано в самой общей форме, т.к. эти свойства будут рассмотрены в одной из последующих лекций.
Для студентов технологических специальностей.
Ил. 29. Табл. 4. Библиогр.: 9 назв.
УДК 546
ББК 24.1
© Новомосковский институт Российского химико-технологического университета им. Д.И. Менделеева, 2000
3
ВВЕДЕНИЕ
Простое вещество – это соединение, состоящее из атомов одного элемента. Иногда эти вещества называют гомоатомными соединениями, в отличие от тех соединений, которые образованы атомами различных эле- ментов, и которые называют гетероатомными.
Изучение свойств простых веществ имеет фундаментальное значе- ние в неорганической химии. Оно является первым этапом в описательной химии элементов.
Последовательное и аналитическое изучение фактического мате- риала о свойствах простых веществ (химических, физических, физико- химических) позволяет составить общее представление о химическом эле- менте, представить природу химической связи, состав и свойства его харак- теристических соединений, их кислотно-основные и окислительно- восстановительные характеристики и т.п.
При рассмотрении простых веществ нет проблем с определением состава, т.к. состав, естественно, одинаков на всем протяжении вещества.
Однако, представлять себе простые вещества как совокупность ав- тономно существующих атомов данного элемента, будет глубоким заблуж- дением.
1.Атомы простых веществ химически связаны между собой, они образу- ют молекулы и кристаллы. Связь между атомами специфична для каж- дого элемента. Простым веществам присущи явления аллотропии и по- лиморфизма.
2.Другим важным фактором, который должен учитываться, является чис- тота вещества, т.к. даже незначительные примеси существенно влияют на свойства простых веществ.
На Земле простые вещества в чистом виде встречаются довольно редко – самородное золото, редкие скопления ртути, графит и некоторые другие. Обычно же простые вещества встречаются или в трудно разделяе- мых смесях: мелкие крупинки золота, платина, серебро в породе; кислород, азот, аргон в газовой смеси, каковым является воздух; крупинки серы впе- ремешку с песком и т.д.
Но чаще элементы существуют на Земле в виде химических соеди- нений с другими элементами, поэтому чтобы получить простое вещество соответствующего элемента приходится прибегать подчас к непростым фи-
зическим или химическим методам извлечения этого вещества из смесей или соединений.
4
§1. ОСНОВНЫЕ ПРИНЦИПЫ И СПОСОБЫ ПОЛУЧЕНИЯ ПРОСТЫХ ВЕЩЕСТВ
Принципы получения простых веществ сводятся к тому, чтобы вы- делить интересующее нас вещество, если оно находится в смеси. Если же элемент находится в составе химического соединения, - то перевести эле- мент из ионного состояния в атомарное, для чего используются различные методы, в основе которых лежат окислительно-восстановительные процес- сы, и атомы нужного нам вещества отделить от других. В табл. 1.1 приведе- ны основные способы получения простых веществ.
Вот несколько примеров.
Простые вещества кислород, азот, аргон, неон и др. получают раз- делением их смеси – воздуха. Воздух охлаждается до сжижения, а затем эта смесь жидкостей разделяется на ректификационных колоннах, за счет раз- ницы температур кипения веществ, составляющих эту смесь:
|
Ne |
N2 |
Ar |
O2 |
Tкип., К |
27,3 |
77,4 |
87,5 |
89,5 |
Золото или платину отделяют от песка или измельченной породы, содержащей эти металлы, промыванием водой. Грамотно подобранная ско- рость движения воды смывает породу, но оставляет золото и платину. При этом используется разница в плотности породы (около 5 г/см3) и металлов
(Au – 19,3; Pt – 21,45 г/см3).
Сера, которая иногда находится в мелко раздробленном виде в пес- ке, извлекается оттуда нагреванием в автоклавах с подогревом, или под землей с помощью перегретого пара (метод Фарша). Она стекает из авто- клава или выдавливается из-под земли воздухом под давлением. Раньше в емкости загружали смесь песка с серой и поджигали. Часть серы сгорала и за счет этого тепла плавилась другая часть серы, и стекала из емкости в под- готовленную тару. Конечно, это варварство, но это было.
Все перечисленные способы – чисто физические и служат только отделению одного простого вещества от других простых или сложных ве- ществ, не связанных с ним химической связью, т.е. пригодны только для разделения смесей.
Иначе обстоит дело, когда элемент входит в состав химического соединения. Атомы элемента находятся в окисленном (положительная сте- пень окисления) или в восстановленном (отрицательная степень окисления) состоянии.
Отсюда два принципиально разных подхода. В одном случае эле- мент необходимо восстановить, а в другом – окислить до нейтральных ато- мов, а затем отделить их от атомов других элементов.

5
|
|
Таблица 1. 1 |
|
Основные способы получения простых веществ |
|||
|
|
|
|
Метод |
Исходная форма |
Получаемые вещества |
|
|
Физические методы |
||
1. Разделение сме- |
Самородные простые |
S, Au, Pt, Hg, Ag, |
|
сей |
вещества |
платиновые металлы |
|
2. Фракционная |
Воздух (жидкий) |
O2, N2, благородные газы |
|
перегонка |
|||
|
|
||
|
Химические методы |
||
1. Восстановление |
Оксиды, галогениды, |
|
|
а) водородное |
Ga, In, Si, Ge, Mo, W, Re, B |
||
соли |
|||
|
Fe, Co, Ni, Cr, Mn, Si, Pb, Sn, |
||
б) карботермия |
Оксиды, соли |
||
Zn, Cd, Cu, P, As, Sb, Bi, Mo, W |
|||
|
|
||
в) алюмотермия |
Оксиды |
Cr, Fe, Co, Ni, Mn, |
|
щелочноземельные металлы |
|||
|
|
||
цинктермия |
ü |
Si, Ag, Au |
|
магнийтермия |
÷ |
Be, Tl, Zr, Hf, Si, B |
|
кальцийтермия |
ý Оксиды, галогениды |
U, V, Nb, Ta, Sc, Y, La, |
|
÷ |
лантаноиды |
||
|
|||
натрийтермия |
þ |
Nb, Ta, Ti, Zr, Hf |
|
г) на катоде элек- |
Галогениды, соли, |
Щелочные и щелочноземель- |
|
ные металлы, Al, Ga, In, Tl, Be, |
|||
тролизера |
вода |
||
Mg, Zn, Pb, Nb, Cu, H2 |
|||
|
|
||
2. Окисление |
|
|
|
а) вытеснение Cl2 |
Бромиды, иодиды |
Br2, I2 |
|
б) на аноде элек- |
Расплавы фторидов, |
|
|
растворы, расплавы |
F2, Cl2, O2 |
||
тролизера |
|||
хлоридов, вода |
|
||
|
|
||
3. Разложение и |
Галогениды, |
Si, Ge, Ti, Zr, Hf, Mo, W, V, Nb, |
|
диспропорциони- |
|||
карбонилы |
Ta, Al, B, Fe, Co, Ni, Mn |
||
рование |
|||
|
|
||
Металлы в природе находятся, как правило, в окисленном состоя- нии. Восстановление их проводится разными методами и различными вос- становителями, выбор которых – серьезная технологическая задача. Вот несколько примеров.
Природный сульфид ртути (киноварь – HgS) достаточно нагреть, и за счет внутримолекулярного окислительно-восстановительного процесса восстанавливается ртуть:

6
+2 |
-2 |
t 0 |
0 |
HgS = Hg + S |
|||
|
- |
|
|
|
2e |
|
|
Сульфидные руды Zn, Cu, Pb, Co, Ni и других металлов сначала |
|||
обжигают: |
|
t |
|
|
|
|
|
2CuS + 3O2 |
= 2CuO + 2SO2 |
||
затем восстанавливаютCO, углеродом, водородом или другими восстанови- |
|||
телями: |
|
|
|
+2 |
0 |
t |
0 +4 |
2 Cu O + C = 2 Cu+ C O2
Такие металлы, как Ti, V, Cr и некоторые другие, получают восста- новлением активными металлами:
+4 |
0 t 0 +2 |
Ti O2 |
+ 2 Mg = Ti+ 2 Mg O |
Эта реакция лежит в основе процесса получения титана на титано- магниевых комбинатах.
Самые активные металлы, такие как Li, Na, K, Rb, Cs, Ba и некото- рые другие, можно получить только путем электролиза расплавов их солей.
Алюминий получают тоже электролизом, причем исходный про- дукт – глинозем (Al2O3) – предварительно растворяют в расплаве криолита (3NaF×AlF3), и этот раствор подвергают электролизу при напряжении 4,0 – 4,5 В и силе тока до 150 тыс. А, при t = 2000 °С. Не расплавление глинозема,
а его растворение в криолите обусловлено необходимостью экономить
энергию: tпл.(криолита) » 1000 °С, а tпл.(Al2O3) = 2050 °С.
Существует немало способов получения особо чистых металлов, например, разложением карбонилов:
t
Fe(CO)5 = Fe + 5CO
Полученные восстановлением так называемые черновые металлы, часто рафинируют – очищают от других металлов и иных примесей. Черно- вую медь рафинируют путем электролиза с растворимым анодом из черно- вой меди. Рафинированием чистоту меди доводят от 98,5-99,0% до 99,5- 99,9%.
Свинец от цинка очищают дистилляцией. Температуры плавления
Zn и Pb близки: tпл.(Zn) = 419,5 °С, tпл.(Pb) = 327,4 °С, а температуры кипе-
ния существенно разнятся: tкип.(Zn) = 907 °С, а tкип.(Pb) = 1740 °С. Цинк уле- тучивается в виде паров.
Человек получает много разных металлов. Отрасль промышленно- сти, призванная производить металлы, называется «металлургия». Эта от- расль промышленности подразделяется по металлам – на черную и цветную металлургии, а по способам получения металлов – пирометаллургию (высо-
7
кая температура), электрометаллургию (электропроцессы), гидрометаллур- гию (используются различные экстрагенты, например, производство урана) и т.д.
Неметаллы встречаются в природе и в окисленном, и в восстанов- ленном виде, в зависимости от их активности. Сравнительно малоактивные неметаллы, которые находятся в природе в окисленном состоянии (бор, кремний, фосфор, мышьяк, сурьма), выделяют в виде простых веществ дей- ствием соответствующих восстановителей. Так бор и кремний восстанавли- вают магнийтермически из оксидов; водородом – из хлоридов BCl3 и SiCl4, а кремний еще и цинком из SiCl4.
t
B2O3 + 3Mg = 3MgO + 2B
1900 °
2BCl3 + 3H2 |
= 2B + 6HCl |
|
t |
SiO2 + 2Mg = Si + 2MgO |
|
|
t |
SiCl4 + 2H2 |
= Si + 4HCl |
|
t |
SiCl4 + 2Zn = Si + 2ZnCl2 |
|
Пниктогены (кроме азота и фосфора) получают карботермическим восстановлением оксидов Э2О3, а фосфор – карботермическим восстановле- нием фосфорита Ca3(PO4)2.
t
As2O3 + 3C = 2As + 3CO
+5 0 +2 0
2Ca3 (P O4 )2(к) +10 C(к) + 6SiO2(т) = 10 C O(г) + P4(г) + CaSiO3
SiO2 добавляется как флюс для связывания кальция.
Наиболее активные неметаллы – галогены находятся в природе только в восстановленном виде (Г-), поэтому их можно выделить из при- родных соединений только окислением. Бром и иод можно извлечь из рас- творов бромидов и иодидов, окислив более энергичным окислителем – хло- ром. Чаще всего источник иодидов и бромидов – зола водорослей (морская капуста).
2NaBr + Cl2 → 2NaCl + Br2
Хлор и фтор получают электролизом, причем в случае хлора ис- пользуют растворы и расплавы хлоридов, а в случае фтора – только распла- вы фторидов, поскольку свободный фтор активно реагирует с водой с выде- лением ряда побочных продуктов.
Водород в промышленности получают: а) главным образом из при- родного метана. При нагревании в присутствии катализатора смеси природ- ного газа, водяного пара и воздуха происходят реакции:
t, cat
CH4 + H2O = CO + 3H2
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
t, cat |
|
|
|
|
|
|
|
2CH4 + O2 |
= |
2CO + 4H2 |
|
|
|
||
Это реакции пароводяной и кислородной конверсии метана. Далее идет |
|||||||||
процесс окисления водяным паром окиси углерода (конверсия оксида угле- |
|||||||||
рода (II)): |
|
|
|
|
|
|
|
|
|
|
|
|
|
t, cat |
|
|
|
|
|
|
|
CO + H2O = CO2 + H2 |
|
|
|
||||
б) железо-паровым способом: |
|
|
|
|
|
|
|
||
|
+1 |
0 |
|
+2 |
+3 |
|
|
|
|
|
4 H2 O + 3Fe |
= Fe O |
×Fe2 O3 + 4H2 - |
|
|
|
|||
в) в странах с дешевой электроэнергией и недостатком природного газа, |
|||||||||
например, в Швеции, водород получают методом электролиза воды: |
|
||||||||
|
|
2H2O ® 2H2 + O2 |
|
|
|
||||
|
|
|
|
катод |
анод |
|
|
|
|
используется этот метод и у нас в стране в регионах, где есть избыток элек- |
|||||||||
троэнергии (Сибирь). |
|
|
|
|
|
|
|
|
|
|
§2. ОСОБО ЧИСТЫЕ ВЕЩЕСТВА |
|
|
||||||
|
Понятие о чистоте вещества имеет принципиальное значение в со- |
||||||||
временной химии. Абсолютно чистые вещества в природе не существуют, |
|||||||||
поскольку загрязнение примесями (образование ограниченных растворов) |
|||||||||
происходит самопроизвольно, о чем свидетельствует ход изменения энтро- |
|||||||||
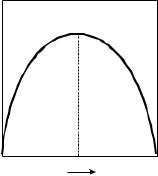
пии (рис. 2.1). Поэтому нет абсолютно нерастворимых веществ, и, следова- |
|||||||||
тельно, любое вещество загрязнено примесями, даже в тех случаях, когда |
|||||||||
вещество очищено до очень высокой степени. |
|
|
|
||||||
Sсм. |
|
|
|
|
|
Вероятность |
загрязнения |
и |
|
|
|
|
|
|
трудности очистки |
возрастают |
|||
|
|
|
|
|
|
по мере приближения к полной |
|||
|
|
|
|
|
|
очищенности данного вещества |
|||
|
|
|
|
|
|
от примесей (см. ход кривой |
|||
|
|
|
|
|
|
изменения энтропии при при- |
|||
|
|
|
|
|
|
ближении к веществу А или В |
|||
|
|
|
|
|
|
(рис. 2.1)). Абсолютное число |
|||
|
|
|
|
|
|
атомов примеси в единице мас- |
|||
|
|
|
|
|
|
сы или объема вещества даже |
|||
A |
0,5 |
|
|
B |
|
очень высокой очистки огромно. |
|||
|
|
|
Так, |
в |
германии |
||||
|
XB |
|
|
|
|
полупроводниковой |
чистоты |
||
Рис. 2.1. Изменение энтропии сме- |
|
99,9999999% |
Ge, |
содержание |
|||||
|
атомов примесей не превышает |
||||||||
шения в зависимости от состава. |
|
||||||||
|
10-7 ат. доли %, т.е. один атом |
||||||||
9
примеси приходится на 1 млрд. атомов Ge. Тем не менее, 1 см3 этого особо чистого германия содержит около 1013 атомов примеси.
Примеси коренным образом влияют на свойства вещества. Напри- мер, хорошо известная хрупкость и исключительная твердость металличе- ского хрома, как выяснилось, являются следствием наличия в нем неболь- шого количества примесей, в основном кислорода. Хром, полученный в условиях глубокого вакуума, оказался мягким и пластичным.
Небольшие примеси воды делают хлор реакционноспособным по отношению к железу. Сухой хлор инертен по отношению к железу и его перевозят в стальных ж/д цистернах. Немало и других примеров, когда не- большие примеси существенно меняют свойства вещества.
Проблема получения чистых веществ имеет три основных аспекта. Первый из них состоит в том, что свойства вещества можно опре-
делить, только получив его в нужной степени чистоты.
Второй аспект заключается в выборе подходящих материалов, ме- тодов, позволяющих очистить вещество до необходимой степени чистоты.
И, наконец, третий аспект проблемы – обеспечение достаточно чувствительных и селективных методов контроля чистоты.
По мере развития науки и техники возникает проблема получения все более чистых веществ. До сравнительно недавнего времени использова- лись вещества, которые в настоящее время можно считать грязными. Очи- стка таких веществ обеспечивалась главным образом химическими метода- ми, контроль чистоты – химическим анализом. Такие вещества в ряде слу- чаев и сейчас используются на практике. Для них разработана градация оценки чистоты на четырех уровнях:
1)«технический» (Т);
2)«чистый» (Ч);
3)«чистый для анализа» (ЧДА);
4)«химически чистый» (ХЧ);
Так, серная кислота квалификации «Ч» содержит 1×10-2 масс. доли, % при- месей, «ЧДА» - 2×10-3 масс. доли, %, а «ХЧ» - 1×10-3 масс. доли, %.
В современных отраслях техники: ядерной энергетике, полупро- водниковом материаловедении, квантовой электронике и т.п., требуются материалы значительно более высокой степени чистоты. Такие особо чис- тые вещества можно получить только с помощью специальных физико- химических методов очистки, основанных на различном распределении примесей в сосуществующих фазах. Методы сублимации, экстракции, хро- матографии, направленной кристаллизации, зонной плавки дают возмож- ность получить вещества, которым присваивается квалификация «особо чистый» (ОСЧ). Для характеристики материалов используется не общее содержание примесей, а содержание так называемых анализируемых при- месей. При этом число анализируемых примесей достаточно велико: 10-20,
10
а иногда и более. В маркировке ОСЧ материала указывается количество анализируемых примесей и их общее содержание. Например, мышьяк мар- кировки ОСЧ-10-5 означает, что в материале определено содержание 10 примесей, а их суммарное количество 10-5 масс. доли, %, т.е. содержание основного вещества 99,99999%.
В ряде случаев нет необходимости очищать вещество от всех при- месей, достаточно удалить лишь некоторые, наиболее нежелательные для данного целевого назначения. Так, для качественного анализа на мышьяк (проба Марша) требуется цинк, не содержащий примесей мышьяка, а со- держание других примесей не регламентируется. Поэтому вводится понятие
о так называемой чистоте целевой и веществах эталонной чистоты
(ВЭЧ). В маркировке таких веществ три вида значащих цифр, например, 003ВЭЧ4-7. Первые три цифры означают общее содержание всех примесей (10-3 масс. доли, %), вторая – число анализируемых примесей (4), а третья – их содержание (10-7 масс. доли, %). В веществах эталонной чистоты в отли- чие от особо чистых веществ, количество анализируемых примесей сущест- венно меньше, поэтому их суммарное содержание не совпадает с общим содержанием примесей.
§3. ХИМИЧЕСКИЙ ЭЛЕМЕНТ И ПРОСТОЕ ВЕЩЕСТВО
Основополагающим понятием современной химии является поня- тие о химическом элементе, т.е. виде атомов с определенной совокупностью свойств. Под свойствами изолированных атомов подразумевается заряд яд- ра и атомная масса, особенности электронного строения, потенциалы иони- зации, сродство к электрону и электроотрицательность, атомные, орбиталь- ные и ионные радиусы и т.д. Однако, необходимо иметь в виду, что изоли-
рованные атомы как форма организации вещества могут существовать в природе лишь при достаточно высоких температурах в виде моноатомного пара. Единственным исключением являются благородные газы, для которых при любых условиях и в любом агрегатном состоянии структурной едини- цей является атом. Жидкое и твердое агрегатные состояния у них достига- ются за счет не валентной химической связи, а за счет сил Ван-дер-Ваальса
– дисперсионного эффекта. Все остальные элементы существуют в природе в виде более сложных агрегатов: молекул и кристаллов. Таким образом, следует строго различать понятия химического элемента как вида изолиро-
ванных атомов и простого вещества как формы существования элемента в свободном состоянии. Следует особо подчеркнуть нетождественность этих понятий хотя бы потому, что один элемент может существовать в виде не- скольких простых веществ (аллотропия).
Несмотря на очевидность различия между этими понятиями, даже в учебной и научной литературе допускают их смешение, употребляя, напри-
