
- •Министерство образования и науки Российской Федерации
- •Титриметрические методы анализа. Сущность титриметрии
- •Прямое титрование
- •Обратное титрование (титрование по остатку)
- •Метод замещения
- •Единицы количества вещества и разные способы выражения концентраций растворов. Формулы для расчетов
- •1. Метод кислотно–основного титрования
- •1.1 Расчёты в методе кислотно–основного титрования Закон эквивалентов. Эквиваленты веществ
- •1.2. Лабораторные работы. Метод кислотно-основного титрования Лабораторная работа № 1 Определение содержания щелочи в контрольном объеме раствора
- •Лабораторная работа № 2 Определение миллиграммового содержания NaOh и Na2co3 при совместном присутствии
- •Лабораторная работа № 4 Определение процентного содержания аммиака в солях аммония методом обратного титрования
- •Лабораторная работа № 5 Определение сильной и слабой кислот при совместном присутствии
- •1.3 Задачи и примеры решений
- •I Вычислить рН и рОн растворов, если:
- •III Вычислить рН и рОн растворов, если:
- •IV Вычислить рН и рОн растворов, если смешали:
- •0,1 М раствора NaOh и 19,0 мл 0,1 м
- •V Вычислить рН и рОн растворов, если смешали:
- •0,1 Н раствора нСl и 20 мл. 0,1 н. Nh4он.
- •VI Выбрать индикатор для титрования раствора (1) рабочим
- •VII Вычислить эквивалентную массу вещества (а), которое
- •VIII Расчеты, связанные с приготовлением рабочих растворов
- •IX. Вычисление результатов титриметрического анализа
- •X. Вычисление результатов титриметрического анализа
- •2. Метод редоксометрии (перманганатометрия и иодометрия)
- •2.1. Метод перманганатометрии
- •Метод перманганатометрии имеет следующие достоинства:
- •Недостатки метода:
- •Приготовление и хранение раствора kMnO4
- •Техника безопасности
- •2.2 Лабораторные работы Перманганатометрия Лабораторная работа №1
- •Лабораторная работа №2 Определение миллиграммового содержания железа (II) в солях, рудах и технических материалах
- •Лабораторная работа №3 Определение миллиграммового содержания хрома в бихромате калия методом обратного титрования
- •План работы
- •Метод иодометрии
- •Лабораторная работа №4 Установка нормальности рабочего раствора тиосульфата натрия
- •Лабораторная работа №5 Определение миллиграммового содержания меди в сульфате меди
- •2.3. Задачи и примеры решений
- •II. Оценка возможности протекания реакций
- •III. Расчет потенциалов
- •IV. Составление окислительно-восстановительных реакций
- •V. Определение молярных масс эквивалентов окислителей и восстановителей в реакциях
- •VI. Расчеты навесок и концентраций растворов
- •VII. Рассчитать область скачка титрования, окислительно-восстановительный потенциал в точке эквивалентности и подобрать индикатор при титровании
- •Пусть исходные данные
- •Потенциал исходного раствора
- •Расчет потенциала до точки эквивалентности
- •В растворе присутствуют Fe (III) и Сe (III) в эквивалентных количествах.
- •Расчет потенциала раствора до точки эквивалентности.
- •VIII. Расчеты по результатам прямого титрования
- •IX. Расчеты по результатам обратного и заместительного (косвенного) титрования
- •3. Метод комплексонометрии
- •3.1. Лабораторные работы (Метод комплексонометрии). Лабораторная работа № 1 Приготовление рабочего раствора трилона б илиNa2c10h14o8n2
- •Лабораторная работа №2 Определение общей жесткости воды
- •Лабораторная работа №3 Определение миллиграммового содержания ионов кальция и магния при совместном присутствии
- •Лабораторная работа №4 Определение миллиграммового содержания иона кобальта в неизвестном объеме
- •Лабораторная работа № 5 Определение миллиграммового содержания
- •3.2. Задачи и примеры решений. Определение результатов, комплексонометрических определений
- •3.3 Варианты домашних заданий.
- •4. Метод гравиметрии
- •4.1 Лабораторные работы (метод гравиметрии).
- •244,3 Г/моль – 98 г/моль – 1000 мл
- •4.2. Задачи и примеры решений.
- •I. Расчет навески
- •II. Расчёт осадителя
- •III. Определение факторов пересчёта
- •IV. Вычисление результатов весовых анализов
- •5. Приложения
IX. Вычисление результатов титриметрического анализа
(прямое титрование).
Сколько граммов Na2CO3содержится в растворе, если на титрование доNaHCO3идет 21,50 млHClс титром 0,002900 г/мл ?
Сколько граммов Na2CO3содержится в растворе, если на титрование доH2CO3идет 22,00 млHClс концентрацией 0,1010 моль/л?
На титрование навески NaOHмассой 0,09978 г израсходовали 22,00 млHCl. Определить титр раствораHCl по Na2O.
На титрование раствора, содержащего 3,158 г технического КОН, израсходовали 27,45 мл 0,1020н раствора НСl. Вычислить массовую долю (%) КОН в образце.
Вычислить массу К2СО3, если на титрование соли в реакции с образованием Н2СО3израсходовано 20,42 мл 0,2232М раствора НСl.
В мерной колбе на 250,0 мл приготовили раствор, содержащий КОН. На титрование 50,00 мл этого раствора затрачено 38,56 мл 0,05040М раствора H2SO4. Вычислить массу КОН.
Сколько процентов HNO3содержит концентрированная азотная кислота, если после растворения 9,7770 г её в мерной колбе на 1 л на титрование 25,00 мл 0,1040н раствораNaOHизрасходовано 25,45 мл полученного раствораHNO3.
Сколько граммов Н3РО4содержится в данном растворе, если на титрование его с фенолфталеином затрачивается 25,50 мл 0,2000н раствораNaOH?
Сколько граммов Н3РО4содержится в растворе, если при титровании его с метиловым оранжевым пошло 25,50 мл 0,2000н раствораNaOH?
Сколько граммов КОН и К2СО3содержит отдельная навеска препарата гидроксида калия, если при титровании её с фенолфталеином затратили 22,40 мл 0,09500н раствораHCl, а с метиловым оранжевым ушло 25,80 мл этой кислоты?
На титрование 25,00 мл смеси Na2CO3иNaHCO3с фенолфталеином пошло 9,46 мл, а с метиловым оранжевым – 24,86 мл 0,1200н раствораH2SO4.Сколько граммов Na2CO3 и NaHCO3 содержится в 250 мл раствора?
Сколько граммов NaOHсодержится в 200 мл раствора, если на титрование 15,00 мл этого раствора расходуется 17,00 мл 0,1500МHCl?
Навеску 0,5341 г щёлочи NaOHрастворили в мерной колбе на 100 мл. На титрование 15,00 мл этого раствора израсходовано 19,50 мл 0,1010М раствораHCl. Определить процентное содержаниеNaOHв навеске.
Навеску технического NaOHмассой 0,4000 г растворили в мерной колбе на 100 мл. На титрование 20 мл этого раствора израсходовали 19,2 мл 0,09863М раствораHCl. Определить процентное содержаниеNaOHв навеске.
Навеску технического NaOHмассой 0,3900 г растворили в мерной колбе на 100 мл. На титрование 20 мл этого раствора израсходовали 18,0 мл 0,09863М раствораHCl. Определить процентное содержаниеNaOHв навеске.
Пример: Рассчитать массовую долю (%) основного компонента
(Na2B4O7x10H2O) в загрязнённой буре, если при
титровании 0,8530 г её идёт 20,20 мл 0,2100М
раствора HCl?
Решение: Определение ведётся методом отдельных навесок. Процентное содержание чистой буры определяется по формуле:
![]()
Находим сначала массу чистой буры (mчист.) по результатам титрования:
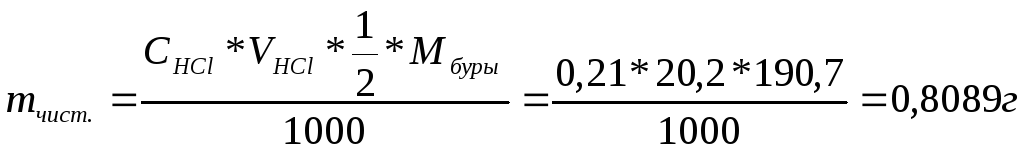
![]() Ответ:94,84 %.
Ответ:94,84 %.
X. Вычисление результатов титриметрического анализа
(метод обратного титрования)
К навеске Na2CO3массой 0,1032 г прилили 50,00 мл 0,09496М НСl, избыток кислоты оттитровали 24,80 мл 0,1298МNaOHпо метиловому оранжевому. Вычислить массовую долю (%) индиффирентных примесей в образце.
В каком объёме соляной кислоты (Т(HCl)=0,003638 г/мл) нужно растворить навеску СаСО3массой 0,1234 г, чтобы на титрование избытка кислоты с метиловым оранжевым израсходовать 19,50 мл 0,1200М раствораNaOH?
Какую навеску нашатыря, содержащего около 30% NH3, взяли для анализа, если после добавления к ней 50,00 мл 0,1000нNaOHи нагревания до полного удаления аммиака, избыток щёлочи оттитровали 25,00 мл 0,1нHCl.
К раствору (NH4)2SO4добавили 25,00 мл 0,1010М раствораNaOH. Кипячением удалили аммиак, а на титрование оставшейся щёлочи затратили 8,65 мл 0,100 раствора НСl. Вычислить массу(NH4)2SO4.
Какой объём 0,10М раствора HClнужно взять для поглощения аммиака, выделяемого из 0,50 г вещества, содержащего 5% азота, чтобы на титрование избыткаHClрасходовать 6 мл 0,10М раствораNaOH?
Для определения содержания азота навеску 0,9145 г муки обработали концентрированной серной кислотой, переведя азот в аммонийную соль. Действием щёлочи и продувкой воздухом выделили аммиак, который поглотили 20,00 мл 0,1010М раствора НСl. На титрование избытка кислоты затратили 6,30 мл 0,1200М раствораNaOH. Вычислить массовую долю азота в муке.
Через 25,00 мл раствора соляной кислоты с титром 0,006970 г/мл пропущен газ, содержащий аммиак, на тирование остатка кислоты пошло 7,25 мл раствора NaOH. Определить массу аммиака, если на 25 мл кислоты расходуется 14 млNaOH.
Какую навеску х.ч. NaNO3взяли для анализа по методу восстановленияNO3-доNH3, если выделившийся аммиак был поглощён 40,00 мл 0,1245н соляной кислоты и избыток кислоты оттитрован 22,40 мл 0,1002нNaOH?
Навеску 0,1032 г Na2CO3обработали 50,00 мл 0,09496нHCl, избыток кислоты оттитровали 29,80 мл 0,1298нNaOH. Вычислить процентное содержание индифферентных примесей в образце.
В каком объёме соляной кислоты (Т(HCl)=0,003814 г/мл) нужно растворить навеску 0,1234 г СаСО3, чтобы на титрование избытка кислоты израсходовать 19,50 мл 0,1143н раствораNaOH?
Пробу соли аммония в 1,000 г. обработали избытком концентрированного раствора NаОН. Выделившийся аммиак был поглощен 50,00 мл. 1,0720 н. HСl. Избыток кислоты был оттитрован 25,40 мл. раствора NaOH (Т( NaOH) = 0,004120 г/мл). Вычислить процентное содержание индифферентных примесей в образце.
Сколько было металлического магния, если по растворении его в 50,00 мл 0,5200 н. раствора HСl на обратное титрование остатка HСl пошло 15,00 мл.0,2000 н. раствора NаОН?
Азот из навески 0,8880 г. органического вещества перевели в NH3, который поглотили 0,1200 н. раствором Н2SO4объемом 50,0 мл. Сколько процентов азота содержит органическое вещество, если на титрование избытка Н2SO4 пошло 12,00 мл. 0,09800 н. раствора NаОН?
Сколько было граммов СаСО3, если после обработки навески его 50,0 мл. 0,2000 н. раствора НСl на титрование остатка НСl пошло 10,00 мл. раствора NаОН? Известно, что на титрование 25,00 мл. НСl идет 24,00 мл. раствора NаОН.
Для определения содержания NH3в техническом (NH4)2SO4навеску сульфата аммония (1,6160 г) растворили в мерной колбе на 250 мл. Из 25,00 мл полученного раствора выделили аммиак, который поглотили 40,00 мл 0,1020 н раствораH2SO4, а на обратное титрование оставшейся кислоты пошло 17,00 мл 0,09600 н раствораNaOH.Вычислить процентное содержание NH3 в (NH4)2SO4.
Пример: Для определения вольфрама в стали навеску 1,000 г
обработали соответствующим образом и превратили
вольфрам , находящийся в ней, в H2WO4. К этой
кислоте добавили избыток (40,00 мл) 0,005548М
раствора NaOH. На обратное титрование избытка
NaOH с фенолфталеином пошло 18,00 мл 0,005659М
раствора HNО3. Сколько процентов вольфрама
содержит сталь?
Решение:При титровании с фенолфталеином вольфрамовая кислота титруется как одноосновная до кислой соли:
H2WO4 + NaOH = NaHWO4 + H2O
ZH2WO4 = 1; Эквивалентная масса H2WO4 равна М(H2WO4).
Эквивалентная масса вольфрама равна его атомной массе (183,85 г/моль). Находим массу чистого вольфрама:
![]()
![]()
Ответ:2,21%.
