
- •2. Особенности адсорбции на поверхности твердого адсорбента. Уравнение Фрейндлиха, его анализ и определение констант уравнения.
- •3. Что понимается под поверхностным слоем, поверхностной энергией и поверхностными явлениями. Какие параметры относятся к количественным характеристикам дисперсности? Дайте их полную характеристику.
- •4. Представьте, что Вам необходимо сделать доклад по теме: “Суспензия”. Напишите план доклада и в соответствии с ним составьте тезисы доклада.
- •5. Что понимается под поверхностным натяжением и как оно зависит от природы веществ, образующих поверхность раздела фаз?
- •6. Что такое капиллярное давление? Каковы причины его возникновения? Вывод и анализ уравнения Лапласа.
- •8. Поверхностное натяжение: причины возникновения, его физический смысл с термодинамической и силовой точек зрения, определение и методы измерения.
- •9. Что такое агрегативная устойчивость? Факторы, обеспечивающие агрегативную устойчивость лиофобных золей.
- •10. Характеристика порошков как дисперсных систем. Какие порошки обладают более высокой текучестью – грубодисперсные или высокодисперсные? Какие порошки легче распылять гидрофильные или гидрофобные?
- •11. Влияние температуры на термодинамические параметры поверхностного слоя – Us , qs , σ, Ss. (Вывод и анализ уравнения Гиббса-Гельмгольца для поверхностного слоя).
- •12. Адгезия и когезия. Какими силами они обусловлены? Что понимается под работой адгезии и когезии? Вывод уравнений, используемых для вычисления работы адгезии (Дюпре) и работы когезии.
- •13. Что такое аэрозоли? Приведите примеры аэрозолей бытовых, атмосферных и промышленных.
- •14. Рассмотрите процесс смачивания в зависимости от соотношения работы адгезии и когезии (вывод и анализ уравнения Юнга-Дюпре).
- •15. Теория кинетики быстрой коагуляции м. Смолуховского: основные положения; вывод и анализ уравнения, представляющего кинетику изменения общего числа частиц в процессе коагуляции? (Схож с 74)
- •16. Каковы условия поднятия жидкостей в капиллярах? Какова роль этого явления в природе и технике?
- •19. Рассмотрите возможные механизмы возникновения двойного электрического слоя (дэс) на границе раздела твердое тело – раствор.
- •21. В чем заключается инверсия смачивания? Какое практическое значение имеет это явление?
- •22. Какие величины используют для количественного описания адсорбции? Дайте определение этих величин и покажите, как их можно вычислить в общем виде.
- •23. Почему в случае смачивания капилляра жидкость в нем поднимается, а при несмачивании, наоборот, опускается?
- •25. Какие поверхностные явления сопровождают технологические процессы? Перечислите и дайте их краткую характеристику.
- •26. Теория мономолекулярной адсорбции Ленгмюра: основные положения теории, вывод уравнения изотермы адсорбции и ее анализ.
- •29. Смачивание: покажите взаимосвязь между адгезией и способностью жидкости смачивать твердую поверхность. В чем состоит различие между явлениями адгезии и смачивания?
- •30. Чем объяснить, что концентрация кислорода в воздухе земной атмосферы уменьшается в два раза при удалении от поверхности Земли на 5 км, а суспензии гуммигута на высоте 30 мкм?
- •31. По каким признакам классифицируют дисперсные системы? Привести их классификацию по всем классификационным признакам.
- •32. В чем заключается сущность ионообменной адсорбции? Какое состояние называется ионообменным равновесием? Какая величина его характеризует?
- •33. Что такое расклинивающее давление и каковы причины его возникновения? Назовите составляющие расклинивающего давления и охарактеризуйте их.
- •34. Адсорбция на границе раздела раствор – газ (воздух). Вывод и анализ уравнения адсорбции Гиббса для разбавленных растворов бинарной системы.
- •35. Зависимость термодинамической реакционной способности от дисперсности.
- •37. Кинетическая устойчивость. Связь между кинетической устойчивостью и гипсометрическим законом.
- •38. Как, используя уравнение Шишковского, можно определить константы уравнения Ленгмюра (к и а).
- •40. Свойства поверхностей жидких и твердых тел. Каковы особенности адсорбции пав из растворов на поверхности твердого тела?
- •41. Дайте сравнительную характеристику мономолекулярной и полимолекулярной адсорбции. Приведите основные типы изотерм для полимолекулярной адсорбции.
- •42. Дайте характеристику двойного электрического слоя на границе раздела фаз твердое тело – раствор. Как изменяется потенциал в этом слое с расстоянием от поверхности твердой фазы?
- •43. Что понимается под термином “разрушение дисперсной системы”, какая устойчивость при этом теряется? Правила электролитной коагуляции лиофобных золей.
- •44. Капиллярные явления. Поднятия и опускания жидкости в капиллярах: уравнение Жюрена, его вывод и анализ.
- •46. Поверхностная энергия и равновесная форма тела: правило Гиббса-Кюри для твердых и жидких тел.
- •47. Электрокинетические явления 1-го рода, история их открытия и практическое приложение. Как по скорости электрофореза и электроосмоса можно вычислить электрокинетический потенциал?
- •48. Как объяснить зависимость, установленную правилом Дюкло-Траубе?
- •50. Дайте полную характеристику дисперсной системы. Классификационная характеристика этих систем по агрегатному состоянию дисперсной фазы и дисперсионной среды, по виду дисперсной фазы.
- •51. Представьте, что Вам необходимо сделать доклад по теме “Эмульсии”. Напишите план доклада и составьте к нему тезисы.
- •55. Каковы возможные механизмы образования на поверхности раздела фаз двойного электрического слоя.
- •57. Составьте задачу, для решения которой нужно использовать правило Панета-Фаянса.
- •58. Чем обусловлено светорассеяние в дисперсных системах и истинных растворах? Какими параметрами характеризуют рассеяние света в системе?
- •59. Электрокинетические явления 2-го рода: история их открытия, характеристика и практическое приложение.
- •61. Какова взаимосвязь давления насыщенного пара с кривизной поверхности: вывод и анализ уравнения Томсона-Кельвина.
- •63. Каков физический смысл термина “поверхностная активность”? к каким веществам применяется этот термин? Дайте их характеристику и приведите полную классификацию по всем классификационным признакам.
- •64. Дайте характеристику коллоидных растворов (золей) по всем классификационным признакам. Чем они отличаются от суспензий. Приведите примеры таких систем.
- •65. Что представляет собой релаксационный эффект, электрофоретическое торможение и поверхностная проводимость? Как их нужно учитывать при определении величины -потенциала?
- •70. Какая связь существует между уравнениями Гиббса и Ленгмюра? Напишите уравнение, выражающее эту взаимосвязь, и поясните физико-химический смысл входящих в него величин.
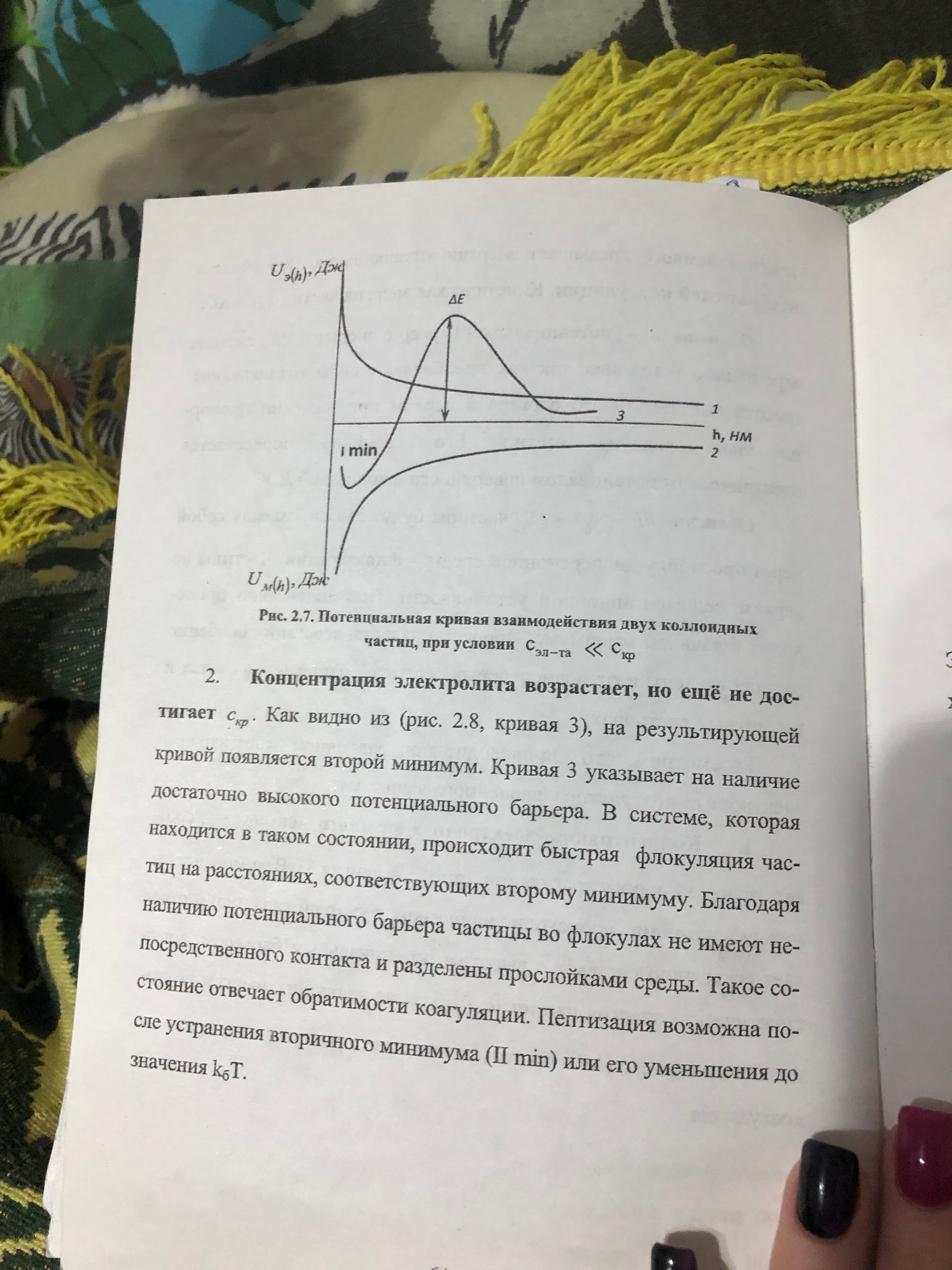
- •72. Что представляют собой потенциальные кривые взаимодействия между коллоидными частицами? Как на их основе объясняют явление коагуляции?
- •75. Что понимается под работой адсорбции? Как, используя это понятие, можно объяснить связь поверхностной активности пав с длиной углеводородного радикала в молекуле пав (правило Дюкло-Траубе).
16. Каковы условия поднятия жидкостей в капиллярах? Какова роль этого явления в природе и технике?
Поднятие и опускание жидкостей в капиллярах
Наиболее распространенный пример капиллярных явлений – это подъем или опускание жидкостей в узких трубках (капиллярах) и в пористых средах. Эти явления обусловливают многие процессы, происходящие в природе и технике (миграция воды в почвах и других пористых телах, капиллярная пропитка всевозможных материалов, широко применяемая в различных процессах химической технологии).
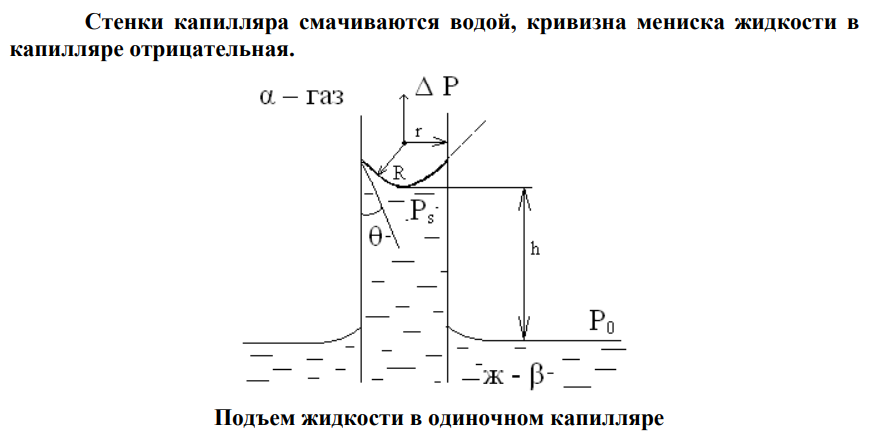


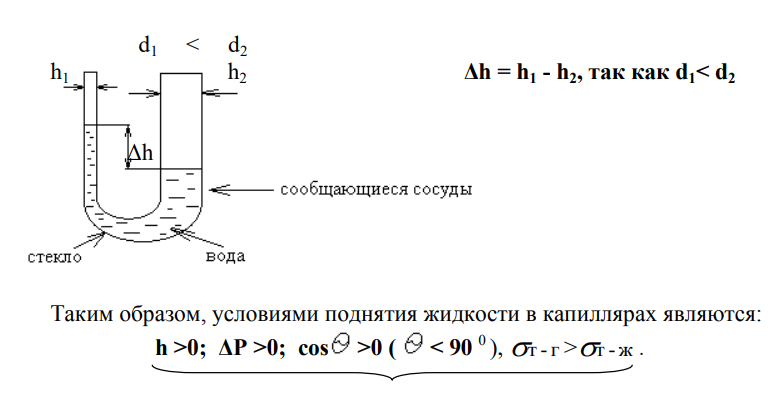

Значение капиллярных явлений
Роль капиллярных явлений в природе и технике огромна. Ими обусловлено проникновение жидкости по тонким каналам в почвах и растениях, пропитка бумаги, тканей, появление сырости в подвалах зданий. Водонепроницаемость тканей обеспечивается их гидрофобностью, то есть отрицательным значением величины высоты капиллярного поднятия жидкости.
17. Что понимается под поверхностной активностью, мерой поверхностной активности? Какие вещества являются поверхностно-активными? Дайте характеристику этих веществ и приведите различные принципы их классификации. (Похож на 63)
Для установления зависимости адсорбционной способности вещества от его состава введено понятие поверхностной активности
Вещества, уменьшающие поверхностное натяжение растворителя, называются поверхностно-активными веществами (ПАВ); увеличивающем – поверхностно-инактивными (ПИВ); не влияющие на поверхностное натяжение растворителя – поверхностно-неактивными (ПНВ).
Характеризует природу вещества. Чем сильнее уменьшается поверхностное натяжение с увеличением концентрации тем выше поверхностная активность.
Физический смысл: это сила, удерживающая вещество на поверхности, рассчитанная на единицу гиббсовской адсорбции.
Количественной мерой поверхностной активности, т.е. способности ПАВ изменять поверхностное натяжение, служит величина производной . Ее обозначают через g и выражают в Дж•м/моль или Н•м2/моль:
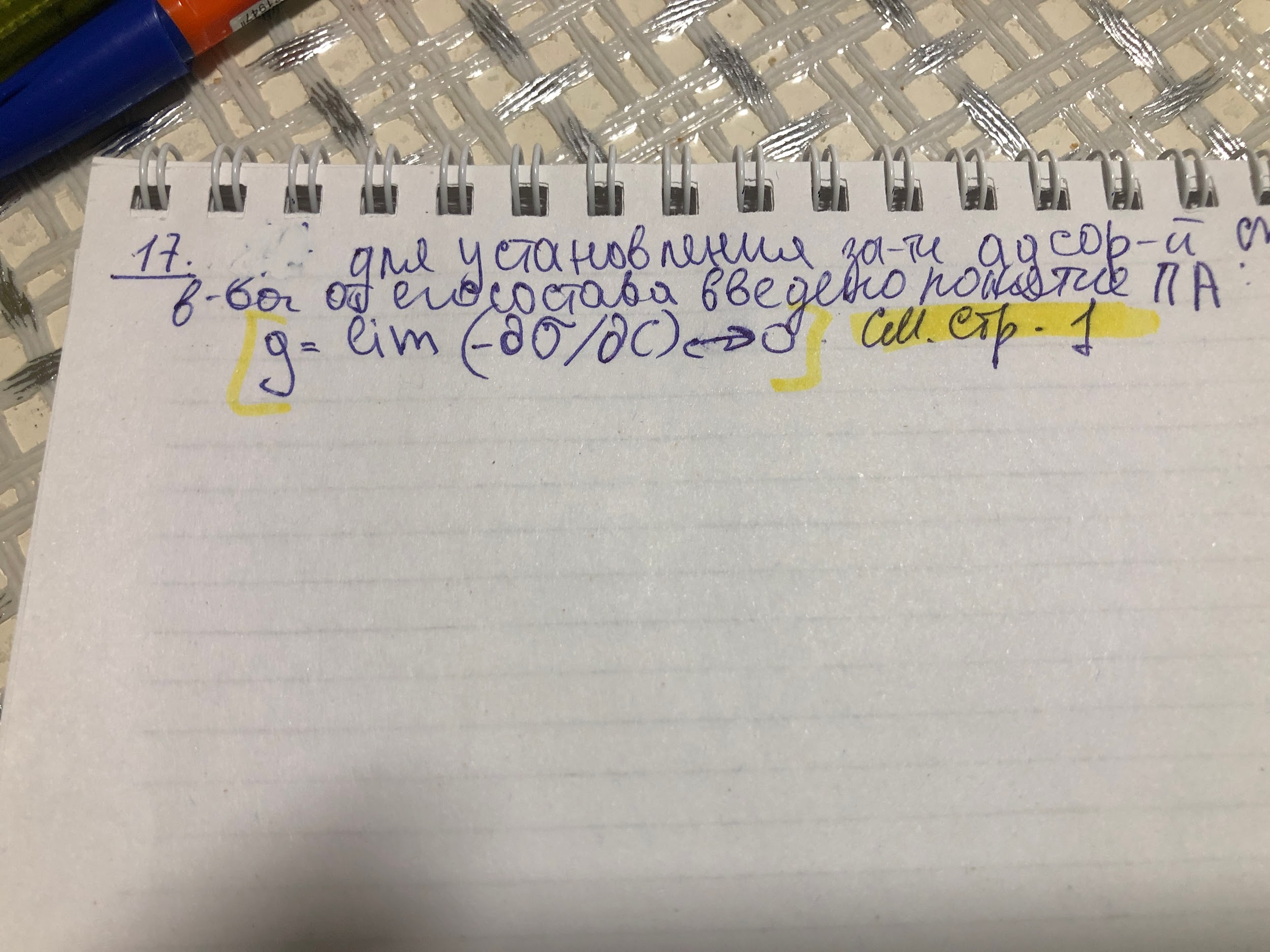
Характеристика и классификация, какие ПАВ смотреть 63 вопрос
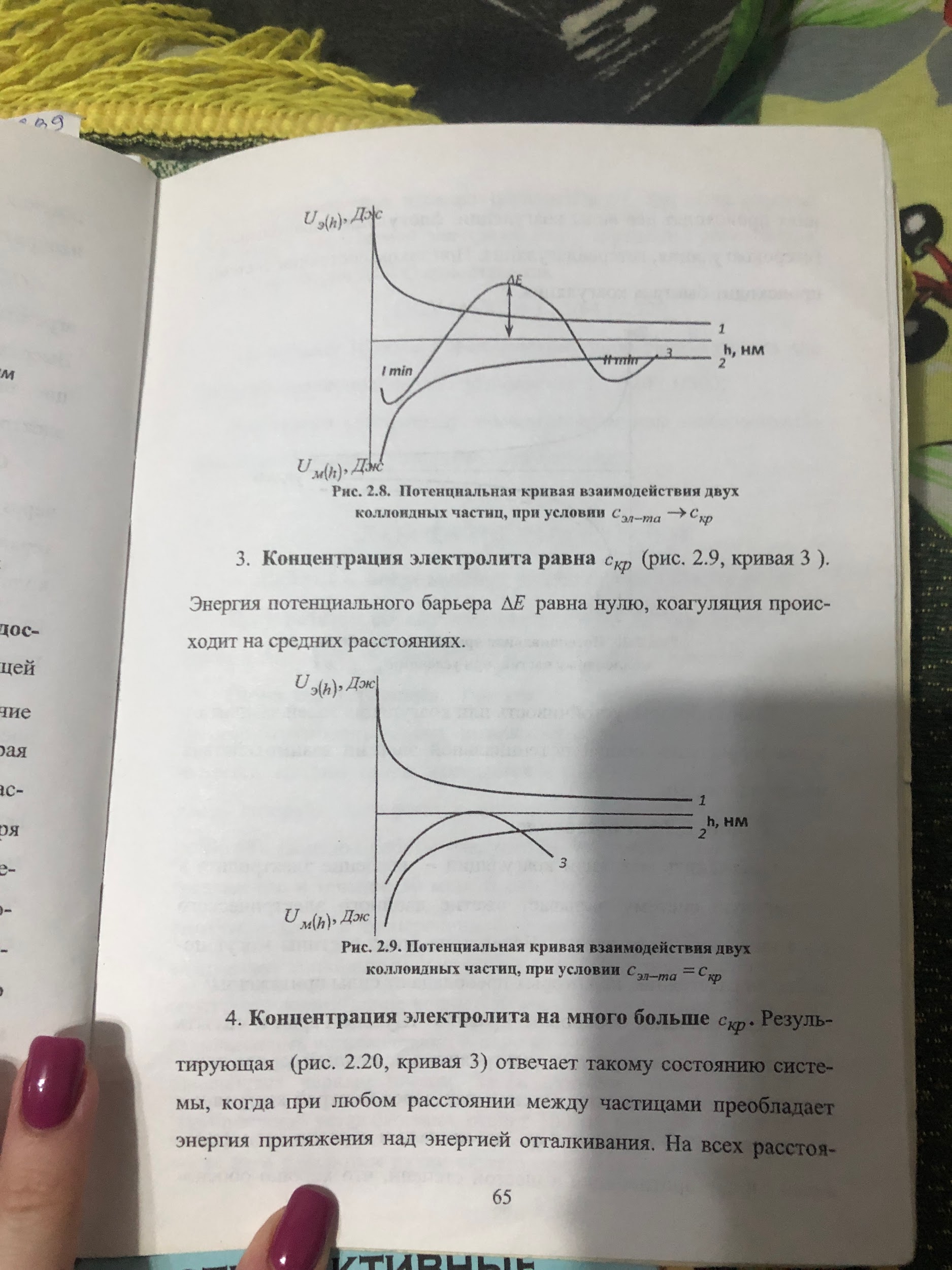
18. Рассмотрите количественную интерпретацию сил электростатического отталкивания и молекулярного притяжения в соответствии с теорией ДЛФО с использованием потенциальных кривых (зависимостей энергий взаимодействия между частицами от расстояния между ними).






19. Рассмотрите возможные механизмы возникновения двойного электрического слоя (дэс) на границе раздела твердое тело – раствор.
Двойной электрический слой возникает при контакте двух фаз, из которых хотя бы одна является жидкой. Стремление системы понизить поверхностную энергию приводит к тому, что частицы на поверхности раздела фаз ориентируются особым образом. Вследствие этого контактирующие фазы приобретают заряды противоположного знака, но равной величины, что приводит к образованию двойного электрического слоя. Можно выделить три механизма образования ДЭС:
Переход ионов или электронов из одной фазы в другую (поверхностная ионизация). Примером может служить диссоциация поверхностных функциональных групп, принадлежащих одной из фаз (как правило, твердой). Для определения знака заряда поверхности используется правило Фаянса — Панета
Преимущественная адсорбция в межфазном слое ионов одного знака.
Ориентирование полярных молекул в поверхностном слое. По этому механизму ДЭС образуется в случае, если вещества, составляющие фазы системы, не могут обмениваться зарядами. Для определения знака заряда поверхности используют правило Кёна, гласящее, что из двух соприкасающихся фаз положительно заряжается та, которая имеет большую диэлектрическую проницаемость.
20. Что понимается под дисперсной системой? Каковы ее отличительные признаки и качественные особенности? По какому признаку дисперсные системы делят на лиофильные и лиофобные? Дайте полную характеристику этих систем.
Дисперсная система - гетерофазная система (состоит из двух и более фаз), при условии взаимной нерастворимости фаз. Она состоит из дисперсионной среды - непрерывной - и дисперсных частиц - раздробленных.
*формулировка ЖИ: Дисперсная система гетерогенна (гетерофазна), в ней одно в-во раздроблено в другом при условии взаимной нерастворимости.
Дисперсная фаза: раздробленная, дискретная (тв. частицы, капли жидкости, пузырьки газа, волокна, нити)
Дисперсионная среда: сплошная, непрерывная (газ/жидкость/тв. тело)
Качественные особенности: большая удельная поверхность раздела фаз; избыточная энергия на поверхности раздела фаз; интенсификация всех процессов за счет кривизны поверхности частиц.
Отличительные признаки: гетерогенность и дисперсность
Лиофильные (любящие среду): эти системы не обладают внутренней гетерогенностью в зависимости от природы дисперсионной среды, они могут быть и гомогенными и гетерогенными. Поэтому в этих системах отсутствует избыточная поверхностная энергия (ΔG<0). Они термодинамически устойчивы. К ним относятся р-ры ПАВ, р-ры ВМС, р-ры некоторых глин (бентонитовая), которые способны к набуханию и самопроизвольному диспергированию.
Лиофобные (боящиеся среды): гетерогенные системы, ΔG>0, поэтому они термодинамически неустойчивы. Для достижения термодинамической устойчивости, к ним добавляется электролит-стабилизатор. К ним относятся все системы с жидкой дисперсионной средой.
