
- •2. Особенности адсорбции на поверхности твердого адсорбента. Уравнение Фрейндлиха, его анализ и определение констант уравнения.
- •3. Что понимается под поверхностным слоем, поверхностной энергией и поверхностными явлениями. Какие параметры относятся к количественным характеристикам дисперсности? Дайте их полную характеристику.
- •4. Представьте, что Вам необходимо сделать доклад по теме: “Суспензия”. Напишите план доклада и в соответствии с ним составьте тезисы доклада.
- •5. Что понимается под поверхностным натяжением и как оно зависит от природы веществ, образующих поверхность раздела фаз?
- •6. Что такое капиллярное давление? Каковы причины его возникновения? Вывод и анализ уравнения Лапласа.
- •8. Поверхностное натяжение: причины возникновения, его физический смысл с термодинамической и силовой точек зрения, определение и методы измерения.
- •9. Что такое агрегативная устойчивость? Факторы, обеспечивающие агрегативную устойчивость лиофобных золей.
- •10. Характеристика порошков как дисперсных систем. Какие порошки обладают более высокой текучестью – грубодисперсные или высокодисперсные? Какие порошки легче распылять гидрофильные или гидрофобные?
- •11. Влияние температуры на термодинамические параметры поверхностного слоя – Us , qs , σ, Ss. (Вывод и анализ уравнения Гиббса-Гельмгольца для поверхностного слоя).
- •12. Адгезия и когезия. Какими силами они обусловлены? Что понимается под работой адгезии и когезии? Вывод уравнений, используемых для вычисления работы адгезии (Дюпре) и работы когезии.
- •13. Что такое аэрозоли? Приведите примеры аэрозолей бытовых, атмосферных и промышленных.
- •14. Рассмотрите процесс смачивания в зависимости от соотношения работы адгезии и когезии (вывод и анализ уравнения Юнга-Дюпре).
- •15. Теория кинетики быстрой коагуляции м. Смолуховского: основные положения; вывод и анализ уравнения, представляющего кинетику изменения общего числа частиц в процессе коагуляции? (Схож с 74)
- •16. Каковы условия поднятия жидкостей в капиллярах? Какова роль этого явления в природе и технике?
- •19. Рассмотрите возможные механизмы возникновения двойного электрического слоя (дэс) на границе раздела твердое тело – раствор.
- •21. В чем заключается инверсия смачивания? Какое практическое значение имеет это явление?
- •22. Какие величины используют для количественного описания адсорбции? Дайте определение этих величин и покажите, как их можно вычислить в общем виде.
- •23. Почему в случае смачивания капилляра жидкость в нем поднимается, а при несмачивании, наоборот, опускается?
- •25. Какие поверхностные явления сопровождают технологические процессы? Перечислите и дайте их краткую характеристику.
- •26. Теория мономолекулярной адсорбции Ленгмюра: основные положения теории, вывод уравнения изотермы адсорбции и ее анализ.
- •29. Смачивание: покажите взаимосвязь между адгезией и способностью жидкости смачивать твердую поверхность. В чем состоит различие между явлениями адгезии и смачивания?
- •30. Чем объяснить, что концентрация кислорода в воздухе земной атмосферы уменьшается в два раза при удалении от поверхности Земли на 5 км, а суспензии гуммигута на высоте 30 мкм?
- •31. По каким признакам классифицируют дисперсные системы? Привести их классификацию по всем классификационным признакам.
- •32. В чем заключается сущность ионообменной адсорбции? Какое состояние называется ионообменным равновесием? Какая величина его характеризует?
- •33. Что такое расклинивающее давление и каковы причины его возникновения? Назовите составляющие расклинивающего давления и охарактеризуйте их.
- •34. Адсорбция на границе раздела раствор – газ (воздух). Вывод и анализ уравнения адсорбции Гиббса для разбавленных растворов бинарной системы.
- •35. Зависимость термодинамической реакционной способности от дисперсности.
- •37. Кинетическая устойчивость. Связь между кинетической устойчивостью и гипсометрическим законом.
- •38. Как, используя уравнение Шишковского, можно определить константы уравнения Ленгмюра (к и а).
- •40. Свойства поверхностей жидких и твердых тел. Каковы особенности адсорбции пав из растворов на поверхности твердого тела?
- •41. Дайте сравнительную характеристику мономолекулярной и полимолекулярной адсорбции. Приведите основные типы изотерм для полимолекулярной адсорбции.
- •42. Дайте характеристику двойного электрического слоя на границе раздела фаз твердое тело – раствор. Как изменяется потенциал в этом слое с расстоянием от поверхности твердой фазы?
- •43. Что понимается под термином “разрушение дисперсной системы”, какая устойчивость при этом теряется? Правила электролитной коагуляции лиофобных золей.
- •44. Капиллярные явления. Поднятия и опускания жидкости в капиллярах: уравнение Жюрена, его вывод и анализ.
- •46. Поверхностная энергия и равновесная форма тела: правило Гиббса-Кюри для твердых и жидких тел.
- •47. Электрокинетические явления 1-го рода, история их открытия и практическое приложение. Как по скорости электрофореза и электроосмоса можно вычислить электрокинетический потенциал?
- •48. Как объяснить зависимость, установленную правилом Дюкло-Траубе?
- •50. Дайте полную характеристику дисперсной системы. Классификационная характеристика этих систем по агрегатному состоянию дисперсной фазы и дисперсионной среды, по виду дисперсной фазы.
- •51. Представьте, что Вам необходимо сделать доклад по теме “Эмульсии”. Напишите план доклада и составьте к нему тезисы.
- •55. Каковы возможные механизмы образования на поверхности раздела фаз двойного электрического слоя.
- •57. Составьте задачу, для решения которой нужно использовать правило Панета-Фаянса.
- •58. Чем обусловлено светорассеяние в дисперсных системах и истинных растворах? Какими параметрами характеризуют рассеяние света в системе?
- •59. Электрокинетические явления 2-го рода: история их открытия, характеристика и практическое приложение.
- •61. Какова взаимосвязь давления насыщенного пара с кривизной поверхности: вывод и анализ уравнения Томсона-Кельвина.
- •63. Каков физический смысл термина “поверхностная активность”? к каким веществам применяется этот термин? Дайте их характеристику и приведите полную классификацию по всем классификационным признакам.
- •64. Дайте характеристику коллоидных растворов (золей) по всем классификационным признакам. Чем они отличаются от суспензий. Приведите примеры таких систем.
- •65. Что представляет собой релаксационный эффект, электрофоретическое торможение и поверхностная проводимость? Как их нужно учитывать при определении величины -потенциала?
- •70. Какая связь существует между уравнениями Гиббса и Ленгмюра? Напишите уравнение, выражающее эту взаимосвязь, и поясните физико-химический смысл входящих в него величин.
- •72. Что представляют собой потенциальные кривые взаимодействия между коллоидными частицами? Как на их основе объясняют явление коагуляции?
- •75. Что понимается под работой адсорбции? Как, используя это понятие, можно объяснить связь поверхностной активности пав с длиной углеводородного радикала в молекуле пав (правило Дюкло-Траубе).
72. Что представляют собой потенциальные кривые взаимодействия между коллоидными частицами? Как на их основе объясняют явление коагуляции?
Потенциальные кривые взаимодействия между частицами представляют собой зависимости сил электростатического отталкивания и молекулярного притяжения от расстояния между частицами. Результирующая энергия взаимодействия между частицами представлена кривой 3. Область 1- ближний минимум, преобладают силы притяжения, он отвечает непосредственному взаимодействию частиц в результате броуновского движения. Это область быстрой( необратимой) коагуляции. Область 2- система агрегативно устойчива, так как преобладают силы электростатического отталкивания. Высота потенциального барьера ΔE пропорциональна радиусу частиц. Область 3- частицы связаны между собой через прослойку дисперсионной среды (флокуляция). Частицы не теряют седиментационной устойчивости. Взаимодействие происходит в дальнем минимуме.

При увеличении концентрации электролита-коагулятора высота потенциального барьера уменьшается, вплоть до его полного исчезновения. Чем выше концентрация электролита-коагулятора, тем быстрее скорость коагуляции. При превышении критической концентрации электролита и исчезновении потенциального барьера происходят все виды коагуляции.
73. Седиментация. Методы седиментационного анализа. Для каких дисперсных систем применяется седиментационный анализ в гравитационном и каких в центробежном поле? Как можно рассчитать радиус частиц дисперсной фазы, которые оседают под действием гравитационной и центробежной силы?
Седиментация-
процесс оседания частиц дисперсной
фазы. Обратная седиментация-всплывание
частиц.
Седиментационный анализ-
принцип седиментационного анализа
основан на измерении скорости оседания
частиц дисперсной фазы в какой-либо
вязкой дисперсионной среде. Скорость
оседания пропорциональна квадрату
размеров частиц, и измерив ее, можно
легко найти средние размеры частиц
суспензии. Преимуществом этого метода
анализа перед микроскопическим или
ситовым является то, что он позволяет
определять размеры частиц в довольно
большом интервале. Он крайне прост и
удобен в аппаратурном оформлении и в
выполнении. Область дисперсности,
охватываемая седиментационным анализом
( 10^-7 - 10^-4), позволяет применять его в
самых разных областях для контроля
дисперсности.
Методы седиментационного
анализа в гравитационном
поле:
-отмучивание;
-отбор проб
осадка и взвешивание его после сушки
или измерение объема осадка в процессе
его накопления;
-пипеточный;
-определение
концентрации на различной глубине
суспензии оптическим методом;
-определение
изменения гидростатического давления
столба суспензии в процессе ее оседания;
-
весовые методы, основанные на изучении
процесса накопления осадка на чашке
гидростатических весов.
Отмучивание-
многократное отделение части суспензии
с частицами, меньшими чем rкр. Важно при
подготовке суспензии к седиментационному
анализу.
Пипеточный метод основан
на взятии пробы пипеткой с определенной
глубины. Затем взвешивают либо сухой
остаток пробы, либо определяют ее
плотность пикнометрическим методом.
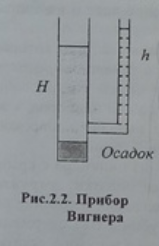
Метод
измерения гидростатического давления
столба суспензии предложен Вигнером.
Гидростатическое давление измеряют с
помощью сообщающихся сосудов.
Широкая
трубка наполняется суспензией, а узкая-
чисто дисперсионной средой. Высоты
столбов этих жидкостей обратно
пропорциональны их плотностям. В процессе
оседания осадок накапливается на дне
трубки и плотность суспензии уменьшается,
в результате чего уменьшается и разность
уровней столбов жидкостей. Разность
высот столбов в каждый момент времени
пропорциональна массе осевшего вещества
дисперсной фазы.
Оптические методы основаны на определении концентрации оседающего вещества оптическим методом. Абсорбция света при прохождении через слой суспензии определяется концентрацией частиц, размерами, формой и условиями их нахождения во взвешенном состоянии в данной среде. Весовые методы седиментационного анализа основаны на измерении увеличения массы осадка за определенное время на чашке гидростатических весов.
Определение
размера частиц в гравитационном поле:

74. Как по степени коагуляции можно сделать вывод, будет ли коагуляция медленной или быстрой? Изложите основные положения теории кинетики быстрой коагуляции. Как изменится суммарная численная концентрация частиц от времени коагуляции ? (ПОХОЖ НА 15)
Степень коагуляции – это отношение числа столкновений, которые приводят к слипанию, к общему числу столкновений.

Если =1, то коагуляция быстрая, если =0, коагуляции нет, а если между – медленная коагуляция.
В качестве меры агрегативной устойчивости дисперсной системы можно рассматривать скорость ее коагуляции.
Скорость коагуляции – изменение частичной концентрации дисперсных частиц в единице объема в единицу времени.
Скорость коагуляции может быть самой разной в различных системах (от нескольких секунд до нескольких лет). Система тем более устойчива, чем медленнее она коагулирует.
Различают: быструю коагуляцию, при которой каждое столкновение частиц приводит к их слипанию (все соударения эффективны); и медленную коагуляцию, когда не все столкновения частиц являются эффективными.
Теория кинетики быстрой коагуляции однородных сферических частиц была разработана польским ученым М. Смолуховским в 1916 г.
Основные положения теории быстрой коагуляции Смолуховского:
частицы дисперсной фазы сближаются в результате броуновского движения, слипаются, образуют агрегат, который совершает дальнейшее броуновское движение как единое целое;
скорость сближения частиц определяется коэффициентом диффузии и средним расстоянием между частицами;
в каждом элементарном акте участвуют только две частицы дисперсной фазы;
все частицы имеют одинаковый размер и обладают одинаковой подвижностью, форму частиц считают сферической.
Кинетика изменения общего числа частиц в процессе коагуляции в теории Смолуховского:
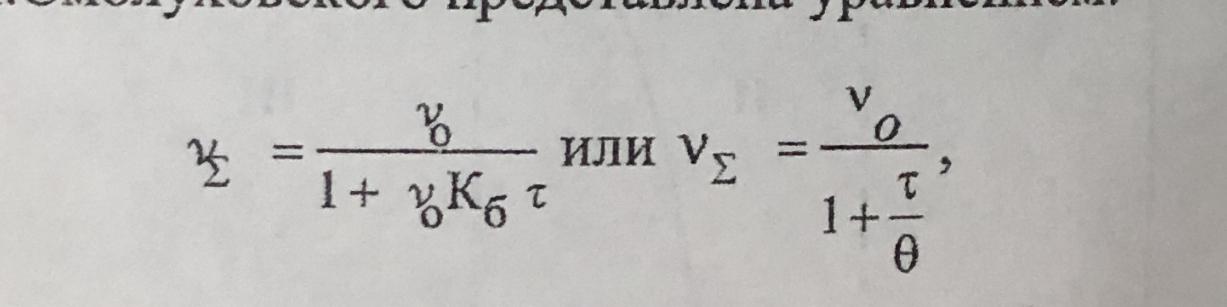

Начальная концентрация: v0=c/m
с — массовая концентрация, кг*м^-3, m — масса частиц дисперсной фазы, кг.
Масса частиц: m=Vp=(4/3) π r^3p (p это плотность, r— радиус)

Теория Смолуховского также позволяет вычислить расстояния, на которые должны приблизится центры двух частиц для того, чтобы произошло их слияние.
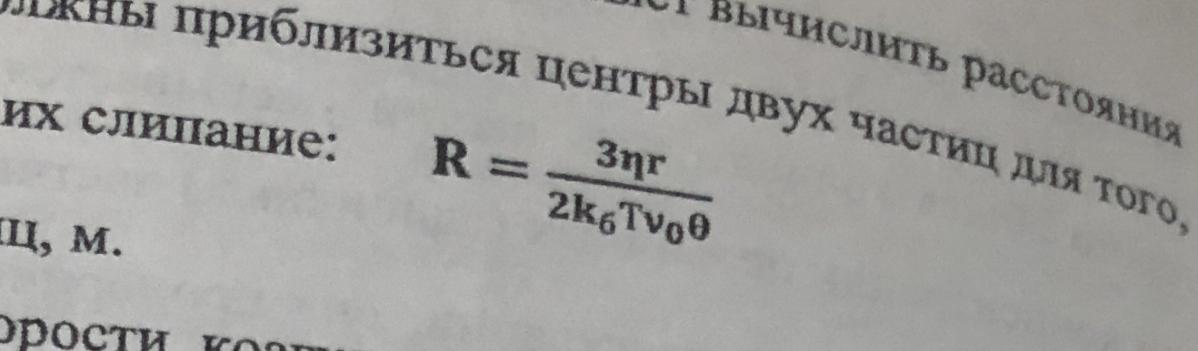
Константу скорости коагуляции определяет соотношение:
K=kб*Рехр[-ΔE/(kб*T)]
P — стерический множитель, учитывающий благоприятное пространственное расположение частиц при столкновении, их форму, размеры.
ΔE — потенциальный барьер
Если ΔE=0, Р=1, то коагуляция быстрая
Если ΔE не равно нулю и Р не равно 1, то медленная коагуляция
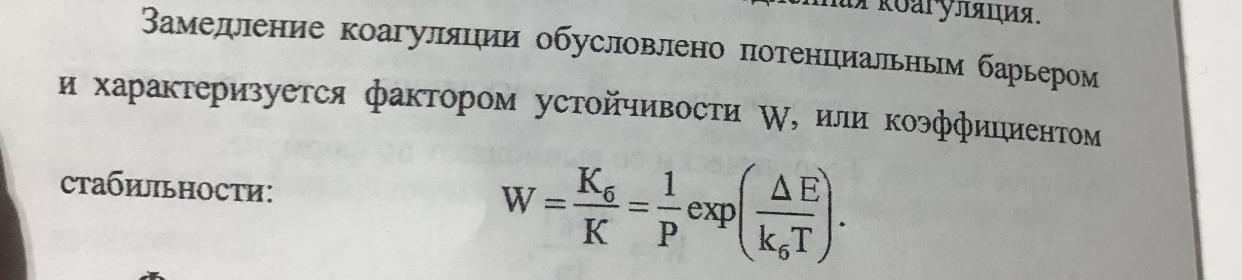
Фактор устойчивости показывает во сколько раз константы скорости медленной коагуляции меньше константы быстрой коагуляции
При высоком значении потенциального барьера может наступить такое состояние системы, когда скорость агрегации будет равна скорости дезагрегации.
В этом случае система становится термодинамически устойчивой к коагуляции
