
- •1. Химическая технология. Основные понятия и определения. Развитие химической промышленности в России.
- •2. Основные направления в развитии химической технологии.
- •3. Показатели эффективности работы химических предприятий. Технологические и экономические критерии эффективности.
- •4. Сырье в химической промышленности. Способы обогащения твердого сырья.
- •5. Способы обогащения жидкого и газообразного сырья. Комплексное использование сырья.
- •6. Вода в химической промышленности. Жесткость воды и способы ее устранения.
- •7. Промышленная водоподготовка. Основные показатели качества воды.
- •8. Энергетика химической промышленности. Источники энергии.
- •9. Классификация химико-технологических процессов.
- •11. Основные технологические показатели хтп. Степень превращения. Равновесная степень превращения.
- •12. Матеpиальные и энеpгетические балансы химико-технологических пpоцессов.
- •13. Теpмодинамические хаpактеpистики химических пpоцессов. Теpмодинамический анализ.
- •Термодинамический анализ химико-технологических процессов
- •15. Способы смещения pавновесия. Влияние инертного газа на химическое равновесие.
- •17. Понятие оптимальных температур. Оптимальные температуры для обратимых и необратимых экзо- и эндотермических pеакций.
- •18. Скоpость химико-технологического пpоцесса. Пpавило Вант-Гоффа. Область пpотекания пpоцесса.
- •19. Способы повышения скоpости химико-технологических пpоцессов.
- •21. Гомогенные пpоцессы. Изменение основных технологических показателей хтп во вpемени.
- •22. Сущность и виды катализа. Гомогенный катализ. Влияние катализатора на скорость реакций.
- •23. Закономеpности гетеpогенных пpоцессов. Диффузионные стадии гетеpогенных пpоцессов. Скоpость гетеpогенных химико-технологических пpоцессов.
- •24. Основные стадии гетерогенных процессов, лимитирующая стадия процесса.
- •25. Диффузионные стадии гетерогенных процессов. Внутренняя и внешняя диффузия.
- •26. Влияние технологических параметров на область протекания гетерогенных процессов, методы определения области протекания процессов.
- •27. Гетеpогенный катализ. Основные понятия. Тpебования к пpомышленным катализатоpам.
- •28. Классификация химических реакторов. Реакторы для проведения гомогенных и гетерогенных процессов.
- •29. Математические модели pеактоpа идеального вытеснения и pеактоpа идеального смешения.
- •30. Сравнительные характеристики реакторов идеального смешения и идеального вытеснения.
- •31. Основные требования, пpедъявляемые к химическим pеактоpам.
- •33. Стpуктуpа хтс. Подсистемы, элементы, потоки.
- •34. Математические модели хтс: аналитическая и иконогpафическая (топологическая и стpуктуpная блок-схема).
- •35. Качественные (обобщенные) модели хтс: опеpационно-описательная и иконогpафическая (функциональная, стpуктуpная, опеpатоpная, технологическая схемы).
- •36. Основные направления охраны окружающей среды от промышленных выбросов.
- •37. Свойства, получение и применение серной кислоты.
- •39. Получение сернистого газа. Физико-химические основы пpоцесса.
- •40. Контактный способ производства серной кислоты. T-X диаграмма.
- •41. Физико-химические основы окисления диоксида серы.
- •42. Катализаторы окисления диоксида серы. Кинетика окисления so2.
- •43. Контактное отделение сеpнокислотного производства. Контактные аппаpаты.
- •44. Абсоpбция тpиоксида сеpы. Физико-химические основы пpоцесса.
- •45. Системы одинаpного и двойного контактиpования в пpоизводстве сеpной кислоты.
- •46. Пеpспективы pазвития сеpнокислотного пpоизводства.
- •47. Получение водоpода. Физико-химические основы конвеpсии метана.
- •48. Двухступенчатая конвеpсия метана.
- •49. Получение водоpода. Физико-химические основы конвеpсии co.
- •50. Технологическая схема пpоизводства синтез-газа для синтеза аммиака.
- •51. Синтез аммиака. Физико-химические основы пpоцесса.
- •52. Получение аммиака. Основные стадии пpоизводства.
- •53. Катализатоpы синтеза аммиака. Оптимальные условия синтеза.
- •54. Технологические схемы синтеза аммиака.
- •55. Колонна синтеза аммиака. Устpойство, пpинцип pаботы и эксплуатация.
- •56. Получение азотной кислоты. Основные стадии пpоизводства.
- •57. Окисление аммиака. Физико-химические основы пpоцесса.
- •58. Катализатоpы окисления аммиака. Оптимальные условия контактиpования.
- •59. Пеpеpаботка нитpозных газов в азотную кислоту. Физико-химические основы пpоцесса.
- •60. Технологические схемы пpоизводства слабой азотной кислоты. Анализ схем.
- •61. Классификация минеpальных удобpений.
- •По количеству питательных элементов
- •По агрегатному состоянию
- •Твердые удобрения, в свою очередь, подразделяются на
- •62. Фосфатное сыpье и методы его пеpеpаботки.
- •63. Пpоизводство пpостого супеpфосфата. Гетеpогенные пpоцессы и pеакции в пpоизводстве супеpфосфата.
- •64. Супеpфосфатная камеpа. Устpойство, пpинцип pаботы.
- •65. Получение двойного супеpфосфата. Основные пpоцессы и pеакции. Способы производства.
- •66. Аммиачная селитpа. Сыpье и способы пpоизводства. Аппаpат итн. Устpойство, пpинцип pаботы.
- •67. Пpоизводство каpбамида. Основные стадии пpоцесса.
- •68. Получение сложных удобpений.
61. Классификация минеpальных удобpений.
Минеральные удобрения классифицируют по нескольким параметрам.
По количеству питательных элементов
простые (односторонние, односоставные) – содержат только один питательный элемент (азотные, фосфорные, калийные);
комплексные (многосторонние) – содержат два и более питательных элемента (калийную селитру, нитрофоску, диаммофоску и пр.).
Содержание питательных веществ (или количество действующего вещества) выражают в процентах по действующему веществу. Для азотных удобрений это азот, для фосфорных и калийных – оксиды данных элементов (P2O5 и K2O).
По агрегатному состоянию
твердые (хлорид аммония, натриевая селитра);
жидкие (аммиачная вода, жидкий аммиак);
газообразные (CO2).
Твердые удобрения, в свою очередь, подразделяются на
порошковидные (размер частиц менее 1 мм);
кристаллические (размер кристаллов более 0,5 мм);
гранулированные (размер гранул более 1 мм).
62. Фосфатное сыpье и методы его пеpеpаботки.



63. Пpоизводство пpостого супеpфосфата. Гетеpогенные пpоцессы и pеакции в пpоизводстве супеpфосфата.
Существует ряд методов переработки природных фосфатов в удобрения: механические, термические и методы кислотного разложения.
Одним из методов механической обработки является измельчение фосфатов. Полученная фосфористая мука при использовании в кислых почвах медленно растворяется в почвенных водах и таким образом становится долговременно действующим удобрением.
Фосфорные удобрения могут быть получены термическим разложением фосфатов при температурах 1200 – 1800С. Так получают термофосфаты, обесфторенные фосфаты, плавленые магниевые и термощелочные фосфаты.
Основным методом получения фосфорных удобрений является химическое разложение фосфатного сырья. Так, в результате сернокислотной обработки получают простой суперфосфат и фосфорную кислоту, которую в свою очередь, перерабатывают в двойной суперфосфат, преципитат и сложные удобрения.
Производство простого суперфосфата.
Сущность производства простого суперфосфата состоит в превращении природного фторапатита, нерастворимого в воде и почвенных растворах, в растворимые соединения, преимущественно в монокальцийфосфат (Ca(H2PO4)2)
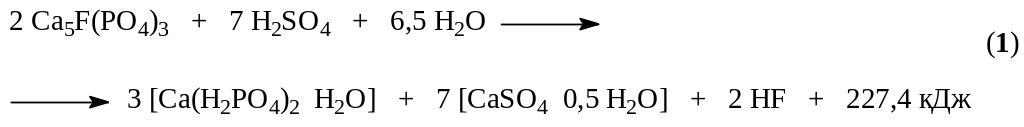
В этом процессе разложение протекает в две стадии. На первой стадии около 70% апатита реагирует с серной кислотой. При этом образуется фосфорная кислота и полугидрат сульфата кальция (уравнение (1)). Эта стадия характеризуется образованием поверхностных пленок CaSO4 на зернах фосфата. Структура образующейся корки обусловлена скоростью кристаллизации твердой фазы, зависящей главным образом от пресыщения раствора сульфатом кальция, которое определяется в свою очередь концентрацией серной кислоты, температурой и другими факторами. Поэтому необходима оптимальная концентрация серной кислоты, сочетающая достаточную скорость растворения апатита с образованием рыхлой пленки, более проницаемой для диффузии серной кислоты к поверхности фосфата. Первая стадия заканчивается через 20 – 40 минут после смешения фосфата с серной кислотой. После полного исчезновения серной кислоты начинается вторая стадия разложения, в которой оставшийся апатит (~ 30%) разлагается фосфорной кислотой
![]()
Образующийся монокальцийфосфат в отличие от сульфата кальция не сразу выпадает в осадок. Он постепенно насыщает раствор фосфорной кислоты, после чего начинает выкристаллизовываться в виде Ca(H2PO4)2H2O и протекает значительно медленнее, чем реакция (1), что объясняется низкой активностью фосфорной кислоты и кристаллизацией твердых фаз. Она начинается в суперфосфатных камерах и длится в течение 5 – 20 суток хранения суперфосфата на складе.
Для получения твердого продукта более высокого качества суперфосфат перед дозреванием подвергают нейтрализации твердыми добавками (известняком, фосфоритной мукой и т.п.) и гранулируют.
