- •1. Химическая технология. Основные понятия и определения. Развитие химической промышленности в России.
- •2. Основные направления в развитии химической технологии.
- •3. Показатели эффективности работы химических предприятий. Технологические и экономические критерии эффективности.
- •4. Сырье в химической промышленности. Способы обогащения твердого сырья.
- •5. Способы обогащения жидкого и газообразного сырья. Комплексное использование сырья.
- •6. Вода в химической промышленности. Жесткость воды и способы ее устранения.
- •7. Промышленная водоподготовка. Основные показатели качества воды.
- •8. Энергетика химической промышленности. Источники энергии.
- •9. Классификация химико-технологических процессов.
- •11. Основные технологические показатели хтп. Степень превращения. Равновесная степень превращения.
- •12. Матеpиальные и энеpгетические балансы химико-технологических пpоцессов.
- •13. Теpмодинамические хаpактеpистики химических пpоцессов. Теpмодинамический анализ.
- •Термодинамический анализ химико-технологических процессов
- •15. Способы смещения pавновесия. Влияние инертного газа на химическое равновесие.
- •17. Понятие оптимальных температур. Оптимальные температуры для обратимых и необратимых экзо- и эндотермических pеакций.
- •18. Скоpость химико-технологического пpоцесса. Пpавило Вант-Гоффа. Область пpотекания пpоцесса.
- •19. Способы повышения скоpости химико-технологических пpоцессов.
- •21. Гомогенные пpоцессы. Изменение основных технологических показателей хтп во вpемени.
- •22. Сущность и виды катализа. Гомогенный катализ. Влияние катализатора на скорость реакций.
- •23. Закономеpности гетеpогенных пpоцессов. Диффузионные стадии гетеpогенных пpоцессов. Скоpость гетеpогенных химико-технологических пpоцессов.
- •24. Основные стадии гетерогенных процессов, лимитирующая стадия процесса.
- •25. Диффузионные стадии гетерогенных процессов. Внутренняя и внешняя диффузия.
- •26. Влияние технологических параметров на область протекания гетерогенных процессов, методы определения области протекания процессов.
- •27. Гетеpогенный катализ. Основные понятия. Тpебования к пpомышленным катализатоpам.
- •28. Классификация химических реакторов. Реакторы для проведения гомогенных и гетерогенных процессов.
- •29. Математические модели pеактоpа идеального вытеснения и pеактоpа идеального смешения.
- •30. Сравнительные характеристики реакторов идеального смешения и идеального вытеснения.
- •31. Основные требования, пpедъявляемые к химическим pеактоpам.
- •33. Стpуктуpа хтс. Подсистемы, элементы, потоки.
- •34. Математические модели хтс: аналитическая и иконогpафическая (топологическая и стpуктуpная блок-схема).
- •35. Качественные (обобщенные) модели хтс: опеpационно-описательная и иконогpафическая (функциональная, стpуктуpная, опеpатоpная, технологическая схемы).
- •36. Основные направления охраны окружающей среды от промышленных выбросов.
- •37. Свойства, получение и применение серной кислоты.
- •39. Получение сернистого газа. Физико-химические основы пpоцесса.
- •40. Контактный способ производства серной кислоты. T-X диаграмма.
- •41. Физико-химические основы окисления диоксида серы.
- •42. Катализаторы окисления диоксида серы. Кинетика окисления so2.
- •43. Контактное отделение сеpнокислотного производства. Контактные аппаpаты.
- •44. Абсоpбция тpиоксида сеpы. Физико-химические основы пpоцесса.
- •45. Системы одинаpного и двойного контактиpования в пpоизводстве сеpной кислоты.
- •46. Пеpспективы pазвития сеpнокислотного пpоизводства.
- •47. Получение водоpода. Физико-химические основы конвеpсии метана.
- •48. Двухступенчатая конвеpсия метана.
- •49. Получение водоpода. Физико-химические основы конвеpсии co.
- •50. Технологическая схема пpоизводства синтез-газа для синтеза аммиака.
- •51. Синтез аммиака. Физико-химические основы пpоцесса.
- •52. Получение аммиака. Основные стадии пpоизводства.
- •53. Катализатоpы синтеза аммиака. Оптимальные условия синтеза.
- •54. Технологические схемы синтеза аммиака.
- •55. Колонна синтеза аммиака. Устpойство, пpинцип pаботы и эксплуатация.
- •56. Получение азотной кислоты. Основные стадии пpоизводства.
- •57. Окисление аммиака. Физико-химические основы пpоцесса.
- •58. Катализатоpы окисления аммиака. Оптимальные условия контактиpования.
- •59. Пеpеpаботка нитpозных газов в азотную кислоту. Физико-химические основы пpоцесса.
- •60. Технологические схемы пpоизводства слабой азотной кислоты. Анализ схем.
- •61. Классификация минеpальных удобpений.
- •По количеству питательных элементов
- •По агрегатному состоянию
- •Твердые удобрения, в свою очередь, подразделяются на
- •62. Фосфатное сыpье и методы его пеpеpаботки.
- •63. Пpоизводство пpостого супеpфосфата. Гетеpогенные пpоцессы и pеакции в пpоизводстве супеpфосфата.
- •64. Супеpфосфатная камеpа. Устpойство, пpинцип pаботы.
- •65. Получение двойного супеpфосфата. Основные пpоцессы и pеакции. Способы производства.
- •66. Аммиачная селитpа. Сыpье и способы пpоизводства. Аппаpат итн. Устpойство, пpинцип pаботы.
- •67. Пpоизводство каpбамида. Основные стадии пpоцесса.
- •68. Получение сложных удобpений.
52. Получение аммиака. Основные стадии пpоизводства.
В лаборатории аммиак получают при взаимодействии солей аммония с щелочами. Поскольку аммиак очень хорошо растворим в воде, для получения чистого аммиака используют твердые вещества.
Например, аммиак можно получить нагреванием смеси хлорида аммония и гидроксида кальция. При нагревании смеси происходит образование соли, аммиака и воды:
2NH4Cl + Са(OH)2 → CaCl2 + 2NH3 + 2Н2O
Тщательно растирают ступкой смесь соли и основания и нагревают смесь. Выделяющийся газ собирают в пробирку (аммиак — легкий газ и пробирку нужно перевернуть вверх дном). Влажная лакмусовая бумажка синеет в присутствии аммиака.
Видеоопыт получения аммиака из хлорида аммония и гидроксида кальция можно посмотреть здесь.
Еще один лабораторный способ получения аммиака – гидролиз нитридов.
Например, гидролиз нитрида кальция:
Ca3N2 + 6H2O → ЗСа(OH)2 + 2NH3
В промышленности аммиак получают с помощью процесса Габера: прямым синтезом из водорода и азота.
N2 + 3Н2 ⇄ 2NH3
Процесс проводят при температуре 500-550оС и в присутствии катализатора. Для синтеза аммиака применяют давления 15-30 МПа. В качестве катализатора используют губчатое железо с добавками оксидов алюминия, калия, кальция, кремния. Для полного использования исходных веществ применяют метод циркуляции непровзаимодействовавших реагентов: не вступившие в реакцию азот и водород вновь возвращают в реактор.
Технологический процесс производства аммиака в общем виде можно представить 8-ю стадиями:
компрессия природного газа,
сероочистка природного газа,
конверсия метана,
конверсия окиси углерода с установкой разгонки газового конденсата,
очистка конвертированного газа от двуокиси углерода,
метанирование,
компрессия азото-водородной смеси
синтез.
53. Катализатоpы синтеза аммиака. Оптимальные условия синтеза.
Наибольшей активностью обладают металлы восьмой группы таблицы Менделеева (Fe; Ru; Re и Os). В промышленности применяют железный катализаторы. Их получают сплавлением оксидов железа (FeO + Fe2O3) с активаторами и последующим восстановлением оксидов железа. В качестве активаторов применяют кислотного и амфотерного характера (Al2O3; SiO2; TiO2 и др.), а так оксиды щелочных и щелочноземельных металлов (K2O; Na2O; CaO; MgO и др.). Полученный катализатор имеет марку СА-1.
Восстановление смеси оксидов железа производится водородом по реакции:
(FeO+Fe2O3) + 4Н2 ⇔ 3Fe + 4Н2О - Q.
Образующееся железо имеет тонкопористую губчатую структуры с большой удельной поверхностью.
54. Технологические схемы синтеза аммиака.
Синтез аммиака осуществляется из азота и водорода по реакции: N 2 + 3Н 2 ⇔ 2 NН 3 + Q, Реакция обратимая, экзотермическая и характеризуется большим тепловым эффектном. Согласно принципу Ле-Шателье равновесие ее смещается вправо с повышением давления и понижением температуры.
55. Колонна синтеза аммиака. Устpойство, пpинцип pаботы и эксплуатация.
Таким образом, скорость реакции и, следовательно, производительность цеха синтеза аммиака в сильной степени зависит от объемной скорости, температуры процесса и давления с системе.
На рисунке 4.8 приведена технологическая схема производства аммиака при среднем давлении:
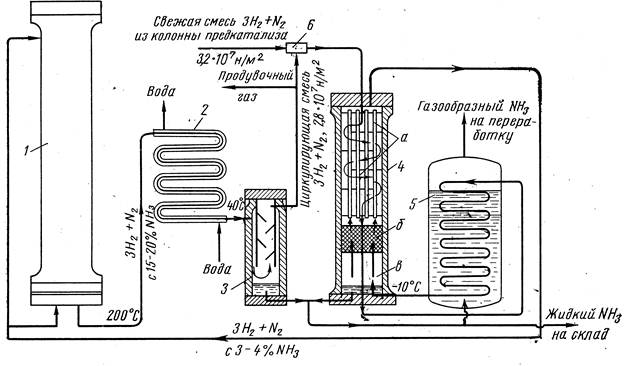
Рис. 4.8. Схема установки синтеза аммиака при среднем давлении:
1 - колонна синтеза; 2 - водяной конденсатор; 3 - газоотделитель; 4 - конденсационная колонна (а - теплообменник, б - насадка из керамических колец, в - газоотделитель); 5 - испаритель жидкого аммиака; 6 - инжектор для смешения свежей и циркулирующей АВС.
Рассмотрим элементарную технологическую схему современного производства аммиака при среднем давлении производительностью 1360 т/сутки. Режим ее работы характеризуется следующими параметрами:
- температура контактирования 450 – 550 °С,
- давление 32 МПа,
- объемная скорость газовой смеси 4×104 нм3/м3×ч.
- стехиометрический состав АВС (азотоводородной смеси)
Режим работы установки характеризуется следующими параметрами:
- температураконтактирования 450-500ºС;
- давление32 МПа.
1. Смесь циркуляционного газа и свежая порция АВС, сжатая до 32 МПа, подаётся в колонну синтеза, где происходит образование аммиака.
2. Выходящий из колонны синтеза газ, содержащий до 20% NH3, подвергается2-х стадийной конденсации с цельюотделения аммиака в жидком и газообразном виде.
Первая стадия конденсации:
- циркуляционный газ последовательно проходит через водяной холодильник и холодильник-конденсатор;
- при прохождении газа через холодильники вследствие снижения температуры происходит конденсация газообразного аммиака с образованием жидкого аммиака;
- в результате этого жидкий аммиак отделяется от циркуляционного газа и поступает на складготовой продукции.
Вторая стадия конденсации состоит из 3-х операций:
а) первая операция: циркуляционный газ смешивается сосвежейпорцией АВС и поступает в конденсационную колонну.
б) вторая операция: в конденсационной колонне газ постепенно охлаждается до -10ºС. При прохождении газа через теплообменник конденсационной колонны вследствие снижения температуры происходит конденсацияосновной частигазообразного аммиака с образованием жидкого аммиака.Часть жидкого аммиаканаправляется насклад готовой продукции, а частьпоступает в испаритель жидкого аммиака.
в) третья операция: в испарителе жидкого аммиака при охлаждениидо -20ºС происходит испарение жидкого аммиака с образованием товарного газообразного продукта.
После чего смесь циркуляционного газа, содержащего до 3-4% аммиака и АВС, вновь подают в колонну синтеза.
Цикл замыкается!!!
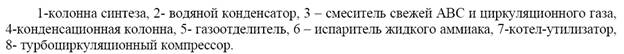
Смесь свежей АВС и циркуляционного газа под давлением подается из смесителя 3 в конденсационную колонну 4, где из циркуляционного газа конденсируется часть аммиака, откуда поступает в колонну синтеза 1. Выходящий из колонны газ, содержащий до 0.2 объемной доли аммиака направляется в водяной холодильник-конденсатор 2 и затем в газоотделитель 5, где из него отделяется жидкий аммиак. Оставшийся газ после компрессора смешивается со свежей АВС и направляется сначала в конденсационную колонну 4, а затем в испаритель жидкого аммиака 6, где при охлаждении до -20 °С также конденсируется большая часть аммиака. Затем циркуляционный газ, содержащий около 0.03 об. долей аммиака, поступает в колонну синтеза 1. В испарителе 6, одновременно с охлаждением циркуляционного газа и конденсацией содержащегося в нем аммиака, происходит испарение жидкого аммиака с образованием товарного продукта.
Основной аппарат технологической схемы – колонна синтеза аммиака. Колонна состоит из корпуса и насадки, включающей катализаторную коробку в которой размещена контактная масса, и систему теплообменных труб.
Для процесса синтеза аммиака существенное значение имеет оптимальный температурный режим.
Для обеспечения максимальной синтеза процесс следует начинать при высокой температуры и по мере увеличения степени превращения понижать ее. Регулирование температуры и обеспечение автотермичности процесса обеспечивается с помощью теплообменников, расположенных в слое контактной массы и дополнительно, подачей части холодной АВС в контактную массу, минуя теплообменник.
Для снижения температуры стенок холодная азотоводородная смесь, поступающая в колонну синтеза, проходит вдоль внутренней поверхности цилиндрического корпуса колонны. Применяют полочные и трубчатые колонны.
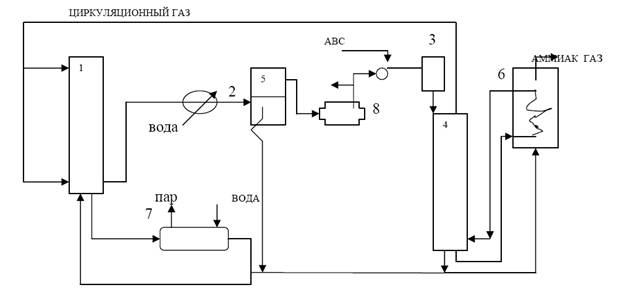
На рисунке показана трубчатая колонна синтеза аммиака для системы среднего давления, представляющая собой цилиндр из хромоникелевой стали с толщиной стенок 175 мм, диаметром 1,2 - 1,4 м и высотой 24 м. В верхней части колонны находится катализаторная коробка 3, а в нижней – теплообменник 8, обеспечивающий автотермичность процесса. Катализатор загружается на колосниковую решетку 6. Для обеспечения равномерного распределения температуры в слой катализатора вводятся двойные трубы, выполняющие функции теплообменника. Основной газ, поступающий в колонну синтеза сверху, проходит вдоль стенок внутреннего стакана в межтрубном пространстве теплообменника 1 и, нагреваясь за счет теплоты процесса катализа, по центральной трубе 7 поднимается в надкаталитическое пространство. Затем азоводородная смесь распределяется по теплообменным трубкам, опускается по центральной теплообменной трубке вниз и, поднимаясь вверх по кольцевому пространству между внутренней и внешней трубками, нагревается до температуры реакции, охлаждая контактную массу. Далее газ фильтруется через катализатор, на котором происходит синтез. Аммиачно-азотоводородная смесь при 500 °С поступает в трубное пространство теплообменника и нагревает свежую порцию азотоводородной смеси. Для регулирования температурного режима в зоне катализатора предусматривается подача части (холодного) газа снизу через центральную трубку, минуя теплообменные устройства.
Основной аппарат для синтезааммиака – колонна синтеза (рисунок 4.10). Колонна состоит из корпуса и насадки.
|
Рис 4.10. Колона синтеза аммиака среднего давления: 1 - кольцевое пространство между корпусом колонны 2 и стенками 3 катализаторной коробки; 4 и 5 - теплообменник; 6 - колосниковая решётка; 7 - центральная труба; 8 - второй теплообменник; 9 - труба для дополнительной подачи АВС (байпас) |
Насадка состоит: из катализаторной коробки, с размещённой в ней контактной массой, и системы теплообменных труб.
|
В настоящее время применяют полочные колонны синтеза, в которых катализатор находится на полках, размещённых в катализаторной коробке.
Количествокатализатора на полках колонны увеличивается по мере сниженияскорости газа и снижениистепени превращения АВС.
Регулирование температур и обеспечение автотермичности процесса обеспечивается с помощью системывнешних теплообменников и теплообменников, расположенных в слое контактной массы.
Внешний теплообменник находится в нижней части колонны, под катализаторной коробкой. В нём происходит теплообмен между горячим газом, отходящим из колонны, и холодной АВС.