
3 курс / Фармакология / ФАРМАКОЛОГИЯ_ПРЕПАРАТОВ_НА_ОСНОВЕ_ПРИРОДНЫХ_АЛЮМОСИЛИКАТОВ_И_ИХ
.pdf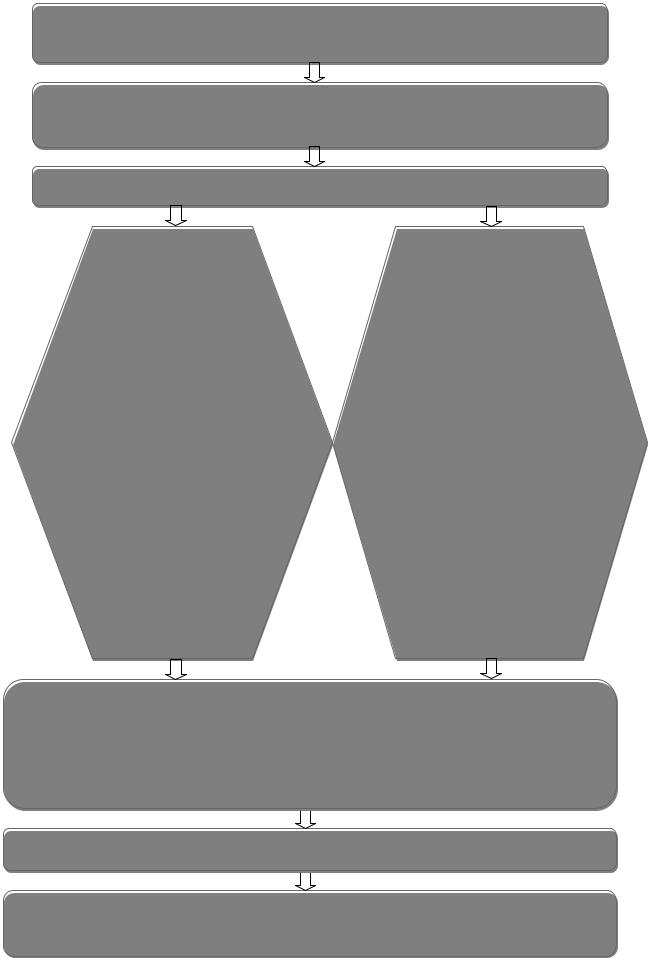
Алгоритм исследований
Разработка препаратов на основе матрицы природных алюмосиликатов
Определение минерального состава и уровня тяжелых металлов, изучение физико-химических свойств
Фармако-токсикологическая оценка
Параметры токсичности:
острая и хроническая токсичность;
местнораздражающее и кожно-резорбтивное действие;
эмбриотоксическое и тератогенное действие;
влияние на функции же- лудочно-кишечного тракта, печень, почки;
патоморфологичесие и гистологические исследования;
ВСЭ продукции после
Фармакологические свойства препаратов:
исследование влияния препаратов на обмен веществ;
исследование влияния препаратов на морфологические показатели крови и уровень железа, на обменные процессы и на показатели неспецифической резистентности;
исследование влияния на заживление ран.
|
Лечебно-профилактическая эффективностьпри: |
–диспепсиях; |
– анемии; |
–гастроэнтеритах; |
– гипокупрозе; |
– гипотрофии; |
– микотоксикозах; |
– колибактериозе; |
– вторичных иммунодефицитах; |
– коррекции минерального обмена;– метаболических нарушениях функциипечени
Экономическая эффективность
Производственные испытания, разработка наставлений по применению
71
Рекомендовано к изучению сайтом МедУнивер - https://meduniver.com/
Лабораторные животные содержались в условиях, соответствующих санитарным правилам по устройству, оборудованию и содержанию экспери-
ментально-биологических клиник (вивариев), в помещениях с температурой
22–24º С, в клетках типового типа на деревянно-стружечной подстилке, с от-
носительной влажностью воздуха 40–50 %, при естественном световом ре-
жимесогласно предъявляемым требованиям по содержанию лабораторных животных (методические рекомендации по содержанию лабораторных жи-
вотных в вивариях научно-исследовательских институтов и учебных заведе-
ний, РД-АПК 3.10.07.02-09) и правил лабораторной практики при проведе-
нии доклинических исследований (ГОСТ 351000.3-964100.4-96).
Изучение токсикологических свойств препаратов проводили на ин-
тактных крысах (нелинейных), мышах, кроликах, поросятах и цыплятах-
бройлерах. В токсикологических опытах использовали здоровых половозре-
лых животных обоих полов, одинакового возраста и массы.
Исследования острой и хронической токсичности препаратов проводи-
ли согласно существующим методикам и нормативным документам: «Мето-
ды определения токсичности и опасности химических веществ (токсикомет-
рия)» (под редакцией Саноцкого И.В., 1970); «Научно-методологические ас-
пекты исследования токсических свойств фармакологических лекарственных средств для животных (Смирнов А.М., Дорожкин В.И., 2008); «Методиче-
ские указания по токсико-экологической оценке лекарственных средств,
применяемых в ветеринарии» (Всесоюзный НИИ незаразных болезней жи-
вотных, Воронеж, 1988).
Определение острой токсичности препаратов осуществляли по методу Г.Н. Першина (1950) и методу Deiсhmann и Le Blank (1943) на белых мышах,
белых крысах и кроликахпутем однократного внутрижелудочного введения в
дозах, многократно превышающих лечебные и профилактические с целью установления (LD50 и LD100). Исследуемые препараты по степени опасности классифицировали согласно ГОСТу 12-1-007-76.
72
Показателями определения острой токсичности служили: внешний вид животных, состояние кожного покрова, поведение (возбуждение или угнете-
ние, подвижность, изменение походки, реакции на внешние раздражения,
выделения из глаз, рта, мышечные подергивания, тремор, судороги, парали-
чи, парезы и т.д.), картина интоксикации, количество погибших и выживших животных.
Параметры субхронической и хронической токсичности препаратов изучали по общепринятым методикам на белых крысах, поросятах и цыпля-
тах-бройлерах. Препараты задавались внутрь индивидуально ежедневно натощак в течение 28 (субхроническая токсичность) и 60-ти (хроническая токсичность) дней по непрерывной схеме в трех дозах, руководствуясь ре-
зультатами, полученными при исследовании острой токсичности.
При ежедневных наблюдениях за животными учитывалось общее со-
стояние и поведение (аппетит, возбуждение или угнетение), изменения реак-
ций на внешние раздражители и функций органов пищеварения и мочеотде-
ления, динамика прироста массы тела. Отмечались клинические симптомы отравления, количество заболевших и павших животных.
Функциональное состояние мочевыделительной системы определяли по диурезу и клиническому анализу мочи. Моча отбиралась до кормления в утрен-
ние часы в момент свободного мочеиспускания. В моче определяли цвет, кон-
систенцию, запах, концентрацию водных ионов, удельный вес, содержание бел-
ка, углеводов, гемоглобина, желчных пигментов при помощи специальных по-
лосок для биохимического анализа мочи фирмы DEKA PHAN Leuco.
Влияние на функцию пищеварительной системы оценивали по физико-
химическим исследованиям фекалий животных и помета птицы, в которых определяли консистенцию, цвет, запах, наличие примесей, растительную клет-
чатку, жировые капли и крахмал, нейтральный жир, переваримую клетчатки,
эритроциты, эпителиальные клетки, лейкоциты, билирубин и скрытую кровь.
73
Рекомендовано к изучению сайтом МедУнивер - https://meduniver.com/
Местно-раздражающее действие веществ определяли методом накож-
ных аппликаций и конъюнктивальных проб согласно «Методическим указа-
ниям, по токсикологической оценке, новых препаратов для лечения и профи-
лактики незаразных болезней животных» (1987). О наличии у препаратов раз-
дражающих свойств судили по появлению на месте аппликации гиперемии,
отека, расчесов, появлению корок и трещин. При исследовании местного дей-
ствия на слизистые глаз обращали внимание на появление гиперемии, отечно-
сти склеры и роговицы, ширину зрачка (миоз, мидриаз) и состояние век.
Выявление отдаленных последствий проводили общепринятыми мето-
дами, оценивая влияние препаратов на эмбриональное развитие и генератив-
ную функцию самок белых крыс, а также физиологическое состояние рож-
денного от них потомства. За молодняком, полученным от крыс, используе-
мых в опытах, вели наблюдения. Показателями общего постнатального раз-
вития служили динамика массы тела крысят, время открытия глаз, появление шерсти, двигательная активность, способность координации движений и вы-
живаемость.
Изучение влияния препаратов на макро- и микроструктуры внутренних органов проводилось в ходе экспериментов по их длительному применению лабораторным и сельскохозяйственным животным. В качестве объекта при гистологическом исследовании использовались кусочки сердца, легких, пе-
чени, почек, селезенки, желудка, кишечника, которые фиксировались в 10%-
ном растворе нейтрального формалина. После фиксации органы заливали в парафин, готовили срезы толщиной 4-6 мкм, окрашивали гематоксилин-
эозином и микроскопировали. Исследования проводились под микроскопом МС 300 (страна-производитель Австрия), при увеличении х5, х10. Критерия-
ми оценки гистологических изменений являлось состояние ткани органа,
стромы, сосудов, нервов, наличие дистрофических и воспалительных процес-
сов, степень однородности ткани и др.
74
Ветеринарно-санитарную экспертизу туш и внутренних органов после применения препаратов проводили на кроликах, свиньях и птице в установ-
ленном порядке, которая включала в себя органолептическую и дегустацион-
ную оценку мяса и жира с обязательными токсикологическим, бактериологи-
ческим и физико-химическим исследованиями согласно ГОСТ 7269-79,
ГОСТ 23392-78, ГОСТ Р 53221-2008, ГОСТ 31470-2012.
Изучение фармакотерапевтического действия препаратов проводи-
лось на сельскохозяйственных животных и птице для оценки фармакодина-
мических эффектов, и лечебно-профилактической эффективности. Группы животных комплектовали по принципу аналогов, с учетом породы, пола,
массы, возраста, условий содержания и кормления. Количество животных в группах определяли целесообразностью объективной оценки полученных ре-
зультатов и их статистической достоверности. Кормление осуществлялось в соответствии с общепринятыми нормами и рационами с учетом технологиче-
ских и физиологических особенностей для разных видов сельскохозяйствен-
ных животных и птицы.
Фармакодинамику препаратов определяли по их влиянию на показате-
ли белкового, углеводного, липидного, минерального обмена веществ, состо-
яние органов кроветворения (эритро- и гемопоэз), на иммунологические по-
казатели и нормализации физиологических функций органов и систем.
За всеми животными в течение периода назначения препаратов еже-
дневно проводились клинические наблюдения, учитывалось общее состоя-
ние, аппетит, продуктивность, заболеваемость и сохранность. Показателем продуктивности служили приросты массы тела животных.
Потребление корма, а также кормов с добавлением исследуемых препа-
ратов в каждой группе животных и птицы рассчитывали ежедневно, начиная с первого дня эксперимента и в дальнейшем в течение всего периода опыта. Со-
гласно полученным количественным данным рассчитывали затраты кормов на одну голову и 1 кг прироста массы тела животного и птицы (конверсия).
75
Рекомендовано к изучению сайтом МедУнивер - https://meduniver.com/
Терапевтические свойства препаратов изучали на больных животных,
профилактические – на клинически здоровых, после предварительного об-
следования, включающего осмотр, термометрию и лабораторные исследова-
ния крови. В ходе экспериментов оценивали общее состояние, упитанность,
отставание в росте и развитии.
Лечебно-профилактическое действие препаратов изучали при анемии, гипо-
купрозе и гипотрофии поросят, заболеваниях желудочно-кишечного тракта (дис-
пепсия, гастроэнтерит, колибактериоз) молодняка сельскохозяйственных живот-
ных (поросята, телята), микотоксикозах, метаболических нарушениях функции печени, при коррекции минерального обмена, вторичных иммунодефицитах.
Влияние на заживление ран изучали на белых крысах и поросятах при внутреннем и наружном применении препарата.
Критерием эффективности препаратов служили результаты комплекс-
ных клинических, биохимических, гематологических методов исследования,
а также контрольного взвешивания. Лечебно-профилактическую эффектив-
ность определяли в сравнении с широко применяемыми в данных показаниях препаратами и отрицательным контролем.
Трупы павших и убитых животных подвергали патологоанатомическо-
му вскрытию. Вскрытие проводили общепринятыми методами. С помощью штангенциркуля и электронных аналитических весов «Acculab» определяли линейные размеры и массы паренхиматозных органов.
Послеубойный ветеринарно-санитарный осмотр тушек животных выпол-
няли общепринятыми методами, руководствуясь «Правилами ветеринарного осмотра убойных животных и ветеринарно-санитарной экспертизы мяса и мяс-
ных продуктов» (1988), «Правилами ветеринарно-санитарного осмотра убойных животных и ветеринарно-санитарной экспертизы мясных продуктов» (2001).
Описание структуры опытов, а также специфики проводимых экспери-
ментов в зависимости от целей и задач исследований представлено в соответ-
ствующих главах диссертационной работы.
76
Для гематологических исследований кровь у поросят получали из со-
судов уха и хвоста, у телят – из яремной вены, цыплят-бройлеров – подкры-
ловой вены, у кроликов – из вены Сафена, у крыс кровь отбиралась при дека-
питации (из сердца).
Во всех случаях кровь бралась с соблюдением правил асептики и антисеп-
тики, место венепункции выстригали и дезинфицировали 70%-ным раствором этилового спирта. Для получения плазмы использовались пробирки с антикоагу-
лянтом (ЭДТА), сыворотки – пробирки с активатором свертывания крови.
Морфологические исследования крови. Исследования проводили на ве-
теринарном гематологическом анализаторе ABACUS (Diatron, Австрия), ско-
рость оседания эритроцитов (СОЭ) определяли микрометодом Панченкова
(Кондрахин И.П., Таланов Г.А., Пак В.В., 2003)
Биохимические исследования крови. Основные биохимические показате-
ли определяли на автоматическом химическом анализаторе – Vitalab Selectra
Junior с версией программного обеспечения 1.0. (открытая система для прове-
дения фотометрических тестов, изготовитель Vital Scientific N. V. Netherlands)
с использование реактивов фирмы ELITech Clinical Systems (Франция) и
Аnalyticon biotechnologies AG (Германия); микроэлементы – методом атомно-
адсорбционной спектрометрии на приборе «Квант-2» (Россия).
В сыворотке крови определяли: концентрацию общего белка; содержа-
ние общего и прямого билирубина; активность аланинаминотрансферазы
(АлАТ), аспартатаминотрансферазы (АсАТ) и щелочной фосфатазы (ЩФ);
содержание мочевины и креатинина; холестерин и триглицериды; содержа-
ние микроэлементов (Ca, P, Zn, Cu, Fe, Мg). Белковые фракции сыворотки крови определяли нефелометрическим методом.
Иммунологические исследования. Исследования иммунного статуса включали в себя морфологические исследования крови (определение общего количества лейкоцитов в счетной камере с сеткой Горяева, лейкоформулу – дифференциальным подсчетом форменных элементов белой крови на мазках)
77
Рекомендовано к изучению сайтом МедУнивер - https://meduniver.com/
и иммунологические (уровень фагоцитоза – постановкой опсонофагоцитар-
ной реакции; фагоцитарную активность – по проценту фагоцитирующих нейтрофилов к общему числу подсчитанных; фагоцитарный индекс – по чис-
лу микробных клеток в пересчете на один нейтрофил от общего количества подсчитанных нейтрофилов; фагоцитарное число – по числу микробных кле-
ток в пересчете на один активный фагоцитирующий нейтрофил; фагоцитар-
ную емкость – по числу фагоцитирующих нейтрофилов в 1 мкл крови; сти-
мулированный НБТ-тест – в реакции восстановления нитросинего тетразо-
лия; популяции Т- и В-лимфоцитов – методом розеткообразования; количе-
ственное определение IgA, IgM, IgG – путем простой радиальной иммуно-
диффузии; бактерицидную активность – фотонефелометрическим методом при учете изменения оптической плотности питательной среды при добавле-
нии в нее сыворотки крови, лизоцимную активность – нефелометрически по изменению оптической плотности суспензии Microcos Lyzodeiticus после добавления в нее сыворотки крови).
Для оценки эндогенной интоксикации определялся уровень среднемо-
лекулярных пептидов – молекул средней массы (МСМ) в сыворотке крови животных. Для диагностики использовали метод, предложенный Н.И. Габри-
элян и др. (1985). Принцип метода заключается в осаждении белков раство-
ром трихлоруксусной кислоты, с последующим определением МСМ путем прямой спектрофотометрии при длине волны 254 и 280 нм в единицах опти-
ческой плотности. Оценку показателей системы ПОЛ-АОЗ проводили в соот-
ветствии с методическим пособием ВНИВИПФиТ (1997) по изучению про-
цессов перекисного окисления липидов и системы антиоксидантной защиты организма животных.
Статистическая обработка результатов. Полученные в опытах циф-
ровые данные обрабатывались методами математической статистики, приня-
той в биологии и медицине (Лакин Г.Ф., 1990), с помощью программного
78
обеспечения фирмы Mikrosoft ®, фирмы Carl Zeiss ®. Критерий достоверно-
сти определяли по таблице Стьюдента.
С целью получения среднего показателя (М) для обработки данных ис-
следования использовались методы описательной статистики c последую-
щим проведением множественного парного сравнения с помощью критерия Ньюмена-Кейлса при 5% уровне значимости различий (р≤0,05).
Кроме того, проведен расчет экономической эффективности примене-
ния изучаемых препаратов по «Методике определения экономической эф-
фективности ветеринарных мероприятий» (1982).
79
Рекомендовано к изучению сайтом МедУнивер - https://meduniver.com/
3.СОБСТВЕННЫЕ ИССЛЕДОВАНИЯ
3.1Изучение химического состава природных алюмосиликатов Краснодарского края и Воронежской области, и препаратов на их основе
На территории Краснодарского края имеются следующие месторожде-
ния природных алюмосиликатов (бентонитовых глин): Горячеключевское,
Черноморское (Абинский район), Варениковское (Крымский район), Госта-
гаевское (Анапский район), Бесленевское (Мостовский район), Зассовское
(Лабинский район).
Методом РФА, электронно-микроскопического и электронно-
графического изучения установлено, что образцы природных глин данных месторождений представляют собой полиминеральную систему, основным минералом которой является монтмориллонит (60-70%) – сорбционно-
активный глинистый минерал группы смектитов с идеализированной форму-
лой Al2[Si4O10] (OH)2·nH2O (Рекшинская Л.Г., 1966), с примесью каолинита,
цеолита, вермикулита, иллита и др.
Согласно энергодисперсионному спектру в монтмориллонитах отмеча-
ется наличие в составе следующих элементов: кремния, алюминия, железа,
кальция, калия, магния и др., удельная поверхность составляет 53 м²/г, объем пор – 0,065 см³/г, средний размер мезопор – 4,8 нм, микропор – 1,23 нм; вы-
явлено подавление роста Escherichia coli в 10 раз, подавление роста
Staphylococcus aures – в 10 раз (Бондарев А. В., 2015).
Для изучения физико-химических, а в дальнейшем и фармакологиче-
ских свойств, были отобраны пробы глин голубовато-зеленого и зеленовато-
желтого оттенка Горячеключевского, Черноморского, Гостагаевского и Ва-
рениковского месторождений.
После проведенного мониторинга химического состава этих глин (таб-
лица 2) было обнаружено, что данные пробы глин отличаются повышенным содержанием железа, т.е. по сути, являются монтмориллонитами железистого профиля – нонтронитами (ферримонтмориллонитами).
80
